Газета «Новости медицины и фармации» 7(320) 2010
Вернуться к номеру
Выбор метаболической терапии при лечении больных с ишемической болезнью сердца
Авторы: В.З. Нетяженко, Т.И. Мальчевская, Г.И. Мишанич, Т.Д. Залевская, А.Г. Машкевич.
Национальный медицинский университет имени А.А. Богомольца, г. Киев
Версия для печати
 Лечение ишемической болезни сердца (ИБС) продолжительное время рассматривалось с позиций улучшения кардиогемодинамики. Известно, что патогенетически обусловленное действие традиционных лечебных средств направлено на снижение потребности миокарда в кислороде или на увеличение поступления кислорода в кардиомиоцит. Препараты, которые влияют на гемодинамические параметры, эффективны, когда речь идет о профилактике приступов стенокардии, но фактически не защищают клетку миокарда от ишемических изменений.
Лечение ишемической болезни сердца (ИБС) продолжительное время рассматривалось с позиций улучшения кардиогемодинамики. Известно, что патогенетически обусловленное действие традиционных лечебных средств направлено на снижение потребности миокарда в кислороде или на увеличение поступления кислорода в кардиомиоцит. Препараты, которые влияют на гемодинамические параметры, эффективны, когда речь идет о профилактике приступов стенокардии, но фактически не защищают клетку миокарда от ишемических изменений.
Вот почему в последние десятилетия научный поиск фармакологов, фармацевтов и клиницистов был направлен на синтез, создание и внедрение в медицинскую практику кардиопротекторов — средств, которые успешно устраняют нарушение клеточного метаболизма, ионного гомеостаза и функций мембран кардиомиоцитов, предупреждая развитие необратимых процессов в миокарде. И на сегодняшний день метаболическая терапия полноправно заняла ведущее место в схемах лечения сердечно-сосудистой патологии, войдя в международные рекомендации [1–4].
Возникновение метаболического подхода в лечении ИБС традиционно связывают с глюкозо-инсулино-калиевой смесью (ГИК), которую в 1962 году D. Sodi-Pallaris и соавт. впервые применили в нерандомизированном исследовании и показали, что ГИК положительно влияет на динамику ЭКГ при остром инфаркте миокарда, улучшает раннюю выживаемость. В последующих исследованиях было продемонстрировано, что ГИК, как и никотиновая кислота, снижает высвобождение свободных жирных кислот (СЖК) адипозоцитами, а это, в свою очередь, способствует снижению концентрации СЖК в зоне ишемизированного миокарда. Полученные данные позволили сделать вывод о том, что, блокируя окисление СЖК, можно достичь значительной активации окисления глюкозы. Именно такой фармакологический подход получил наибольшее распространение в метаболической терапии ИБС и стабильной стенокардии напряжения. Вот почему оптимальным эффектом метаболической терапии считают улучшение эффективности поглощения кислорода миокардом в условиях ишемии [7, 14, 16, 18].
Арсенал медикаментозных средств с признанным метаболическим действием из года в год пополняется. В кардиологической практике широко применяются препараты с метаболическим действием, среди которых признаны такие, как триметазидин, ранолазин, Тиотриазолин, L-карнитин, милдронат, мексикор, кверцетин, кардонат, а в неврологической — актовегин, мексидол, ноотропил, инстенон, Тиоцетам, с присущей им наибольшей тропностью к миокарду или нервной ткани. Большинство средств прошли сравнительные исследования и подтвердили свою клиническую эффективность. Положительными свойствами метаболических средств являются полное отсутствие нежелательных гемодинамических влияний, хорошая переносимость пациентами всех возрастных групп, направленность влияния на глубинные метаболические механизмы развития ишемии и кардиоцитопротекции. Рациональное образование и использование энергии является ключевым моментом в развитии кардиальной патологии, а средства метаболической направленности повышают стойкость тканей к гипоксии и последствиям реперфузии. В последнее время метаболическая терапия стала одним из направлений в лечении коронарогенной сердечной недостаточности [5, 6].
Неопровержимые доводы фармакологической защиты миокарда при синдроме ишемии—реперфузии нашли свое отображение в рекомендациях Европейского общества кардиологов — ЕОК (2006) относительно назначения метаболической терапии больным со стабильной стенокардией. В частности, ЕОК рекомендовало для уменьшения выраженности симптомов и проявлений ишемии применять по возможности метаболические средства (триметазидин, ранолазин) (класс ІІв) как дополнительную терапию или при непереносимости основной терапии.
Ишемические и реперфузионные синдромы как частые спутники ишемической болезни сердца при атеросклеротическом поражении сосудов и собственно ишемия миокарда характеризуются недостаточным обеспечением тканей кислородом, истощением запасов АТФ и креатинфосфата в кардиомиоците, переключением гликолиза с аэробного на анаэробный путь, усилением внутриклеточного ацидоза, дисфункцией ионных насосных каналов, повышением уровней натрия, кальция, снижением уровней калия в цитоплазме кардиомиоцитов. Разбалансированность окислительно-восстановительных процессов в митохондриях приводит к неограниченному образованию свободных радикалов и других агрессивных факторов, которые не только повреждают клеточную мембрану кардиомиоцита, но и инициируют апоптоз [7, 14, 15, 17, 18]. Нарушение процессов микроциркуляции, активация системы фагоцитирующих мононуклеаров, Т-лимфоцитов и лейкоцитов со структурным поражением левого желудочка — вот неполный перечень многогранности ишемических проявлений.
С учетом разносторонности патогенетических механизмов формирования, прогрессирования ишемической болезни сердца как наиболее распространенного заболевания и разнообразных механизмов защиты миокарда классификация медикаментозных средств с кардиопротекторными свойствами является несколько условной. Так, среди двух широко используемых групп препаратов с кардиопротекторным эффектом выделяют препараты прямого действия, которые непосредственно уменьшают выраженность влияния патогенных факторов на кардиомиоцит, и непрямого действия, которые уменьшают нагрузку на сердечную мышцу. Эффект прямых кардиопротекторов обусловлен местным влиянием на метаболизм непосредственно в кардиомиоцитах, стабилизацией клеточных мембран, расширением коронарных сосудов и центральным влиянием на активность нервных центров, которые регулируют сосудистый тонус [7]. К кардиопротекторам с прямым действием относится и Тиотриазолин — отечественный препарат, который является классическим антиоксидантом. Влияя на энергетические процессы миокарда, он уменьшает потребность миокарда в кислороде. Кроме того, он стабилизирует мембрану кардиомиоцитов, обладает антиаритмическим эффектом, имеет выраженную анаболическую способность.
В условиях гипоперфузии миокарда Тиотриазолин эффективно устраняет дисбаланс в системе адениновых нуклеотидов АТФ — АДФ — АМФ, предотвращает быстрое истощение энергетических ресурсов клеток и переход их метаболизма на энергетически менее выгодный анаэробный путь окисления глюкозы.
Пониженный уровень кретинфосфокиназы при лечении больных со стабильной стенокардией отображает его положительное влияние на энергетический обмен и стабилизацию мембран кардиомиоцитов. В условиях тканевой гипоксии Тиотриазолин способен снижать уровень молочной кислоты в цикле Кребса, а также повышать содержание пировиноградной и яблочной кислот.
Экспериментально установлена способность Тиотриазолина уменьшать на 42 % зону ишемии и некроза миокарда, что статистически достоверно было выше, чем при применении карнитина хлорида как признанного антиоксиданта, и это положительно влияло на показатели ишемического повреждения миокарда.
Кардиопротекторный эффект Тиотриазолина реализовался путем влияния на ишемические изменения биоэнергетического обмена в миокарде, что сопровождалось ростом уровня эндогенного гликогена и уменьшением уровня свободных жирных кислот, что было воспроизведено на животных моделях.
В последнее время показано, что антиангинозное действие свойственно метаболическим препаратам — триметазидину, ранолазину, L-карнитину и отечественному препарату Тиотриазолин.
Многочисленные работы посвящены изучению препарата Тиотриазолин у больных со стабильной стенокардией. Анализ исследований показал, что препарат включали в комплекс метаболической терапии в лечении больных со стабильной стенокардией I–IV ФК и с выраженными ЭКГ-признаками ишемии, постинфарктным кардиосклерозом у лиц преклонного возраста. Если триметазидин существенно не влиял на показатели кардиогемодинамики, статистически достоверно не изменял уровень систолического АД и частоту сердечных сокращений, то при лечении Тиотриазолином больных с постинфарктным кардиосклерозом было установлено улучшение как систолической, так и диастолической функции левого желудочка [10, 11, 13, 15]. Установлено, что комплексная терапия больных с постинфарктной стенокардией при использовании нитросорбида, фенигидина и Тиотриазолина положительно влияет на внутрисердечную гемодинамику не только благодаря снижению преднагрузки (нитросорбид), постнагрузки (фенигидин), но и путем повышения инотропной функции сердца посредством кардиопротекторного действия Тиотриазолина как средства метаболической коррекции ишемизированного миокарда.
В работах, посвященных применению Тиотриазолина у больных с ИБС независимо от функционального класса стенокардии в сочетании с гипертонической болезнью, показано благоприятное влияние препарата на течение заболевания. Отмечено уменьшение выраженности болевого синдрома и восстановление сердечного ритма у этой группы больных. У больных со стенокардией уменьшалось количество ангинозных приступов, увеличивалась толерантность к физическим нагрузкам и уменьшалась гиперлипидемия [7, 9, 12].
Интересным для нас оказалась экстраполяция механизма действия Тиотриазолина относительно других кардиопротекторов. Одним из таких препаратов считается триметазидин, который рассматривается как эталонный кардиопротектор, внесенный ЕОК в рекомендации по лечению стабильной стенокардии (2006). Известно, что Тиотриазолин в условиях гипоксии уменьшает зону некроза и степень деструктивных изменений в миокарде. Тиотриазолин, как и триметазидин, является препаратом метаболического действия: оба препарата нормализуют нарушение энергетического обмена.
Благодаря уникальной структуре молекулы Тиотриазолин имеет свойства как прямого, так и непрямого кардиопротектора, то есть действует непосредственно как метаболический препарат, нормализуя энергетические процессы в кардиомиоците, и опосредованно: обладает антиагрегантным и метаболическим эффектом, снижая тем самым нагрузку на миокард [19].
Несмотря на большой арсенал медикаментозных средств в лечении стенокардии, широкомасштабными исследованиями (TRIMPOL II, 2000; TRIKET, 2000) установлено, что 66 % больных со стенокардией оценивают качество своей жизни как неудовлетворительное, плохое, и лишь 17 % больных не ощущают ангинозных болей. В связи с этим определение и оценка качества жизни у больных с ИБС также стали предметом нашего исследования.
Цель и задачи исследования: основной целью данного исследования была оценка эффективности и переносимости препарата Тиотриазолин в таблетках производства фармацевтической корпорации «Артериум» по сравнению с препаратом триметазидин у пациентов с диагнозом «ИБС: стабильная стенокардия напряжения ІІ–ІІІ ФК». Клиническое исследование проводилось как открытое и выполнялось согласно требованиям, которые предъявляются Государственным фармакологическим центром МЗ Украины ко II фазе клинических испытаний.
Материалы и методика исследования
В исследование были включены 90 больных — 56 мужчин и 34 женщины в возрасте 40–70 лет (средний возраст — 63,1 ± 2,0 года) с диагнозом «ИБС: стабильная стенокардия напряжения ІІ–ІІІ ФК». Диагноз устанавливался на основании данных анамнеза, клинического и лабораторного обследований, соответствующих изменений на ЭКГ, ЭхоКГ, тредмил-теста. Обследуемые пациенты были разделены методом случайного распределения на 2 группы: в 1-й группе больным назначалась базисная терапия + Тиотриазолин 100 мг по 2 таблетки 3 раза в сутки в течение 30 дней, во 2-й группе пациентам дополнительно к базисной терапии назначался оригинальный триметазидин 20 мг 3 раза в сутки в течение 30 дней. Продолжительность лечения — 5 недель, продолжительность наблюдения — 6 недель. Все пациенты находились на стационарном лечении в кардиологическом отделении Железнодорожной больницы № 2 ст. Киев.
Всем пациентам проводилось общеклиническое обследование, определялись биохимические показатели: активность трансаминаз и МВ-фракции КФК, уровни билирубина, липидов, креатинина, общего холестерина, триглицеридов, глюкозы крови, калия, натрия и С-реактивного белка. Учитывались особенности течения основного заболевания, включая оценку болевого синдрома и частоту возникновения нарушений сердечного ритма.
Оценивались основные показатели ЭКГ и суточного мониторирования ЭКГ, а именно продолжительность интервалов PQ, QRS и QT, при отсутствии противопоказаний проводился тредмил-тест.
Статистическая обработка результатов проводилась с использованием пакета программ Excel (данные приведены в виде М ± m). Достоверность расхождений показателей оценивали с помощью парного t-критерия Стьюдента.
Критерии эффективности оценивались на основании уменьшения числа эпизодов болевой и безболевой ишемии миокарда по данным суточного мониторирования ЭКГ, увеличения толерантности к физической нагрузке по данным тредмил-теста, нормализации лабораторных показателей.
Показатели эффективности метаболической терапии:
Результаты исследований и их обсуждение
Клиническое исследование показало, что Тиотриазолин улучшал функцию левого желудочка, что является важной детерминантой повышения качества жизни и улучшения ближайшего и отдаленного прогноза больных со стабильной стенокардией напряжения ІІ–ІІІ ФК. Тем не менее это проявлялось тенденцией к уменьшению как систолического, так и диастолического размера левого желудочка, увеличением фракции выброса.
Во время клинических исследований доказана безопасность использования пероральной формы Тиотриазолина. Использование его целесообразно у пациентов со стабильной стенокардией напряжения ІІ–ІІІ ФК на фоне современной базисной терапии, которая включает использование нитратов, β-адреноблокаторов, антагонистов кальция, дезагрегантов, ингибиторов АПФ, диуретиков.
Эффективность препаратов оценивали по результатам суточного мониторирования ЭКГ и двойного тредмил-теста перед лечением и после 30 суток лечения.
Анализ полученных результатов показал, что в обеих группах наблюдалась положительная динамика течения ИБС. Так, в обеих группах было отмечено более быстрое регрессирование болевого синдрома, к 5-му дню пребывания в стационаре болевой синдром наблюдался только у 4 пациентов 1-й и 2-й групп. К 10-му дню ни у одного пациента, который получал терапию, болевой синдром не был отмечен.
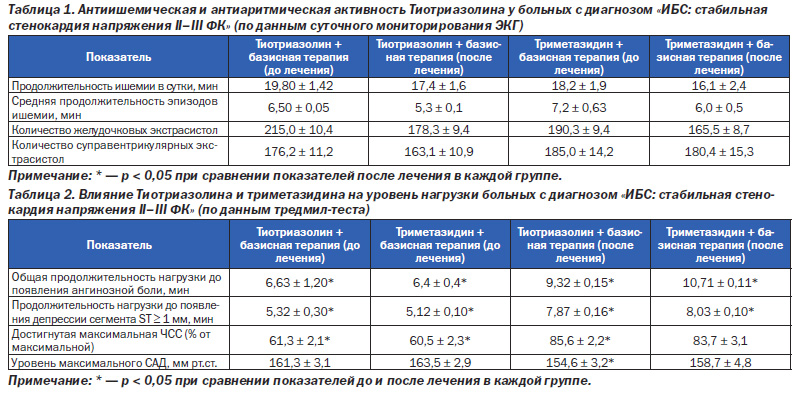
В обеих группах после проведенной терапии Тиотриазолином и триметазидином соответственно была зарегистрирована достоверно меньшая частота желудочковых экстрасистол как проявление уменьшения электрической нестабильности миокарда.
В группе Тиотриазолина было отмечено уменьшение частоты желудочковых и суправентрикулярных экстрасистол, что свидетельствует о значительном улучшении электрофизиологических характеристик миокарда.
По данным тредмил-тестов в начале лечения и после 30 суток было выявлено значительное достоверное увеличение продолжительности физической нагрузки до появления ангинозной боли (с 6,63 ± 1,20 мин до 9,32 ± 0,15 мин в 1-й группе и с 6,4 ± 0,4 мин до 10,71 ± 0,11 мин во 2-й). К тому же достоверно увеличилось время физической нагрузки до появления стойкой депрессии сегмента ST в обеих группах, что свидетельствовало об улучшении как электрофизиологических свойств миокарда, так и его антиишемической стойкости. При сравнении эффективности терапии Тиотриазолином и триметазидином не была выявлена достоверная разница между двумя группами. Оба препарата одинаково положительно влияли на течение ИБС: стабильной стенокардии напряжения ІІ–ІІІ ФК.
Анализ динамики лабораторных данных не выявил отрицательного влияния препаратов в обеих исследуемых группах на показатели общего анализа крови и мочи. Достоверно не изменялись уровни трансаминаз и показатели липидного спектра крови, что свидетельствует об отсутствии отрицательного влияния на состояние печени и почек.
Отсутствие нежелательной динамики лабораторных показателей свидетельствует о безопасности курсового лечения сравниваемыми препаратами.
Сравнительная характеристика переносимости и побочных явлений при приеме Тиотриазолина и триметазидина
Сравнительная оценка переносимости препаратов проведена на основании анализа данных объективного обследования и субъективных ощущений, которые сообщались пациентами, результатов проведенного ЭКГ и суточного мониторирования ЭКГ. Ни у одного пациента на фоне приема препаратов не возникло аллергических реакций, тошноты, бронхообструктивного синдрома и других побочных явлений, которые бы потребовали отмены препарата. По данным тредмил-тестов в начале лечения и на 30-е сутки лечения было выявлено достоверное увеличение продолжительности физической нагрузки до появления ангинозной боли. К тому же достоверно увеличилось время физической нагрузки в обеих исследуемых группах, что свидетельствует об улучшении как электрофизиологических свойств миокарда, так и его антиишемической стойкости. Переносимость обоих препаратов оценена как хорошая.
Выводы
1. Применение Тиотриазолина улучшает клинические параметры и качество жизни больных с диагнозом «ИБС: стабильная стенокардия напряжения ІІ–ІІІ ФК».
2. У 68 % больных группы Тиотриазолина по сравнению с группой, в которой препарат не применяли, клинически наблюдаются: уменьшение частоты и выраженности ангинозных приступов, средней продолжительности ишемии и продолжительности ишемии за сутки, уменьшение частоты аритмий по данным холтеровского мониторирования ЭКГ, увеличение толерантности к физическим нагрузкам по данным тредмил-теста (табл. 1, 2).
3. Тиотриазолин обладает аддитивным эффектом, потенцируя влияние нитратов, β-адреноблокаторов, антагонистов кальция, дезагрегантов, ингибиторов АПФ, диуретиков при лечении больных со стенокардией напряжения.
4. Тиотриазолин хорошо переносится и является эффективным и безопасным препаратом в терапии больных с диагнозом «ИБС: стабильная стенокардия напряжения ІІ–ІІІ ФК».
5. В обеих группах достоверное увеличение продолжительности физической нагрузки до появления ангинозной боли и времени физической нагрузки до появления стойкой депрессии сегмента ST подтверждает выявленную антиишемическую стойкость миокарда.
6. В группе Тиотриазолина было отмечено уменьшение частоты желудочковых и суправентрикулярных экстрасистол, что свидетельствует о значительном улучшении электрофизиологических характеристик миокарда.
1. Амосова Е.Н. Метаболическая терапия повреждений миокарда, обусловленных ишемией. Новый подход к лечению ишемической болезни сердца и сердечной недостаточности // Укр. кардиол. журнал. — 2000. — № 4. — С. 86-92.
2. Бобров В.О., Кулішов С.К. Адаптаційні ішемічні і реперфузійні синдроми у хворих ішемічною хворобою серця: механізми, діагностика, обгрунтування терапії. — Полтава: Дивосвіт, 2004. — 240 с.
3. Гагаріна А.А. Кардіопротектори метаболічного ряду тіотриазолін, цитохром, мілдронат в комплексній терапії аритмій серця при некоронарогенних захворюваннях міокарда: Автореф. дис... канд. мед. наук. — Сімферополь, 2001. — 20 с.
4. Дейнега В.Г., Мамедов А.М., Шапран Н.Ф., Кондратенко Л.В., Дейнега И.В. Применение тиотриазолина и прерывистой нормобарической гипоксии при лечении больных ИБС с артериальной гипертензией // Актуальні питання фармацевтичної та медичної науки i практики: Зб. наук. ст. — Запоріжжя, 2002. — Вип. 8. — С. 64-70.
5. Діагностика та лікування хронічної серцевої недостатності. Головні положення рекомендацій Європейського кардіологічного товариства. — 2006. Частина ІІ // Серце і судини. — 2006. — № 2. — С. 24-33.
6. Кошля О.В. Особливості системної гемодинаміки та перекисного окислення ліпідів у хворих серцевою недостатністю в процесі їх лікування ділтіаземом, нітретом та тіотриазоліном: Автореф. дис... канд. мед. наук. — Запоріжжя, 2000. — 21 с.
7. Мазур И.А., Волошин Н.А., Чекман И.С., Зименковский Б.С., Стец В.Р. Tиотриазолин: фармакологические аспекты и клиническое применение. — Запорожье, 2005. — 160 с.
8. Малая Л.Т., Корж А.Н., Балковая Л.Б. Эндотелиальная дисфункция при патологии сердечно-сосудистой системы. — Харьков: Торсинг, 2000. — 432 с.
9. Пархоменко А.Н. Жизнеспособный миокард и кардиоцитопротекция: возможности метаболической терапии при острой и хронической формах ишемической болезни сердца // Укр. мед. часопис. — 2001. — № 3(23). — С. 5-11.
10. Поливода С.Н., Черепок А.А., Сычев Р.А. Коррекция эндотелиальной дисфункции у больных гипертонической болезнью: эффективность и патофизиологическое обоснование применения тиотриазолина // Медицина світу. — 2004. — С. 18-20.
11. Сиволап В.Д. Оптимізація терапії післяінфарктної стенокардії тіотриазоліном // Журнал практичного лікаря. — 2003. — № 5. — С. 57-59.
12. Стан здоров''я народу України у зв''язку із хворобами системи кровообігу та можливі шляхи його покращання. Аналітично-статистичний посібник для лікарів кардіологів, ревматологів, терапевтів, загальної практики / Під ред. В.М. Коваленка. — К., 2004. — 124 с.
13. Шилов А.М. Некоторые особенности патогенеза ишемической болезни сердца // РМЖ. — 2007. — Т. 15, № 9.
14. Чекман И.С., Горчакова Н.А., Загородний М.І. та ін. Кардіопротектори метаболічної дії: доцільність експериментального і клінічного вивчення // Запорожский мед. журн. — 2003. — № 2. — С. 251-252.
15. Яковлева О.А., Савченко Н.П., Стопинчук А.В., Семененко И.Ф. Влияние тиотриазолина на состояние эндотелиальной дисфункции и липидно-перекисный дисбаланс при моно- и комбинированной терапии с метопрололом у больных ИБС // Актуальні питання фармацевтичної та медичної науки і практики: Зб. наук. статей. — Запоріжжя, 2002. — Вип. 8. — С. 245-249.
16. Di Napoli P., Taccardi A.A., Barsotti A. Long term cardioprotective action of trimetazidine and potential effect on the inflammatory process in patients with ischaemic dilated cardiomyopathy // Heart. — 2005. — 91. — 161-5.
17. Kantor P.F., Lucien A., Kozak R. et al. The antianginal drug trimetazidine shifts cardiac energy metabolism from fatty acid oxidation to glucose oxidation by inhibiting mitochondrial long-chain 3-ketoacyl coenzyme A thiolase // Circ. Res. — 2000. — Vol. 86. — P. 580-586.
18. Lee L., Horowitz J., Frenneaux M. Metabolic manipulation in ischaemic heart disease, a novel approach to treatment // Eur. Heart. J. — 2004. — 25. — 634-41.
19. Визир В.А., Волошина И.Н., Волошин Н.А., Мазур И.А., Беленичев И.Ф. Метаболические кардиопротекторы: фармакологические свойства и применение в клинической практике: Метод. рекомендации. — ЗГМУ, 2006. —13 с.