Газета «Новости медицины и фармации» Гастроэнтерология (323) 2010 (тематический номер)
Вернуться к номеру
Зовнішньосекреторна недостатність підшлункової залози як предиктор розвитку остеодефіцитних станів: нові можливості у лікуванні
Авторы: І.Г. Палій, д.м.н., С.П. Колісник, к.м.н. Вінницький національний медичний університет ім. М.І. Пирогова
Версия для печати
Захворювання органів травлення та опорно-рухового апарату є вельми актуальними проблемами сучасної медицини. Патологія органів травлення є однією з найпоширеніших у структурі захворюваності та займає третє місце після серцево-судинної та онкологічної. Залишається велика кількість невирішених питань діагностики, класифікації гастроентерологічних захворювань, лікування та реабілітації хворих, особливо при наявності в них супутньої патології, що ускладнює впровадження у практику вищеназваних заходів.
Зв''язок між патологією опорно-рухового апарату та органами травлення хоча і є загальновідомим, проте не завжди очевидним. Реалізація патологічного впливу (наприклад, патології хребта) на функціональний стан органів черевної порожнини може проявлятись у вигляді порушень моторики, секреції, хронізації запальних процесів за рахунок дистопії органів, порушення сегментарної вегетативної іннервації, патологічних змін мікроциркуляції тощо [6].
Вплив патології органів травлення на процеси ремоделювання кісткової тканини також широко відомий та висвітлений у медичній літературі. Проблема остеодефіцитних станів при патології органів травлення зумовлена розвитком патологічних змін процесів травлення, що проявляється синдромами мальдигестії та мальабсорбції з порушенням засвоєння мінеральних і органічних речовин [1, 3, 5].
Остеопенія та остеопороз настільки поширені, що за останні десятиріччя набули, на думку багатьох авторів, статусу «німої» епідемії [2, 4, 6]. Остеопороз та остеопенія високого ступеня зустрічаються в 30–40 % жінок та 10–15 % чоловіків віком понад 60 років. Розвиток даних патологічних станів значно прискорюється при наявності супутніх хронічних захворювань інших органів та систем, до яких відноситься патологія органів травлення [1, 2, 5].
Зниження функціональної здатності органів шлунково-кишкового тракту та їх ферментативної активності спричинює погіршення засвоєння кальцію та інших мінеральних речовин, мікроелементів та вітамінів, білків та інших структурних елементів кісткового матриксу з продуктів харчування навіть при достатньому їх надходженні, що, у свою чергу, є предиктором розвитку остеопенічних станів та остеопорозу [5].
Отже, своєчасне виявлення та адекватна корекція ензимопатій та зовнішньосекреторних дисфункцій при гастроентерологічній патології є надзвичайно важливим компонентом адекватного лікування пацієнтів із розладами шлунково-кишкового тракту та супутніми патологічними станами, зокрема остеопенією та остеопорозом.
Загальновідомо, що іони кальцію регулюють не лише тонус гладкої мускулатури шлунково-кишкового тракту, але й впливають на регуляцію секреції амілази ацинарними клітинами підшлункової залози (ПЗ), а також на продукцію секретину, панкреозиміну і протеолітичних ферментів [7].
Формування замкненого патологічного кола відбувається за рахунок взаємного обтяження гастроентерологічної патології та остеопенічних станів, що призводить до прогресування як остеопорозу, так і гастроентерологічної патології.
Для неінвазивної діагностики остеопорозу широко застосовують денситометрію. Золотим стандартом серед методів діагностики остеопорозу вважається двохенергетична рентгенівська денситометрія (DEXA). Недоліками методу є відносно велика вартість і малодоступність. Тому альтернативним скринінговим методом визначення мінеральної щільності кісткової тканини (МЩКТ) вважається ультразвукова кісткова денситометрія. Даний метод застосовується для ранньої діагностики остеопенічних станів і виявлення груп ризику. Відсутність променевого навантаження дозволяє використовувати їх для діагностики порушень кісткового метаболізму в дітей та вагітних. Висока відтворюваність результатів і можливість проведення багаторазових досліджень при відсутності променевого навантаження дозволяють вірогідно виявляти напрямок і величину змін щільності кісткової тканини на тлі терапії [4].
На базі кафедри внутрішньої та сімейної медицини та гастроентерологічної лабораторії Вінницького національного медичного університету ім. М.І. Пирогова, а також Центру медичної реабілітації та спортивної медицини нами було проведено комплексне клініко-лабораторно-інструментальне обстеження 82 гастроентерологічних хворих (54 жінки, 28 чоловіків) віком від 19 до 78 років (середній вік становив 50,44 ± 13,9 року).
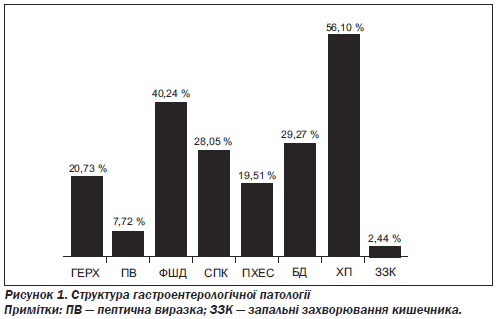
Найбільш поширеними нозологіями у структурі гастроентерологічної патології (рис. 1) були: гастроезофагеальна рефлюксна хвороба (ГЕРХ) — 20,73 %, синдром подразненого кишечника (СПК) — 28,05 %, біліарна дисфункція (БД) — 29,27 %, функціональна шлункова диспепсія (ФШД) — 40,24 %, що супроводжувались у більшості випадків наявністю ознак хронічного панкреатиту (ХП) — 56,10 % пацієнтів. Були також хворі на ерозивно-виразкові захворювання гастродуоденальної (7,32 %) зони та кишечника (2,44 %), а також пацієнти з постхолецистектомічним синдромом (ПХЕС). У більшості випадків було констатовано наявність кількох гастроентерологічних нозологій в одного пацієнта.
Діагностика амілазної недостатності (АН) підшлункової залози проводилась за допомогою 13С-амілазного дихального тесту на радіоізотопному інфрачервоному аналізаторі IRIS, WAGNER, Німеччина, згідно з методикою, рекомендованою для визначення амілазної недостатності [8]. Сумарна оцінка отриманих результатів проводилася за такою методикою: якщо в сумі результат становив 10 ‰ і більше, то це свідчило про відсутність амілазної недостатності. Якщо сумарний результат був < 10 ‰ — у хворого наявна амілазна недостатність [8].
Мінеральну щільність кісткової тканини визначали за допомогою ультра-звукової денситометрії. Визначалися такі показники: BQI (bone quality index) — індекс якості кістки, є одним з основних показників, характеризує мінеральну щільність кісткової тканини, Z-score — значення стандартного відхилення відносно середнього значення для даного віку пацієнта, статі та етнічної приналежності, T-score — значення стандартного відхилення відносно середнього значення у здорових пацієнтів 30-річного віку тієї ж статі та етнічної приналежності, що й пацієнт, який обстежується.
Зниження мінеральної щільності кісткової тканини за даними ультразвукової денситометрії спостерігалося у всіх пацієнтів із гастроентерологічною патологією за показниками T-score та Z-score (рис. 2), а також BQI (рис. 3).
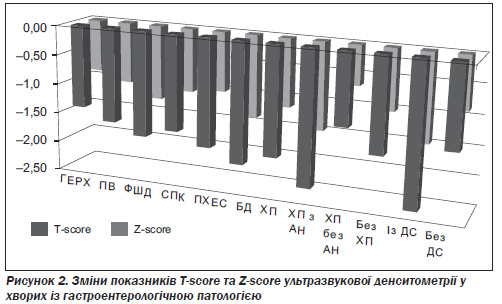
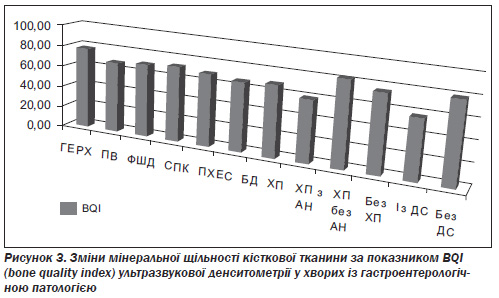

Найбільш вірогідними були зміни вищезгаданих показників у хворих із гастроентерологічною патологією, що супроводжувалася діарейним синдромом (ДС) (p < 0,01), порівняно з гастроентерологічними хворими без діареї, незалежно від нозологічної форми, проте найбільш вираженими були зміни у хворих на хронічний панкреатит. Серед хворих із зовнішньосекреторною амілазною недостатністю остеопороз та остео-
пенія третього ступеня (T-score < 2,0) зустрічалися вірогідно частіше, ніж у пацієнтів із нормальним рівнем амілолітичної функції (приріст концентрації вуглекислого газу, міченого ізотопом 13С, понад 10 %).
Найбільше зниження показників ультразвукової денситометрії спостерігалось у гастроентерологічних хворих із панкреатитом та амілазною недостатністю, незалежно від того, чи був у них синдром діареї.
Отже, основними предикторами зниження мінеральної щільності кісткової тканини слід вважати, крім факту наявності гастроентерологічної патології, наступні чинники: хронічний панкреатит, наявність амілазної недостатності та синдрому діареї.
Застосування замісної ферментної терапії повинно проводитись у схемах лікування остеопорозу при патології шлунково-кишкового тракту з ознаками амілазної недостатності, незалежно від нозологічної форми. Це, очевидно, пов''язане з особливостями всмоктування кальцію з продуктів харчування при недостатній амілолітичній функції підшлункової залози.
Сьогодні в розпорядженні лікаря є значна кількість ферментних препаратів, що відрізняються за кількістю компонентів, що входять до їх складу, ензимною активністю, способом виробництва та формами випуску.
Основними групами поліферментних препаратів, що широко використовуються сьогодні, є:
Вибір препарату для лікування зовнішньосекреторної панкреатичної недостатності повинен базуватися на таких критеріях:
На українському фармацевтичному ринку панкреатичні ферменти присутні у двох найбільш часто застосовуваних формах випуску — таблетки й капсули, вплив яких на ефективність лікування як больового абдомінального синдрому, так і зовнішньосекреторної недостатності підшлункової залози з урахуванням еквівалентних доз панкреатину є порівнянним. Інтерес для клініциста може становити ферментний препарат Панзинорм форте 20 000, а також Панзинорм 10 000, що відносно недавно з''явився на ринку у формі капсул, заповнених мікропелетами.
Висока клінічна ефективність капсульованих ферментних препаратів, що вкриті кишковорозчинною оболонкою й містять мікропелети (мікротаблетки, мікросфери), в корекції порушень екзокринної функції ПЗ доведена численними клінічними дослідженнями, що відповідають принципам доказової медицини. Дана форма ферментного препарату має оптимальний пасаж по травному тракту. Капсула швидко розчиняється в шлунку, вивільняючи мікрочастинки (мікрогранули, мікропелети), які, перемішуючись із хімусом, потрапляють у дванадцятипалу кишку й активізуються в її дистальних відділах, корегуючи таким чином недостатність зовнішньосекреторної функції ПЗ.
У цьому сенсі хотілося б відзначити, що капсульований ферментний препарат Панзинорм 10 000, який має у своєму складі 10 000 ОД Ph. Eur. ліпази, 7200 ОД Ph. Eur. амілази, 400 ОД Ph. Eur. протеаз та містить мікропелети, може зайняти гідні позиції в терапії екзокринної недостатності ПЗ.
Відсутність у препараті Панзинорм 10 000 компонентів жовчі, гідрохлоридів амінокислот, яловичого білка робить можливим призначення даного препарату в першу чергу в пацієнтів із загостренням хронічного панкреатиту та тяжкою патологією печінки (гепатити, цирози), з вираженим дуоденітом, що супроводжується шлунковою гіперсекрецією, тобто в тих випадках, коли присутність жовчних кислот украй небажана.
Крім того, відсутність компонентів жовчі й оптимальне співвідношення панкреатичних ферментів робить можливим призначення препарату Панзинорм 10 000 для тривалої ферментної замісної терапії у хворих із хронічною патологією підшлункової залози з різними ступенями зовнішньосекреторної недостатності, у тому числі тяжкого ступеня, із вираженою стеатореєю.
У цілому Панзинорм 10 000 відповідає основним вимогам, що висуваються до ферментних засобів, призначених для лікування хворих із патологією підшлункової залози, особливо з хронічним панкреатитом:
Серед достоїнств Панзинорму 10 000 слід відзначити відсутність побічних ефектів і добру переносимість, завдяки чому його можна застосовувати в усіх вікових групах без ризику виникнення яких-небудь негативних наслідків.
Лікування зовнішньосекреторної панкреатичної недостатності за допомогою препарату Панзинорм 10 000 спрямоване на ліквідацію порушень перетравлювання жирів, білків і вуглеводів із метою профілактики розвитку мальдигестії, а згодом і синдрому мальабсорбції в пацієнтів із тяжкою хронічною патологією підшлункової залози.
Режими дозування і тривалість застосування ферментного препарату Панзинорм 10 000 залежать від ступеня вираженості екзокринної недостатності ПЗ:
Тривалість призначення препарату Панзинорм 10 000 становить від 1 міс.; за необхідності препарат можна приймати постійно.
Висновки
1. При гастроентерологічній патології слід очікувати зниження мінеральної щільності кісткової тканини.
2. Наявність у хворого на хронічний панкреатит ознак зовнішньосекреторної амілазної недостатності є предиктором розвитку остеопенії високого ступеня та остеопорозу.
3. При гастроентерологічній патології слід проводити своєчасне визначення мінеральної щільності кісткової тканини з метою ранньої діагностики вторинного остеопорозу.
4. У хворих на остеопороз та остеопенію другого та третього ступенів потрібно проводити визначення амілазної недостатності підшлункової залози для диференційованого призначення замісної ферментативної терапії.
5. Капсульований ферментний препарат Панзинорм 10 000, що має у своєму складі 10 000 ОД Ph. Eur. ліпази, 7200 ОД Ph. Eur. амілази, 400 ОД Ph. Eur. протеаз та містить мікропелети, може бути препаратом вибору в лікуванні екзокринної недостатності ПЗ.
1. Пасиешвили Л.М., Моргулис М.В. Роль кальция в системе гомеостаза и функционировании поджелудочной железы // Сучас. гастроентерологія. — 2004. — № 5. — С. 97-100.
2. Поворознюк В.В. Кальций и остеопороз: современный взгляд на проблему // Здоров''я України. — 2002. — № 3. — С. 37.
3. Пасиешвили Л.М., Бобро Л.Н. Роль заболеваний пищеварительного канала в формировании и прогрессировании вторичного остеопороза // Сучас. гастроентерологія. — 2008. — № 4. — С. 12-18.
4. Stewart A., Reid D.M. Quantitative ultrasond in osteoporosis // Semin. Musculoscelet. Radiol. — 2002. — Vol. 6, № 3. — P. 229-232.
5. Христич Т.Н., Пишак В.П., Кендзерская Т.Б. Хронический панкреатит: нерешенные проблемы. — Черновцы: Медуниверситет, 2006. — 280 с.
6. Колісник П.Ф. Патологія хребта як ланка патогенезу захворювань внутрішніх органів та фактор їх резистентності до лікування: Дис… д-ра мед. наук. — Вінниця, 2002. — 308 с.
7. Glasbrenner B., Kahl S., Malfertheiner P. Modern diagnostics of chronic pancreatitis // Eur. J. Gastroenterol. Hepatol. — 2002. — 14(9). — P. 935-41.
8. Wetzel K., Fischer H. 13C-Breath Tests in Medical Research and Clinical Diagnosis // Fischer ANalysen Instrumente GmbH (FAN). — Leipzig, 2001. — Р. 51.
