Газета «Новости медицины и фармации» Гастроэнтерология (323) 2010 (тематический номер)
Вернуться к номеру
Дифференцированные методы ранней санаторно-курортной реабилитации больных после холецистэктомии
Авторы: Н.В. Драгомирецкая, д.м.н., профессор; И.Б. Заболотная, к.м.н.
Украинский НИИ медицинской реабилитации и курортологии, г. Одесса
Версия для печати
Калькулезный холецистит — одно из наиболее распространенных заболеваний органов пищеварения. По данным разных авторов [2, 3, 5, 12], он составляет 36,1–38,7 % в структуре патологии желудочно-кишечного тракта, имеет тенденцию к постоянному росту. В по-следние 40–50 лет заболеваемость холелитиазом за каждые 10 лет удваивалась. В Украине, согласно данным [3], с 1992 по 1999 год частота желчнокаменной болезни (ЖКБ) увеличилась в 2,1 раза. А по материалам патологоанатомических исследований, за последние 25 лет заболеваемость ЖКБ выросла приблизительно в 2,8 раза [3, 5].
Параллельно росту заболеваемости увеличивается и количество операций по поводу ЖКБ. Для большинства больных сегодня золотым стандартом является эндовидеохирургическая (лапароскопическая) холецистэктомия (ХЭ), которая имеет определенные показания и преимущества над традиционной ХЭ. Однако, невзирая на успехи хирургии, оперативные вмешательства не всегда избавляют от страданий. Последствия холецистэктомии в виде многочисленных патологических функциональных и органических синдромов выявляют у 30–40 % оперированных больных [2, 5, 12], поскольку при ЖКБ в патологический процесс закономерно втягиваются печень, поджелудочная железа, желудок, двенадцатиперстная кишка (ДПК) и кишечник. Это приводит к формированию хронической патологии, которая имеет сложный патогенез и разнообразные проявления. Этим и определяется клиническая значимость проблемы постхолецистэктомического синдрома, исследованию которого в последние годы уделяется неоправданно мало внимания [12].
Поэтому целью работы было повышение эффективности лечения больных в ранние сроки после холецистэктомии на основе дифференцированного применения минеральной воды (МВ) и различных методов физиотерапии с учетом патологических изменений в гепатопанкреатобилиарной и гастродуоденальной системах (ГДС), а также метаболических расстройств.
Природные и преформированные физические факторы были выбраны нами не случайно, поскольку кроме влияния на причину и патогенез заболевания, отдельные симптомы они обладают саногенетической и превентивной направленностью действия.
Материалы и методы исследования
Под нашим наблюдением находилось 87 больных, перенесших холецистэктомию по поводу ЖКБ и поступивших на раннюю курортную реабилитацию в Одесский гастроэнтерологический санаторий им. М. Горького непосредственно после выписки из хирургического стационара. Больные, перенесшие лапароскопическую ХЭ, поступали в среднем на 5–6-й день, а пациенты, прооперированные традиционным путем, — на 10–14-й день после оперативного вмешательства.
Всем больным до и после лечения проводили общеклиническое исследование крови и мочи, биохимическое исследование крови, ультразвуковое исследование (УЗИ) органов брюшной полости, компьютерную внутрижелудочную рН-метрию, эзофагогастродуоденофиброскопию. Определение Н.руlоri осуществлялось с помощью мазков отпечатков биоптатов ткани желудка с последующей окраской по Романовскому — Гимзе и с помощью дыхательного хелик-теста.
Кроме того, обязательно проводилось копрологическое исследование, которое позволяет оценить функциональное состояние органов пищеварения. В нашей работе были исследованы переваривающая способность секрета поджелудочной железы по признакам стеатореи и амилореи и функция желчеотделения по наличию жирных кислот в кале.
Исследование состояния углеводного обмена начинали с определения концентрации глюкозы в крови и моче натощак. В случаях когда гликемия натощак не имела отклонений от нормы и глюкозурия не определялась, для выявления скрытых нарушений углеводного обмена применяли тест толерантности к глюкозе (ТТГ).
Больному натощак давали выпить
Алгоритм оценки результатов теста толерантности к глюкозе формализован следующим образом:
δ = 3,6(у1 – 4,44) + 6,1(у2 – 6,66) + 8,3(у3 – 4,44),
где δ — обобщенный критерий (показатель) отклонений гликемической кривой от нормы; у1, у2, у3 — уровень гликемии натощак и соответственно за 1 и 2 часа после нагрузки глюкозой, наблюдающийся у конкретного пациента (собственные показатели).
Для дифференциальной диагностики результатов ТТГ границы отличительных состояний системы регуляции глюкозы крови относительно обобщенного критерия представлены так: норма — 0–15; группа повышенного риска — 16–25; нарушенная толерантность к глюкозе — 26–40; диабетический тип гликемической кривой — более 40.
Все больные методом рандомизации были разделены на 3 группы. Первая группа (28 человек) являлась контрольной и получала базисный комплекс лечения, включавший: дифференцированный двигательный режим, лечебное питание (диета № 5 дробная), прием внутрь маломинерализованной сульфатно-гидрокарбонатно-хлоридной натриевой минеральной воды Одесская № 1 по 200 мл 3 раза в день за 40–60 минут до еды в зависимости от уровня кислотообразования.
Больным второй группы (31 человек) дополнительно назначали курс амплипульс-терапии (терапия синусоидальными модулированными токами — СМТ-терапия) на эпигастральную область (ІІ комплекс лечения). Действие СМТ проводили от аппарата «Амплипульс – 4» в переменном режиме; применяли ІІ и IV роды работ по 3–5 минут каждый, частота модуляции 100–50 Гц, глубина модуляции 50–75 %. Сила тока — 5–12 мА. Электроды размером 150 см2 располагали на эпигастральной области и на область нижнегрудного отдела позвоночника. Процедуры общей длительностью 6–10 минут проводили через день, 10–12 процедур на курс.
В ІІІ комплекс восстановительного лечения (28 пациентов) включали ДМВ-терапию (дециметровые волны) на участок правого подреберья. Процедуры проводились от аппарата «Ранет». Продольный излучатель располагали на участке правого подреберья с зазором 3–4 см, мощность — 25 Вт, экспозиция 15 минут, через день, на курс 10–12 процедур.
Длительность лечения составляла 24 дня.
Группы больных были сопоставимы по полу и возрасту, частоте выявленных патологических изменений.
Статистическая обработка результатов проводилась на персональном компьютере с использованием программ Exсel.
Результаты и их обсуждение
Среди обследованных больных были преимущественно женщины — 83,91 %, мужчин всего 16,09 %.
В плановом порядке было прооперировано 64 человека (73,56 %), ургентную холецистэктомию перенесли 23 пациента (26,44 %).
Из общего числа лиц, вошедших в исследование, лапароскопическим путем удаление желчного пузыря было сделано 36 больным, с помощью лапаротомного доступа оперативное вмешательство перенес 51 пациент.
При поступлении в санаторий у больных определялись астеновегетативний (81,61 ± 3,66 % случаев), болевой (79,31 ± 2,43 % случаев) и диспептический (51,72 ± 4,66 % пациентов) синдромы различной степени выраженности.
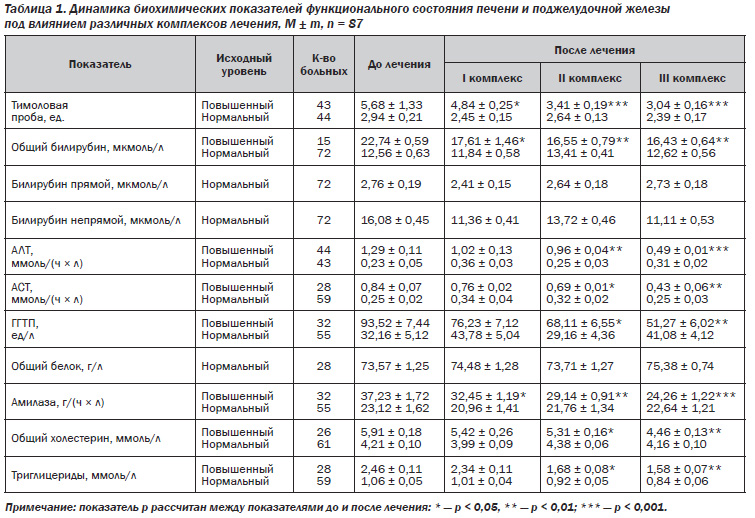
У части пациентов были выявлены нарушения функционального состояния печени, обусловленные непосред-ственно течением ЖКБ и оперативным вмешательством. Так, показатель тимолового помутнения был повышенным у 49,42 ± 3,68 % больных и составлял в среднем 5,68 ± 1,33 ед. SH, незначительные гипербилирубинемия и гипертрансфераземия наблюдались соответственно в 17,24 ± 3,44 % и 18,39 ± 3,58 % случаев.
В то же время у трети пациентов выявлены нарушения функционального состояния печени, обусловленные скорее наличием стеатоза печени или стеатогепатита, нежели течением ЖКБ и оперативным вмешательством. Это подтверждалось 2–2,5-кратным увеличением аланиновой трансаминазы (АЛТ), повышением гамма-глутамилтранспептидазы (ГГТП) в среднем до 1,5 нормы и сочеталось с достоверным (р < 0,05) увеличением абсолютных концентраций общего холестерина и триглицеридов. Следует сказать, что такие показатели наблюдались у этих пациентов и до операции (результат обследования на маркеры вирусных гепатитов отрицательный). Также все эти больные были прооперированы в так называемый холодный период, в основном лапароскопическим путем.
Описанные биохимические признаки неалкогольной жировой болезни печени подтверждались проведением УЗИ, где наблюдалась повышенная эхогенность паренхимы печени, размытый сосудистый рисунок, нечеткая визуализация диафрагмального контура органа.
Явления хронического панкреатита характеризовались гиперамилаземией у части пациентов (36,78 ± 4,54 %), УЗ-признаками (89,65 ± 2,89 % больных) и дефицитом липолитической и амилолитической активности секрета поджелудочной железы при проведении копроскопии почти у всех вошедших в исследование лиц.
На основании эндоскопических данных в 100 % случаев наблюдалось вовлечение в патологический процесс гастродуоденальной системы разной степени выраженности что в 54,02 ± 4,68 % случаев было ассоциировано с хеликобактериозом различной степени, что, безусловно, осложняет течение послеоперационного периода. Чаще всего (56,32 ± 4,69 % случаев) встречались выраженные воспалительно-дистрофические изменения слизистой оболочки желудка и двенадцатиперстной кишки. Эрозии желудка и/или двенадцатиперстной кишки наблюдали у 20,69 ± 2,12 % пациентов.
Моторно-эвакуаторные расстройства характеризовались дуоденогастральным рефлюксом (ДГР) у 70,11 ± 4,19 % больных, а у 34,48 ± ,16 % пациентов — наличием гастроэзофагеального рефлюкса с сопутствующим эзофагитом. Следует отметить, что частота дуоденогастрального рефлюкса значительно увеличивается после удаления желчного пузыря. Это объясняется нарушением взаимосвязи между пищеварительным каналом и желчным пузырем и потерей концентрационной функции желчного пузыря, когда возникают условия, которые способствуют прогрессированию нарушений моторной деятельности ДПК [4, 6]. ДГР наряду с наличием H.рylori является одним из основных причин формирования воспалительных и эрозивно-язвенных поражений слизистой желудка у больных после холецистэктомии [4].
Нарушение базального кислотообразования регистрировалось в подавляющем количестве исследований и составляло 85,06 ± 3,36 % случаев. При этом гиперацидность наблюдалась у 21,84 ± 3,85 % больных, гипоацидность — в 63,22 ± 4,52 % наблюдений.
Согласно анализу результатов ТТГ по обобщенному критерию, у 67,81 ± ± 6,08% больных были выявлены нарушения углеводного обмена, причем в 48,27 ± 5,69 % случаев это были скрытые нарушения, а в 19,54 ± 5,07 % наблюдений впервые выявлен сахарный диабет 2-го типа. При этом у данных пациентов не наблюдалось гипергликемии при рутинном обследовании.
Нарушения в системе регуляции уровня глюкозы крови даже в латентной форме оказывают повреждающее действие на вегетативную нервную систему и микроциркуляторное русло, что усугубляет течение основного заболевания [6].
Перечисленные патологические явления протекают по принципу взаимосвязи и взаимоотягощения, осложняя течение послеоперационного периода и обусловливая трансформацию различных патологических изменений в органах гепатопанкреатобилиарной и гастродуоденальной систем в стойкие расстройства, тяжесть которых усиливается с течением времени, что поддер-живает и усложняет течение метаболических нарушений.
При обобщении всего вышеперечисленного становится понятной необходимость дифференцированного, патогенетически обоснованного подхода к раннему восстановительному лечению данной категории больных.
Проведенное лечение характеризовалось положительной динамикой течения заболевания во всех трех группах: практически у всех больных после курса восстановительного лечения улучшилось общее самочувствие, уменьшилась выраженность астенического, болевого и диспептического синдромов. У подавляющего большинства пациентов отмечена позитивная динамика функционального состояния гепатобилиарной системы, поджелудочной железы, гастродуоденальной системы, метаболических расстройств.
Между тем проведенный анализ эффективности каждого отдельного комплекса курортной терапии выявил существенные отличия, что впоследствии позволило дифференцировать их применение.
Так, положительная динамика астенического синдрома в виде общей слабости, быстрой утомляемости была наиболее выражена у больных II и III групп, где к концу курортной терапии у большинства пациентов эти явления были нивелированы (р < 0,001). В то же время у лиц группы контроля в основном наблюдалось лишь уменьшение описанных жалоб (р < 0,05).
Разным было влияние примененных комплексов на болевой синдром.
Так, наиболее выраженным действием относительно клинических признаков болевого синдрома со стороны гепатобилиарной системы обладал комплекс с использованием ДМВ-терапии, хотя достоверных отличий между II и III группами больных выявлено не было. Назначение курса процедур ДМВ способствовало ликвидации боли в правом подреберье, болезненности при пальпации в этой области и в точке Кера, позитивного симптома Ортнера практически у всех осмотренных пациентов (р < 0,001).
Исчезновение проявлений болевого синдрома у больных, дополнительно получавших амплипульс-терапию, происходило медленнее. В основном это наблюдалось в случаях выраженного болевого синдрома в начале лечения, особенно у больных, перенесших деструктивные формы калькулезного холецистита, реже у больных, перенесших традиционную холецистэктомию. Бесспорно меньшим был лечебный эффект в контрольной группе, где чаще по сравнению с другими группами происходило лишь уменьшение субъективных и объективных проявлений болевого синдрома (р > 0,05).
Если оценивать влияние применяемых комплексов на проявления болевого синдрома со стороны ГДС, то в данном случае наиболее эффективным был лечебный эффект СМТ-терапии. Это выражалось в исчезновении жалоб на боли в эпигастральной области, в том числе ночных и голодных в 100 % случаев, существенном уменьшении объективных признаков поражения желудка и ДПК (болезненность при пальпации гастродуоденальной зоны, положительный симптом Мерфи). В то же время у больных I и III групп в большинстве наблюдений происходило только уменьшение интенсивности, частоты возникновения и продолжительности болевых ощущений (р > 0,05).
Назначение амплипульс-терапии обусловило и наиболее благоприятное влияние на синдром диспепсии (р < 0,003). Так, исчезновение тяжести в надчревной области, изжоги и горечи во рту наблюдалось у абсолютного количества больных, ранее их предъявлявших, чего не происходило в других группах. У больных, получавших процедуры ДМВ-терапии на область правого подреберья, в половине случаев сохранялись изжога и тяжесть в надчревной области (р < 0,05). Значительно медленнее нивелировались явления диспептического синдрома у пациентов, получавших только питьевое лечение: сохранение жалоб, хотя и менее выраженных, в конце курортной терапии регистрировалось почти у половины опрошенных лиц.
Благоприятным было влияние всех видов курортной терапии и на функцио-
нальное состояние печени. Но наименее эффективным оказался I лечебный комплекс, при применении которого нормализация исследуемых показателей наблюдалась лишь у части пациентов. Тогда как в отличие от него у больных II и III групп были достигнуты сравнимая достоверная динамика тимоловой пробы, показателей пигментного обмена, устранение незначительной гипертрансфераземии.
Между тем влияние на показатели стеатоза печени и стеатогепатита максимально выражено было в группе больных, получавших ДМВ-терапию, хотя у пациентов II группы также наблюдалось достоверное снижение средних значений изучаемых показателей.
Исследование липидного спектра плазмы крови после курсового воздействия волнами дециметрового диапазона продемонстрировало достоверное снижение средних концентраций общего холестерина и триглицеридов, хотя у отдельных больных (10,71 ± 5,95 % лиц) эти показатели продолжали превышать норму. Параллельно наблюдалась положительная достоверная динамика активности аланинаминотрансферазы, аспартатаминотрансферазы (АСТ) и ГГТП (табл. 1).
Полученный эффект подтверждался данными УЗИ: наблюдалось восстановление эхогенности органа, улучшение визуализации его диафрагмального контура, уменьшение сглаженности сосудистого рисунка, чего не было зарегистрировано в группах сравнения.
Применение данного комплекса лечения также значительно улучшало желчеобразование и желчеотделение. Так, в конце терапии только у 3,57 % пациентов в копрограмме были найдены жирные кислоты, в то же время у больных, которым назначались I или II комплексы, присутствие жирных кислот в кале наблюдалось в 25,81 ± 7,85 % и 23,07 ± 8,42 % случаев соответственно (р < 0,05).
Такой выраженный терапевтический эффект выбранного вида курортной терапии находит объяснение в патогенетически обоснованном подходе к лечению больных, перенесших холецистэктомию. ДМВ-терапия повышает уровень метаболических реакций, что связано с интенсификацией окислительно-восстановительных реакций, усилением тканевого дыхания, стимуляцией энергетических и трофических процессов. В свою очередь, активизация, метаболизма способствует стимуляции репаративной регенерации в печени, восстановлению ее функционального состояния. ДМВ оказывают выраженный противовоспалительный эффект, что обусловлено благоприятным влиянием на микроцикруляцию органа, а именно, усилением артериального притока и венозного оттока из печени и улучшением тонуса внутрипеченочных сосудов, бактериостатическим влиянием на ряд бактерий, спазмолитическим действием на сфинктерный аппарат. Кроме того, процедуры ДМВ стимулируют выделение основных составляющих желчи, особенно желчных кислот, что характеризует усиление функции гепатоцитов, при этом восстанавливается желчеобразование и желчеотделение, коллоидные свойства желчи [1, 7].
Изучение влияния предложенных комплексов на показатели внешнесекреторной функции поджелудочной железы продемонстрировало максимальную эффективность амплипульс-терапии, что характеризовалось достоверной нормализацией амилазы крови у всех пациентов, амилолитической и липолитической активности секрета поджелудочной железы, по результатам копроскопии. Так, сохранение капель нейтрального жира и зерен крахмала при проведении повторной копрограммы наблюдалось у 16,13 ± 6,60 % и 12,90 ± 6,02 % пациентов соответственно (р < 0,003), в то время как у больных I или III лечебных групп нам удалось достичь лишь тенденции к восстановлению экзокринной функции поджелудочной железы, что проявлялось в основном снижением содержания изуч-аемых патологических элементов кала в большинстве случаев. Полученные результаты применения II комплекса лечения подтверждались и данными УЗИ, что характеризовалось восстановлением эхогенности и структуры поджелудочной железы, нормализацией ее размеров, улучшением визуализации контуров и границ железы по сравнению с больными, получавшими I и III комплексы.
Важным представляется влияние выбранных видов курортной терапии на состояние гастродуоденальной системы.
Здесь также наилучший эффект достигался при использовании синусоидально-модулированных токов, что подтверждалось клинико-эндоскопическими данными. Согласно проведенным наблюдениям, амплипульс-терапия оказывала выраженный противовоспалительный эффект на слизистую оболочку ГДС, что проявлялось отсутствием гиперемии, отека слизистой, заживлением эрозий. В группах сравнения противовоспалительный эффект был существенно слабее, хотя очаговые (эрозивные) дефекты слизистой после лечения не были обнаружены в 5 из 9 наблюдений (у 2 больных III группы и у 3 пациентов I группы). Такие выраженные положительные изменения происходили параллельно с достоверным снижением кислотопродукции, особенно у больных с низкими значениями рН (р < 0,001).
Существенными позитивными сдвигами характеризовалось влияние II лечебного комплекса и на моторно-эвакуаторные расстройства, чего не наблюдалось у больных I и III групп, где в большинстве случаев не удалось восстановить пропульсивную моторику ГДС (рис. 1, 2).

Выраженная динамика патологического процесса в ГДС при использовании синусоидально-модулированных токов сопровождалась и снижением степени контаминации H.рylori в слизистой оболочке желудка у большинства обследованных больных (снижение степени обсеменения зарегистрировано у 9 из 17 лиц с исходным наличием H.рylori), чего не наблюдалось в группах сравнения. Полученные результаты совпадают с результатами других авторов [11], что дает возможность использовать предложенные виды воздействий как дополнительные факторы, способствующие эрадикации при проведении стандартных схем антихеликобактерной терапии.
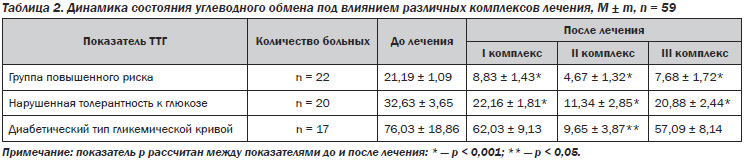
Неравнозначным было влияние различных видов восстановительной терапии на состояние углеводного обмена. Так, у больных I и III групп наблюдалось полное восстановление скрытых нарушений углеводного обмена только при условии принадлежности показателей ТТГ к группе повышенного риска. У пациентов с нарушенной толерантностью к глюкозе, несмотря на достоверное снижение среднего показателя ТТГ, полной нормализации системы регуляции уровня глюкозы крови не наблюдалось ни в одном случае. Кроме того, не зарегистрировано существенной динамики углеводного обмена у пациентов с впервые выявленным сахарным диабетом 2-го типа (табл. 2).
В то же время при использовании II комплекса лечения было достигнуто полное восстановление углеводного обмена не только у больных, которые принадлежали к группе повышенного риска, но и у пациентов с нарушенной толерантностью к глюкозе.
Таким образом, на этапе ранней курортной реабилитации у данных больных под влиянием лечения удалось предотвратить развитие сахарного диабета. Важно подчеркнуть: несмотря на то, что не было достигнуто нормального течения углеводной нагрузки у больных с диабетическим типом гликемической кривой, СМТ-терапия приводила к значительному улучшению состояния углеводного обмена, а именно: показатель ТТГ у 3 из 5 лиц достоверно снизился до пределов группы повышенного риска, а у остальных больных соответствовал нарушенной толерантности к глюкозе. В связи с этим среднее значение по группе в исходе лечения соответствовало показателям нарушенной толерантности к глюкозе. Такая существенная динамика уровня гликемической нагрузки в данной группе является прогностически благоприятным признаком и еще раз подтверждает мысль о целесообразности превентивного применения природных и преформированных физических факторов, когда еще не успела сформироваться стойкая хроническая патология и эффективность лечения существенно выше.
Такой положительный эффект СМТ-терапии на выявленные функциональные и метаболические расстройства при локальном воздействии на эпигастральную область можно объяснить способностью данного вида токов усиливать микроциркуляцию органов гастродуоденальной системы и поджелудочной железы, оказывать противовоспалительный и трофический эффекты, снижать интенсивность кислотообразования, нормализовывать пропульсивную моторику, устраняя явления дуодено-стаза [1, 7, 11].
Следует также отметить и способность лечебных минеральных вод положительно влиять на все виды обмена, в том числе и на углеводный, нивелируя явления инсулинорезистентности благодаря повышению количества и чувствительности инсулиновых рецепторов периферических тканей, увеличению резервов энтероинсулярной оси [9, 10].
Положительное влияние МВ на состояние гепатобилиарной системы объясняется их общеизвестной способностью восстанавливать желчеобразование и желчеотделение, качественный состав желчи [1, 7]. Кроме того, минеральная вода в теплом виде оказывает спазмолитическое действие на сфинктер Одди [1, 7], дисфункция которого рассматривается современной гастроэнтерологией как одна из основных причин прогрессирования хронической патологии гепатобилиарной системы у больных после ХЭ [2].
В то же время лечебных эффектов минеральной воды было недостаточно для получения достоверных сдвигов, что проявлялось лишь тенденцией к положительным изменениям изучаемых показателей в большинстве случаев у пациентов контрольной группы.
Таким образом, ранняя курортная реабилитация больных, перенесших холецистэктомию, с использованием дифференцированного, патогенетически обоснованного подхода к выбору комплексов лечения позволяет предотвратить прогрессирование патологического процесса в органах гепатопанкреатобилиарной и гастродуоденальной систем, а также существенно улучшить течение метаболических процессов.
Выводы
1. У больных в ранние сроки после холецистэктомии (5–14-й дни) в 56,32 ± ± 4,69 % случаев обнаруживаются выраженные воспалительные явления со стороны гастродуоденальной системы наряду с моторно-эвакуаторными расстройствами (70,11 ± 4,19 % больных), что в половине случаев ассоциировано с хеликобактериозом различной степени, а 85,06 ± 3,36 % наблюдений сопровождается нарушением кислотообразования.
2. Скрытые нарушения углеводного обмена у больных после холецистэктомии определяются в 48,27 ± 5,69 % случаев, а неалкогольный стеатогепатит диагностируется у трети пациентов.
3. ДМВ-терапия на область правого подреберья является наиболее эффективной при выраженном патологическом процессе в гепатобилиарной системе, характеризующимся нарушением функционального состояния печени, явлениями стеатоза, нарушением желчеобразования и желчеотделения.
4. СМТ-терапия на область эпигастрия способствует ликвидации воспалительного процесса в эзофагогастродуоденальной системе, восстановлению ее моторно-эвакуаторной функции. Данный метод лечения способствует нормализации углеводного обмена при условии его начальных, скрытых нарушений.
1. Выгоднер Е.Б. Физические факторы в гастроэнтерологии. — М.: Медицина, 1987. — 304 с.
2. Харченко Н.В., Бабак О.Я. Гастроентерологія. — К., 2007. — 720 с.
3. Голубчиков М.В. Статистичный огляд захворювання населення України на хвороби печінки та жовчовивідних шляхів // Сучасна гастроентерологія. — 2000. — № 2. — С. 56-59.
4. Губергриц Н.Б. Применение Маалокса в гастроэнтерологической практике // Сучасна гастроентерологія. — 2002. — № 4. — С. 55-59.
5. Дегтярева И.И. Клиническая гастроэнтерология: Руководство для врачей. — М.: Медицинское информационное агенство, 2004. — 640 с.
6. Камышева Е.П., Покалев Г.М. Сахарный диабет (современные представления, клинические симптомы, синдромы и врачебная тактика). — Нижний Новгород: Изд-во Ниже Новгородской государственной медицинской академии, 1999. — 142 с.
7. Кенц В.В., Шмакова І.П., Косовєров Є.О., Паненко А.В. Медична реабілітація та приватна фізіотерапія. — Одеса: Резон, 2001. — 170 с.
8. Оценка результатов глюкозотолерантного теста по обобщенному критерию: Метод. рекомендации / КНИИ эндокринологии и обмена веществ /Сост. Ю.Г. Антомонов, М.А. Базарнова, Д.Д. Дроздов, Л.С. Ларичев и др. —
К., 1984. — 14 с.
9. Полушина Н.Д. Влияние минеральной воды на продукцию серотонина и инсулина (экспериментальное исследование) // Вопросы курортологии, физиотерапии и ЛФК. — 1998. — № 4. — С. 9-10.
10. Полушина Н.Д., Ботвинева Л.А., Фролков В.К. Изменение чувствительности тканей к инсулину под воздействием питьевых минеральных вод (клинико-экспериментальные исследования) // Вопросы курортологии, физиотерапии и ЛФК. — 1998. — № 6. — С. 21-24.
11. Филимонов Р.М., Обехова Е.В. Физиотерапия в реабилитации больных хроническим гастродуоденитом // Вопросы курортологии, физиотерапии и лечебной физической культуры. — 1998. — № 4. — С. 48-51.
12. Циммерман Я.С. Клиническая гастроэнтерология: избранные разделы. — М.: ГЭОТАР-Медиа, 2009. — 416 с.