Журнал «Здоровье ребенка» 1 (22) 2010
Вернуться к номеру
Муколитическая терапия в педиатрической практике
Авторы: Сорока Ю.А., Донецкий национальный медицинский университет им. М. Горького; Прохорова И.Н., ЖК ЦРП, г. Киев
Рубрики: Педиатрия/Неонатология
Версия для печати
В статье обобщены современные данные о мукоцилиарном клиренсе, о формировании кашлевого рефлекса. Рассмотрены вопросы о принципах муколитической и противокашлевой терапии у детей при заболеваниях респираторного тракта. Даны рекомендации по применению отхаркивающих средств растительного происхождения (Эвкабал).
Дети, мукоцилиарный клиренс, кашель, муколитическая терапия, болезни органов дыхания.
К числу основных факторов патогенеза воспалительных респираторных заболеваний относится нарушение механизма мукоцилиарного транспорта, что чаще всего связано с избыточным образованием и/или повышением вязкости бронхиального секрета [1–3]. Причем независимо от генеза воспалительного процесса в бронхах (инфекционного, аллергического, ирритативного) основные его клинические проявления — это наличие кашля и нарушение оттока мокроты.
Воздух поступает в респираторные отделы легких через верхние (рото- и носоглотка, гортань) и нижние (трахея, бронхи, бронхиолы) дыхательные пути. Проходя через них, он согревается, увлажняется и очищается. Инородные частицы и микроорганизмы, поступающие с вдыхаемым воздухом, осаждаются на слизистых респираторного тракта и в дальнейшем выводятся из дыхательных путей вместе со слизью благодаря содружественной работе ресничек мерцательного эпителия трахеи и бронхов. Гиперсекреция в поврежденных бронхах определяется морфологическими и воспалительными изменениями в трахеобронхиальном дереве. Одними из ведущих факторов патогенеза воспаления при заболеваниях бронхиального дерева являются нарушение образования и эвакуации трахеобронхиального секрета и, как следствие, дезорганизация функции системы самоочищения бронхов, которая играет важную роль в защите легких от проникновения в них мелких твердых частиц и микроорганизмов.
Образование бронхиального секрета и его продвижение в проксимальном направлении от альвеол к крупным бронхам является одним из важных физиологических процессов в организме человека. У детей, даже раннего возраста, система очищения легких функционирует достаточно хорошо.
Источником образования трахеобронхиального секрета являются бронхиальные железы, бокаловидные клетки, секреторные клетки Клара, эпителий бронхиол и альвеол (рис. 1). Количество клеток, вырабатывающих бронхиальный секрет, увеличивается в направлении от альвеол к трахее. Мерцательный эпителий респираторного тракта обеспечивает постоянное движение секрета в направлении полости рта, что способствует эвакуации из дыхательных путей клеточных остатков, инородных частиц, патологических агентов. Трахеобронхиальный секрет благодаря своему составу не только механически защищает слизистую дыхательных путей от микроорганизмов, но и сам оказывает бактериостатическое действие.
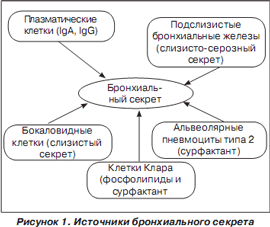
Бронхиальный секрет представляет собой сложную систему, на 95 % состоящую из воды. В его состав также входят клеточные элементы (цилиарный эпителий, макрофаги и др.), органические соединения и микроэлементы, появившиеся в нем как следствие синтеза клеток респираторного эпителия и бронхиальных желез, а также из плазмы крови.
Вязкость бронхиального секрета (мокроты) определяется соотношением двух фаз: наружного слоя — геля (плотного и нерастворимого) и внутреннего слоя — золя (жидкого и растворимого). Золь — это секрет желез, капиллярный транссудат, межклеточная жидкость. Он находится под более плотным слоем геля и напоминает по вязкости плазму. Золь продуцируется в бронхиолах и альвеолах и содержит биологически активные вещества, ферменты, иммуноглобулины, что обусловливает выраженную биологическую защитную функцию слизи. Именно в этом слое реснички мерцательного эпителия совершают свои колебательные движения и передают кинетическую энергию наружному слою трахеобронхиального секрета. Благодаря постоянному движению ресничек существенно укорачивается продолжительность контакта микроорганизмов с клетками слизистых оболочек дыхательных путей и, следовательно, значительно затрудняется проникновение возбудителей в трахеобронхиальный эпителий [2, 4–6].
Гель — это более вязкий поверхностный слой слизистой бронхов, располагающийся на ресничках мерцательного эпителия в виде непрерывной подвижной пленки, в состав которой входят гликопротеины, альбумин, лизоцим, альфа-1-антитрипсин, IgA, сурфактант, комплекс липидов. Гель формируется в результате смешивания золя с секретами бокаловидных и серомукоидных клеток. Перемещение геля, содержащего комочки слизи, осевшие микроорганизмы, чужеродные частицы, становится возможным только после разрыва поперечных дисульфидных связей между гликопротеинами. Гель расположен над ресничками, погруженными в жидкий золь.
Процесс физиологического очищения дыхательных путей называется мукоцилиарным клиренсом (МЦК). У здоровых детей мукоцилиарный клиренс является основным механизмом очищения трахеобронхиального дерева. Выведение бронхиального содержимого обеспечивается перистальтическими скоординированными движениями мелких бронхов и ресничек мерцательного эпителия. Здоровый человек за сутки продуцирует от 10–15 до 100– 150 мл бронхиального секрета. Процесс образования секрета и его выведения является одной из защитных функций органов дыхания. В клинической практике обычно пользуются термином «мокрота», которая представляет собой смесь бронхиального секрета и слюны. Бронхиальный секрет в чистом виде можно получить только при бронхоскопии. Нарушение МЦК происходит как при избыточном образовании мокроты, так и при недостаточном.
Повышение вязкости мокроты нарушает координированную работу МЦК. На функцию мерцательного эпителия оказывает отрицательное влияние ряд факторов: токсины вирусов и бактерий; вдыхание табачного дыма, чистого кислорода, горячего воздуха, аммиака, формальдегида.
Воспаление трахеи и бронхов сопровождается компенсаторным увеличением слизеобразования. Одновременно с гиперпродукцией слизи изменяется и состав трахеобронхиального секрета — в нем уменьшается удельный вес воды и повышается концентрация муцинов (нейтральных и кислых гликопротеинов). Это приводит к увеличению вязкости мокроты (рис. 2). Известно, что чем выше вязкость слизи, тем ниже скорость ее проксимального продвижения по респираторному тракту. Воспаление нижних дыхательных путей не только приводит к нарушениям реологических свойств трахеобронхиальной слизи, но может сопровождаться развитием структурных изменений клеток мерцательного эпителия в виде нарушения ультраструктуры ресничек и их пространственной ориентации, деструкции клеточных органелл и др. Все это способствует нарушению работы мерцательного эпителия и снижению эффективности мукоцилиарного клиренса в целом. Происходит застой мокроты, в результате страдает дренажная функция бронхов, нарушается вентиляционно-респираторная функция легких, снижается эффективность защитных механизмов, таких как мукоцилиарный транспорт и кашель, нарастает колонизация бронхов патогенной микрофлорой. Нарушение транспорта мокроты приводит к поддержанию и прогрессированию бронхолегочного воспаления, к развитию бронхиальной обструкции.
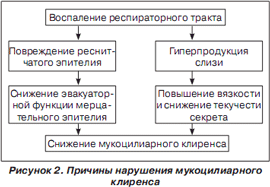
В результате нарушения дренажной функции легких рефлекторно возникает кашель, роль которого заключается в физиологическом очищении дыхательных путей от патологических веществ. Однако в отличие от мукоцилиарного клиренса кашель имеет вспомогательное значение в очищении трахеобронхиального дерева. У здоровых детей кашель наблюдается очень редко, он может появляться только в тех случаях, когда слизь во время сна скапливается в гортани. Кашель является первым звеном в цепи элементов, направленных на улучшение работы МЦК.
В формировании кашлевого рефлекса участвуют:
— кашлевые рецепторы, располагающиеся по ходу гортани, трахеи, бронхов, плевры, слухового прохода, полости носа, околоносовых пазух, глотки, перикарда, диафрагмы, желудка;
— афферентные нервы;
— кашлевой центр (продолговатый мозг);
— эфферентные нервы;
— дыхательные мышцы.
У детей раннего возраста в силу анатомо-физиологических особенностей кашлевой рефлекс несовершенен. Поэтому при воспалительных заболеваниях респираторного тракта у новорожденных и детей первых месяцев жизни кашель нередко отсутствует. Кроме того, кашель у детей раннего возраста может способствовать появлению синдрома срыгивания и рвоты, отказу от еды.
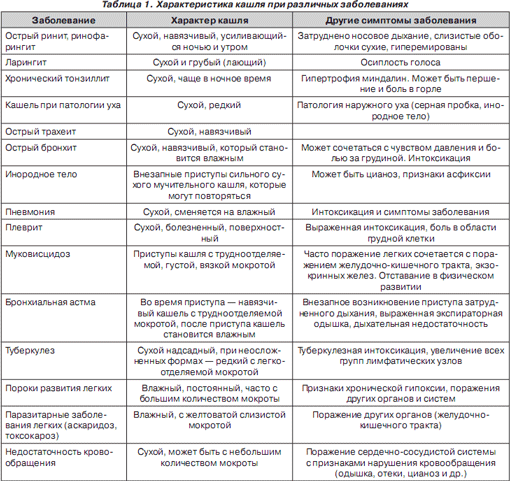
Одной из важнейших характеристик кашля является его продуктивность, т.е. наличие мокроты. В зависимости от количества и качества образующейся в дыхательных путях мокроты различают сухой и влажный кашель (табл. 1). При влажном кашле у детей первых 4–6 лет жизни наличие мокроты обнаружить трудно, так как они ее, как правило, проглатывают. При влажном кашле очень важно обратить внимание на цвет и характер мокроты, которые зависят от характера воспалительного процесса. В некоторых ситуациях кашель является неэффективным и не выполняет дренажной функции.
Неэффективность кашля может быть обусловлена:
— недостаточно выраженным кашлевым рефлексом;
— большой вязкостью мокроты;
— недостаточно глубоким дыханием;
— нарушением бронхиальной проходимости.
Кашель может быть проявлением воспалительного процесса как верхних (ротоносоглотка, гортань), так и нижних (трахея, бронхи) отделов респираторного тракта, а также легочной ткани и плевры (табл. 1).
В настоящее время существует большое количество различных препаратов, влияющих на кашель, которые можно разделить на противокашлевые и мукоактивные. В дебюте острого воспалительного заболевания органов дыхания, как правило, возникает сухой кашель, в связи с чем в этот период показаны препараты, стимулирующие секрецию. При непродуктивном кашле — препараты, разжижающие мокроту, а при появлении продуктивного влажного кашля — мукорегуляторы, нормализирующие образование и состав бронхиального секрета. Наличие кашля требует назначения отхаркивающих средств.
Противокашлевые средства (аntitussiva) — лекарственные препараты, подавляющие кашлевой рефлекс. Терапевтический эффект при их применении достигается за счет снижения чувствительности рецепторов трахеобронхиального дерева или в результате угнетения кашлевого центра продолговатого мозга. Противокашлевые препараты назначаются при сухом, мучительном, непродуктивном кашле, который приводит к нарушению сна и общему истощению пациента при различных воспалительных процессах респираторной системы.
Противокашлевые средства противопоказаны:
— при гиперсекреции слизи, наблюдающейся при любых заболеваниях верхних и нижних дыхательных путей;
— бронхообструктивном синдроме;
— легочном кровотечении.
Выделяют противокашлевые средства центрального и периферического действия. Противокашлевые препараты центрального действия подавляют кашлевой рефлекс за счет угнетающего воздействия на кашлевой центр продолговатого мозга. Средства центрального действия подразделяются на наркотические (кодеин, этилморфин, морфин) и ненаркотические (глауцин, окселадин, бутамират). В педиатрической практике использовать наркотические противокашлевые препараты центрального действия не рекомендуется.
В настоящее время созданы препараты центрального действия, не влияющие на дыхательный центр и не вызывающие привыкание и лекарственную зависимость. К этой группе препаратов относятся синекод, глаувент, пакселадин, тусупрекс, которые могут использоваться в детском возрасте.
В основе механизма действия противокашлевых препаратов периферического действия лежит торможение кашлевого рефлекса за счет снижения чувствительности рецепторов трахеобронхиального дерева. К этой группе препаратов относятся либексин и гелицидин. Они оказывают хорошее противокашлевое действие в течение 3–4 ч, а также некоторый бронхолитический эффект за счет расслабления гладких мышечных волокон и местноанестезирующее действие на слизистую верхних дыхательных путей. В отличие от наркотических препаратов центрального действия средства периферического действия не угнетают дыхательный центр и к ним не развивается лекарственная зависимость.
Противокашлевые препараты противопоказаны при всех патологических состояниях, сопровождающихся обильным отделением мокроты и легочным кровотечением.
Следует подчеркнуть, что у детей, особенно раннего возраста, кашель чаще обусловлен повышенной вязкостью бронхиального секрета, нарушением «скольжения» мокроты по бронхиальному дереву, недостаточной активностью мерцательного эпителия. Поэтому основной целью терапии в подобных случаях является разжижение мокроты, снижение ее адгезивности и увеличение тем самым эффективности кашля.
Лекарственные препараты, улучшающие откашливание мокроты, можно разделить на несколько групп:
— средства, стимулирующие отхаркивание;
— муколитические (или секретолитические) препараты;
— комбинированные препараты.
Средства, стимулирующие отхаркивание. Среди них выделяют рефлекторно действующие препараты и препараты резорбтивного действия. Рефлекторно действующие препараты при приеме внутрь оказывают умеренное раздражающее действие на рецепторы желудка, что возбуждает рвотный центр продолговатого мозга, рефлекторно усиливают секрецию слюнных и слизистых желез бронхов. К этой группе относятся препараты термопсиса, алтей, солодка, терпингидрат, эфирные масла и др. Действующим началом отхаркивающих средств растительного происхождения являются алкалоиды и сапонины, которые способствуют регидратации слизи за счет увеличения транссудации плазмы, усилению моторной функции бронхов и отхаркиванию за счет перистальтических сокращений, повышения активности мерцательного эпителия.
Ко второй группе относят препараты резорбтивного действия: натрия и калия йодид, аммония хлорид, натрия гидрокарбонат и другие солевые препараты, которые, всасываясь в желудочно-кишечном тракте, выделяются слизистой оболочкой бронхов и, увеличивая бронхиальную секрецию, разжижают мокроту, облегчают отхаркивание. Йодосодержащие препараты также стимулируют расщепление белков мокроты при наличии лейкоцитарных протеаз.
Выбор муколитической терапии определяется характером поражения респираторного тракта. Муколитики широко используются в педиатрии при лечении заболеваний нижних дыхательных путей, как острых (трахеиты, бронхиты, пневмонии), так и хронических (хронический бронхит, бронхиальная астма, врожденные и наследственные бронхолегочные заболевания, в том числе муковисцидоз). Назначение муколитиков показано и при болезнях ЛОР-органов, сопровождающихся выделением слизистого и слизисто-гнойного секрета (риниты, синуситы).
С другой стороны, существенное значение имеют возрастные особенности реагирования дыхательных путей на инфекционно-воспалительный или аллергический процесс. В частности, в неонатальном периоде высокая частота, затяжное и осложненное течение респираторной патологии обусловлены анатомо-физиологическими особенностями новорожденного. Одним из причинных факторов может явиться дефицит образования и выброса сурфактанта, в том числе качественный его дефицит. Кроме того, отсутствие кашлевого рефлекса у детей первых дней и недель жизни достаточно часто требует принудительного отсасывания слизи из верхних и нижних дыхательных путей, что может привести к травмированию и инфицированию слизистых. Особенностью физиологических реакций детей первых трех лет жизни является выраженная гиперпродукция и повышение вязкости слизи в сочетании с отеком слизистой бронхов, что вторично нарушает мукоцилиарный транспорт, вызывает обструкцию бронхов, способствует развитию инфекционного воспаления. Таким образом, при проведении комплексной терапии у детей с респираторной патологией необходимо учитывать возраст ребенка и характер патологического процесса в бронхах (рис. 3).Муколитики, безусловно, наиболее часто являются препаратами выбора у детей первых трех лет жизни.
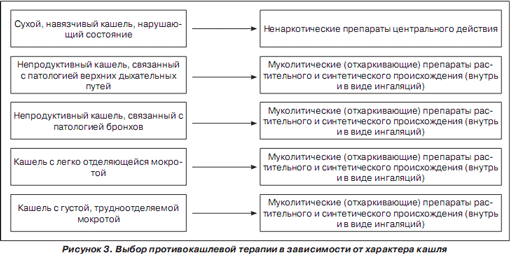
Известно много синтетических препаратов, воздействующих на мокроту, но до настоящего времени с целью нормализации МЦК в большинстве случаев успешно применяются препараты растительного происхождения [6, 8, 10–14]. Традиционными отхаркивающими средствами в педиатрической практике являются тимьян (чабрец) и подорожник, которые входят в состав препарата Эвкабал сироп от кашля. Тимьян и подорожник имеют разные фармакологические свойства, которые в комбинации работают синергично, обеспечивая отхаркивающий, бронхоспазмолитический, секретолитический и противовоспалительный эффект, обусловливая общую эффективность данного
фитопрепарата при остром бронхите с продуктивным кашлем [15].
Основными действующими компонентами тимьяна (чабрец, богородская трава) являются эфирные масла, в особенности тимол. Они действуют местно в легких, поскольку выводятся из организма через дыхательные пути, дезинфицируя их, уменьшая бронхоспазм и проявляя муколитическое действие [16]. Экстракт чабреца благодаря наличию в его составе фитонцидов и фенолов оказывает бактерицидное действие в отношении кокковой микрофлоры и бактериостатическую активность в отношении многих грамотрицательных бактерий. Кроме того, фенолы проявляют активность в отношении антибиотикорезистентной микрофлоры, в том числе L-форм и грибов. Минимальное содержание фенолов в растворе обеспечивает антибактериальное и антимикотическое действие. Отхаркивающее и секретолитическое действие эфирного масла и флавоноидов чабреца обусловлено ферментированием густого вязкого секрета и повышением подвижной активности мерцательного эпителия. Большей частью эффект зависит от свойства поверхностно-активного вещества эфирного масла изменять коллоидное состояние мокроты. Спазмолитический эффект флавоноидов обеспечивает умеренную бронходилатацию, облегчение дыхания, особенно экспираторной фазы.
В листьях подорожника найдены гликозид аукубин, расщепляющийся при гидролизе на аукубигенин и глюкозу, флавоноиды, витамин К, аскорбиновая кислота, дубильные вещества, горечи, следы алкалоидов, полисахариды и т.д. В семенах содержатся слизь, жирное масло, углевод плантеоза. При фармакологическом исследовании препаратов из листьев подорожника установлен их широкий спектр лечебного действия: подорожник используется как мочегонное, потогонное, обезболивающее, противовоспалительное, противоопухолевое, антимикробное и успокаивающее средство. Водный настой из листьев подорожника оказывает отхаркивающее действие, усиливает активность ресничек мерцательного эпителия дыхательных путей, что ведет к усилению секреции бронхиальной слизи, вследствие чего мокрота разжижается и облегчается ее выделение при кашле; используется при бронхитах, коклюше, бронхиальной астме, туберкулезе. Экстракт
из листьев оказывает седативное и гипотензивное действие.
Препарат Эвкабал сироп от кашля следует принимать в неразбавленном виде после еды. Рекомендуемые дозы: дети в возрасте от 6 месяцев до 1 года — по 1 чайной ложке 1 раз/сутки; детям от 1 года до 5 лет — 1 чайная ложка 2 раза/сутки; в школьном возрасте — по 1 столовой ложке 2 раза/сутки. Взрослым — по 1–2 столовые ложки 3–5 раз/сутки. Длительность приема препарата определяется индивидуально, в зависимости от тяжести заболевания, и обычно составляет 2–3 недели. Рекомендуется принимать препарат еще в течение 2–3 дней после исчезновения симптомов заболевания.
Хороший эффект дает применение препарата Эвкабал бальзам С в виде паровых ингаляций. Во время ингаляции эвкалиптовое и хвойное масла непосредственно достигают слизистых оболочек дыхательных путей, оказывая целебное воздействие также на мускулатуру бронхов и нервные рецепторы. Благодаря этому бронхиальный секрет разжижается и облегчается его выделение, восстанавливается свободное дыхание, прекращается кашель. Особенно хорошо зарекомендовал себя в педиатрической практике, в частности у младенцев начиная с трехмесячного возраста, а также у пациентов с ослабленной иммунной системой без возрастных ограничений. Нет ограничений для применения препарата Эвкабал бальзам С и в период беременности и лактации.
1. Домбровская Ю.Ф. Заболевания органов дыхания у детей. — М.: Медгиз, 1957. — 345 с.
2. Рачинский С.В., Таточенко В.К. Болезни органов дыхания у детей. — М.: Медицина, 1987. — 496 с.
3. Волосовец А.П., Юлиш Е.И. Рациональная антибиотикотерапия респираторных заболеваний у детей. — Донецк, 2004. — 389 с.
4. Lucas A.M., Douglas L.C. Principles underlying ciliary activity in the respiratory tract // Arch. Otolaryng. — 1984. — V. 20. — P. 518-541.
5. Федосеев Г.Б., Жихарев С.С. Основные механизмы защиты бронхолегочной системы // Болезни органов дыхания / Под ред. Н.В. Путова. М.: Медицина, 1989. — Т. 1. — С. 112-143.
6. Маев И.В. Муколитические средства в терапии хронической обструктивной болезни легких // Новости медицины и фармации. — 2004. — № 15. — С. 3-4.
7. Делягин В.М., Быстрова Н.Ю. Антибактериальные и мукоактивные препараты. — М.: Алтус, 1999.
8. Царегородцев А.Д., Таболин В.А. Руководство по фармакотерапии в педиатрии и детской хирургии // Пульмонология. — М., 2002. — С. 123-144.
9. Зайцева О.В., Левин А.Б. Рациональный выбор муколитической терапии в комплексном лечении детей с осложненными формами пневмонии // Современная педиатрия. — 2005. — № 3 (8). — С. 103-110.
10. Замотаев И.П. Фармакотерапия в пульмонологии. — М., 1993.
11. Белоусов Ю.Б., Омельяновский В.В. Муколитические и фитотерапевтические средства. Клиническая фармакология болезней органов дыхания. — М.: Универсум Паблишинг, 1996. — С. 131-141.
12. Компендиум, лекарственные препараты / Под ред. проф. В.Н. Коваленко, проф. А.П. Викторова. — К.: Морион, 2007.
13. Кривопустов С.П. Сучасні підходи до діагностики та лікування кашлю у дітей // Мистецтво лікування. — 2003. — № 3.— С. 37-41.
14. Wienman H.M. Ambroxol (Mucosolvan) in pediatrics. Clinical results with different forms of administration // Therapiewoche. — 1981. — 31. — 7940-7947.
15. Thymi herba (Thyme). ESCOP Monographs. European Scientific Cooperation on Phytomedicine, Elburg; 2003.
16. Kohlert C. Systemische Verfugbarkeit und Pharmakokinetik von Thymol nach oraler Applikation einer thymian-haltigen Zubereitung im Menschen [Dissertation]. — Wurzburg: Bayerische Julius-Maximilians-Universitat Wurzburg; 2001.
