Газета «Новости медицины и фармации» 10(326) 2010
Вернуться к номеру
Гастроінтестинальні прояви харчової алергії. Огляд літератури
Авторы: Т.З. Марченко, Л.П. Сакалош. Львівський національний медичний університет імені Данила Галицького, Кафедра педіатрії і неонатології ФПДО
Версия для печати
Гастроінтестинальні прояви харчової алергії — це ураження травного каналу в результаті імунної відповіді на харчові антигени [1], які можуть бути IgE-опосередковані й не-IgE-опосередковані (IgG-/IgM-зумовлені або Т-залежні) [2]. Вони займають друге місце серед патологій, які викликає харчова алергія [3]. До IgE-залежних і/або клітинноопосередкованих належать еозинофільна гастроентеропатія, яка часто поєднується із алергічними ураженнями шкіри, до клітинноопосередкованих — ентеропатія, еозинофільний коліт, проктит внаслідок алергії до білків їжі; а також целіакія і пов’язаний з нею герпетиформний дерматит. До гастроінтестинальних проявів харчової алергії належать: афтозні виразки в роті, географічний язик, синдром оральної алергії, гастрит, коліт (за МКХ-10 — К52.2. Алергічний і аліментарний гастроентерит і коліт), гастроезофагеальний рефлюкс і навіть виразка шлунка та дванадцятипалої кишки і дискінезія кишечника [3].
 Людина народжується здоровою,
Людина народжується здоровою,
а хвороби приходять до неї через рот
із продуктами харчування.
Гіппократ
Перші вказівки на незвичайні реакції на їжу належать ще Гіппократу, який описав прояви підвищеної чутливості до молока. Анафілактичні реакції на яйце і рибу були описані в XVI і XVII століттях [4]. Протягом сторіч реакціям на харчові продукти приділяли увагу лікарі та їх пацієнти. У XX столітті відбувся якісний перелом як у погляді на склад харчового раціону звичайної людини, так і в спробах пояснити можливі механізми незвичайних реакцій на продукти. Різноманіття клінічних проявів, відсутність загальноприйнятої класифікації, можливості «безмежної інтерпретації невідомих механізмів» реакцій на харчові продукти сьогодні часто призводять до сумнівного діагнозу й невиправданих обмежень раціону харчування [3].
Виділяють три форми алергічної реакції органів травлення [6]:
Відомо, що багато запальних і дистрофічних процесів у травному каналі посилюють реакцію «антиген — антитіло» у три — п''ять разів із формуванням в організмі «шокового органу». Одночасно доведено, що алергічний компонент лежить в основі 20 % захворювань органів травного каналу.
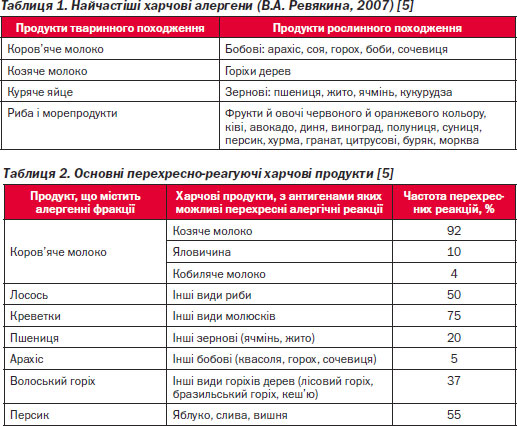
В основі орального алергічного (ОАС) синдрому лежать IgE-залежні алергічні реакції. Клінічні ознаки розвиваються через декілька хвилин після їжі й проявляються сверблячкою губ, слизової оболонки порожнини рота, іноді виникає набряк губ, язика, піднебіння, може бути фарингіт і ларингіт. Алергічний ринокон''юнктивіт виявляється у 2/3 випадків. Анамнез таких пацієнтів зазвичай обтяжений полінозом. Провокуючими факторами ОАС переважно є вживання свіжих фруктів і сирих овочів (яблуко, вишня, персик, кріп, селера тощо), а також контакт з пилком рослин причинно-значущих фруктів або овочів, споріднених їм рослин, що мають схожі антигенні детермінанти. Рідше синдром асоціюється з іншими відомими продуктами (горіхи дерев, арахіс, яйця, молоко або риба). ОАС не характерний для грудних дітей [7].
В основі негайної гастроінтестинальної алергічної гіперчутливості лежать IgE-залежні алергічні реакції, які індукуються коров''ячим молоком, яйцем, пшеницею, соєю, арахісом, горіхами дерев, морепродуктами. Гострий початок із розвитком симптомів через короткий проміжок часу (від декількох хвилин до 1–2 годин) після харчової провокації виявляється нудотою, блюванням, болями в животі з супутньою діареєю [8].
Гастроезофагеальний рефлюкс (ГЕР) відноситься до функціональних розладів травного каналу, що в пацієнтів грудного віку асоційовані переважно з гіперчутливістю до білка коров''ячого молока. 16–42 % дітей першого року життя з проявами ГЕР страждають від алергії до коров''ячого молока. Зазвичай у них проявляються супутні шкірні симптоми харчової алергії або є ознаки алергічного ураження інших органів. Клінічно ГЕР, індукований білками коров''ячого молока, не відрізняється від ГЕР, індукованого іншими причинами. Повторні відрижки і блювота є типовими симптомами рефлюксу в грудних дітей. Бронхообструктивний синдром, що важко піддається лікуванню, є наслідком аспірації харчових мас. Найчастіше відрижки спостерігаються після переводу дитини на вигодовування замінниками грудного молока, приготованими на основі цільного коров''ячого молока. У цьому випадку добрий ефект має заміна сумішей на основі коров''ячого молока на спеціальні лікувальні суміші, що підтверджує роль харчової алергії в етіології рефлюксу [7, 9, 10].
Дитячі кишкові коліки асоційовані перш за все з алергією до білка коров''ячого молока. Більше ніж 40 % немовлят із симптомами алергії до коров''ячого молока страждають від болісних кишкових колік.
Заміна сумішей на основі незбираного коров''ячого молока на високогідролізовані лікувальні суміші більш ефективна, ніж медикаментозне лікування або годування дитини безлактозною сумішшю. Питання про роль алергії до білка коров''ячого молока в механізмі виникнення кишкових колік у грудних дітей, які не мають клінічних ознак харчової алергії з боку інших органів і систем, є предметом дискусій [10, 18].
Термін «еозинофільна гастроентеропатія» об''єднує групу захворювань травного каналу, в основі яких лежать IgE-залежні і/або клітинноопосередковані імунні механізми гіперчутливості до їжі: еозинофільний алергічний езофагіт, еозинофільний алергічний гастрит, еозинофільний алергічний гастроентерит/гастроентероколіт. Найчастішими харчовими алергенами, відповідальними за розвиток еозинофільної гастроентеропатії, є коров''яче молоко, яйце, пшениця, соя. Патологія може спостерігатися у дітей різного віку [10, 11, 16].
Термін «еозинофільний езофагіт» (ЕЕ) на теренах СНД з''явився зовсім недавно, тоді як у США і Європі ця патологія вже декілька десятиріч займає одне з провідних місць у структурі гастроентерологічних захворювань. За даними дослідження R. Noel і співавторів [10], проведеного в 2003 році серед дитячого населення штату Огайо (США), частота ЕЕ становила 1 випадок на 10 тис. на рік, а його поширеність в цій популяції наближається до 4 на 10 тис. населення.
Приблизно в 50 % дітей з ЕЕ присутні інші прояви алергії: бронхоспазм, екзема, алергічний риніт. Близько 35–45 % пацієнтів мають сімейний анамнез харчової алергії або бронхіальної астми. Стриктури, пов''язані з ЕЕ, більш схильні до рецидиву, ніж пептичні стриктури при ГЕРХ [11].
З огляду на вищевказане алергія стравоходу може мати один із трьох наведених варіантів розвитку: 1) стравохід є вхідними воротами для сенсибілізації організму різними алергенами; 2) езофагіти, дивертикуліти, виразки стають тригерними факторами розвитку загальних чи місцевих алергічних реакцій і збільшують їх частоту; 3) перетворення власне стравоходу в «шоковий орган» з відповідними функціональними і органічними змінами різного ступеня тяжкості [12].
У клінічній картині дітей раннього віку переважають відрижка, нудота, блювота, відсутність апетиту, болі в животі, неспокій, а у старших дітей — скарги на відчуття клубка в горлі, пирхоти, печію, болі в грудях, інші ознаки дисфагії. На відміну від класичного рефлюкс-езофагіту, еозинофільний езофагіт не завжди пов''язаний з ГЕР. При ЕЕ слизова оболонка стравоходу уражається по всій довжині, а не тільки в дистальному відділі, як при рефлюкс-езофагіті. У біоптатах слизової оболонки стравоходу виявляються еозинофільна інфільтрація з вогнищевою проліферацією Т-клітин у слизовій оболонці й підслизовому шарі, гіпертрофія папілярної та базальної зон. Кількість еозинофілів досягає 15–25 у полі зору мікроскопа. При рефлюкс-езофагіті без явищ харчової алергії вміст тканинних еозинофілів у слизовій оболонці стравоходу не перевищує п''ять клітин у полі зору мікроскопа. Останнім часом з''явилися повідомлення, що для даної патології характерна висока травматичність слизової оболонки, для її опису навіть був запропонований термін «слизова типу «цигаркового паперу».
При тривалому перебігу ЕЕ виникають стриктури, кільця, борозни й білуваті нашарування. Інтрагастральна рН-метрія при ЕЕ не змінена, а попередня антисекреторна терапія неефективна [12].
Підтверджує діагноз еозинофільного алергічного езофагіту позитивний ефект після елімінації харчового алергену й призначення топічних або системних глюкокортикостероїдів [14].
Проявами еозинофільного алергічного гастроентериту є больовий синдром, блювота, порушення апетиту, ознаки ГЕР, можлива затримка фізичного розвитку дитини при тривалому перебігу хвороби. Інфікування H.pylori може супроводжувати
еозинофільний гастродуоденіт, що, проте, не виключає алергічного характеру патологічного процесу. Доведено, що H.pylori підвищує проникність слизової оболонки травного каналу для харчових алергенів і навіть може сприяти розвитку харчової алергії [15]. Ендоскопічно при цьому зазвичай виявляється антральний гастрит. Підтверджують еозинофільну інфільтрацію результати гістологічного дослідження слизової оболонки шлунка й тонкого кишечника. Щільність еозинофілів перевищує 20 клітин у полі зору мікроскопа. Резистентність до традиційної протизапальної терапії характерна для еозинофільного алергічного гастроентериту [11, 12, 14].
В основі ентеропатії, зумовленої алергією до білків їжі (білків коров''ячого молока, хоча причиною можуть бути також соя, злаки, яйця і морепродукти), лежать Т-клітинноопосередковані імунні механізми. Частіше за все ентеропатії спостерігаються в дітей першого року життя. Маніфестує захворювання, як правило, у пацієнтів віком чотири місяці. Основними клінічними проявами цієї ентеропатії є синдром мальабсорбції з хронічною діареєю, блювотою, метеоризмом на фоні затримки росту й нервово-психічного розвитку. Втрата білка при діареї може призводити до гіпопротеїнемії з розвитком набряків. Нерідко в дітей розвивається анемія. У біоптатах слизової оболонки тонкого кишечника виявляється атрофічний ентерит з незначною атрофією ворсинок і гіперплазією крипт. При морфологічному дослідженні виявляються інтраепітеліальні лімфоцити, підвищена кількість тканинних еозинофілів. Симптоми ентеропатії зазвичай припиняються у більшості пацієнтів віком до одного — трьох років унаслідок формування толерантності до білків коров''ячого молока [16].
Ентероколіт, зумовлений алергією до білків їжі, виникає внаслідок клітинноопосередкованих імунних механізмів. Харчовими алергенами для розвитку ентероколіту є соя (50 % пацієнтів), рис, деякі злакові (овес тощо), м''ясо птиці. Дебют захворювання — у дітей віком від одного тижня до трьох місяців із залученням до патологічного процесу тонкого та товстого кишечника. Рецидивуюча блювота й діарея при постійному надходженні небажаного харчового продукту викликають втрату рідини, поживних речовин, тому дитина стає млявою, відбувається затримка її фізичного розвитку. Блювота й діарея, що виникають при періодичному надходженні алергену через дві години після годування, призводять до дегідратації, ацидозу з метгемоглобінемією. У тяжких випадках клінічна картина може нагадувати сепсис із нейтрофільним лейкоцитозом у периферичній крові. У біоптатах слизової оболонки товстого кишечника виявляються абсцеси крипт і дифузна інфільтрація клітинами запалення. У складі клітинного інфільтрату переважають плазматичні клітини. У біоптатах слизової оболонки тонкого кишечника виявляються ознаки гострого запалення, набряк, незначне пошкодження ворсинок [16, 17].
Проктит/проктоколіт, зумовлений алергією до білків їжі, є клітинноопосередкованим імунним механізмом. Найбільш часто дане захворювання викликають коров''яче молоко, соя. Описаний випадок захворювання після вживання дитиною суміші на основі гідролізату казеїну. На фоні грудного вигодовування також можливий розвиток хвороби через проникнення антигенів коров''ячого молока в грудне молоко матері. Захворювання звичайно маніфестує в перші місяці життя дитини; середній вік початку клінічних проявів — до двох місяців. У дітей із цим захворюванням виявляється слиз з видимими вкрапленнями або смужками крові в калі при зовнішньому видимому благополуччі. Втрата крові мінімальна, у зв''язку з чим анемія розвивається рідко. При ендоскопічному дослідженні виявляється вогнищевий або дифузний коліт із набряком і ерозіями слизової оболонки товстого кишечника. У колонобіоптатах виявляють еозинофільну інфільтрацію слизової оболонки і гіперплазію лімфоїдних фолікулів [18, 19].
A. Ojuawo, D. St Louis та співавтори навели результати обстеження 42 дітей віком до двох років із хронічною неспецифічною діареєю з гістологічно підтвердженим колітом [20]. Період спостереження тривав понад п''яти років. Алергічний коліт був найпоширенішим явищем у цій групі дітей і зустрічався в 62 % хворих. Інші форми діагностованого коліту включали неспецифічний коліт, автоімунний ентероколіт і виразковий коліт, частота кожного з яких становила по 10 %. Крім того, у 7 % випадків визначався виражений комбінований імунодефіцит, а у 3 % дітей була діагностована хвороба Крона. У 48 % випадків була виявлена спадкова схильність до атопії, а у 29 % дітей в анамнезі виявлялися атопічні реакції.
Рівні сироваткового імуноглобуліну G2 і G4 були дуже низькими в більше ніж 50 % дітей з колітом, а у 66 % з них із вираженим комбінованим імунодефіцитом, автоімунним ентероколітом і виразковим колітом (n = 11) був знижений уміст СD3 і CD4 у поєднанні з підвищенням кількості CD8 у 2/3 дітей.
Рівень Т-лімфоцитів не був змінений у дітей з алергічним колітом. Таким чином, у дітей з підтвердженим неінфекційним колітом виявлялося переважання дефіциту IgA, IgG2 і IgG4. Можна припускати, що такий незначний дефіцит продукції імуноглобулінів відіграє роль у патогенезі колітичного процесу [20].
При целіакії розвиток захворювання індукований харчовим білком — гліадином, що міститься в пшениці, вівсі, ячмені. Клінічні прояви целіакії — блювота, діарея, відсутність апетиту, затримка росту. Початкові симптоми хвороби можуть спостерігатися на першому році життя дитини після введення в раціон харчування глютенумісного прикорму. Проте класична клінічна картина частіше за все розвивається у віці більше одного року. При морфологічному дослідженні біоптатів слизової оболонки тонкого кишечника виявляється атрофічний ентерит. Для підтвердження діагнозу визначають серологічні маркери целіакії: автоантитіла до тканинної трансглутамінази, антигліадинові IgA-антитіла [21, 22].
Необхідно пам''ятати про роль харчової алергії в розвитку запорів у дітей. Запори спостерігаються у дітей віком понад два роки, у яких, як правило, обтяжений особистий або сімейний анамнез алергічними захворюваннями. Морфологічною основою патологічного процесу є лімфоцитарна інфільтрація, інтерстиціальний набряк, еозинофільна інфільтрація власної пластинки слизової оболонки товстого кишечника з інтраепітеліальними еозинофільними абсцесами. В основі запорів, обумовлених алергією до білків коров''ячого молока, лежить зниження слизоутворення в товстому кишечнику, що призводить до уповільнення пасажу калових мас. Запори резистентні до традиційної терапії, проте виключення з раціону коров''ячого молока має виражений позитивний ефект і призводить до усунення симптомів.
У більшості пацієнтів із гастроінтестинальними проявами харчової алергії формуються вторинна лактазна недостатність і вторинна панкреатична недостатність. Майже в усіх дітей, які мають симптоми ураження травного каналу, на фоні харчової алергії розвивається дисбіоз кишечника [19] — клініко-лабораторний синдром, що характеризується зміною якісного й кількісного складу мікрофлори, метаболічними й імунними порушеннями [23–24].
Дисбіоз кишечника при гастроінтестинальних проявах харчової алергії є вторинним, але він може посилювати порушення функції органів травлення. Основні чинники, що сприяють розвитку дисбіозу кишечника у дітей:
Діагностика гастроінтестинальних проявів харчової алергії [1, 16, 17, 38] передбачає наявність таких клінічних даних, що вказують на харчову алергію або непереносимість їжі:
Ознаки можливої участі харчової алергії в розвитку захворювань травного каналу:
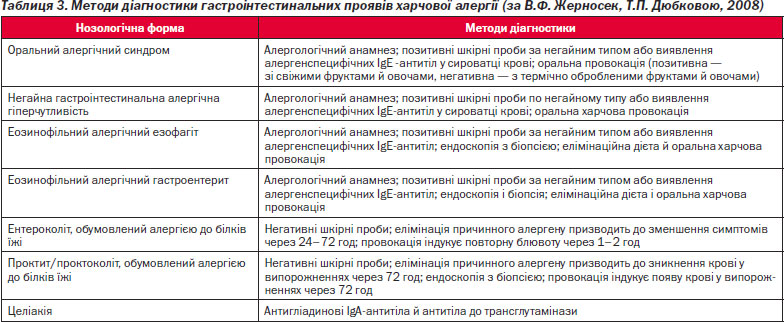
Сучасні методи діагностики гастроінтестинальних проявів харчової алергії систематизовані в табл. 3 [2, 11, 16, 27, 28]. Імовірність постановки точного діагнозу вище при поєднанні декількох методів діагностики і збігу результатів лабораторних та інструментальних методів дослідження з клінічними даними.
Підходи до лікування
Основні напрями лікування уражень травного каналу при харчовій алергії [1, 7, 8, 26, 29, 30]:
Елімінаційні заходи полягають у виключенні з раціону харчування дитини причинно-значущих харчових продуктів і перехресно-реагуючих продуктів із схожими антигенними детермінантами. Оральна харчова провокація доводить етіологічну значущість кожного харчового продукту, що містить алергенні фракції. Єдине протипоказання для харчової провокації — анафілаксія на підозрюваний продукт в анамнезі. Позитивні результати алергологічних шкірних проб або лабораторних методів дослідження за відсутності клінічних проявів харчової алергії не мають самостійної діагностичної цінності (можливість хибнопозитивних результатів).
Раціональна дієтотерапія є основою лікування гастроінтестинальних проявів харчової алергії у дітей. Є думка [7, 11, 29], що при розвитку алергії на фоні грудного вигодовування з раціону харчування матері-годувальниці виключаються коров''яче молоко, куряче яйце, риба, горіхи дерев.
При дефіциті грудного молока або його відсутності прикорм або штучне вигодовування дітей першого року життя проводять лікувальними високогідролізованими сумішами (повний гідроліз білків коров''ячого молока!) із заміною лактози на інші вуглеводи і включенням середньоланцюжкових тригліцеридів. Виключення лактози необхідне у зв''язку з частим поєднанням у дітей грудного віку алергії до білків коров''ячого молока з лактазною недостатністю. Часткова заміна довголанцюжкових тригліцеридів на середньоланцюжкові необхідна, враховуючи наявність у більшості дітей вторинної панкреатичної недостатності. При гастроінтестинальних проявах харчової алергії суміші на основі білка сої протипоказані [31, 32]. Згідно з останніми рекомендаціями Комітету із харчування ESPGHAN, здоровим дітям першого року життя прикорм рекомендується вводити не раніше 17-го і не пізніше 26-го тижня життя [33]. При харчовій алергії прикорм вводять не раніше шести місяців життя. На першому році життя дітям з гастроінтестинальними проявами харчової алергії в раціон не вводять коров''яче молоко, сир, рибу, яйце, до трьох років протипоказані горіхи дерев. Дітям старшого віку призначається індивідуальна гіпоалергенна дієта з обов''язковим виключенням харчових продуктів, етіологічна значущість яких строго доведена харчовою провокацією. Тривалість елімінаційної дієти — не менше шести місяців. При високій чутливості до білків коров''ячого молока тривалість виключення даного продукту харчування з раціону дитини може становити 1–2 роки. У зв''язку з тим, що білок є пластичним матеріалом для організму, що росте, добова потреба в ньому задовольняється збільшенням кількості м''яса. Отже, будь-яка елімінаційна дієта в дитячому віці повинна передбачати заміну продукту, що виключається, іншим, добре переносимим і повноцінним за харчовою й енергетичною цінністю. Дефіцит макро- і мікронутрієнтів при харчовій алергії в дітей недопустимий, оскільки він збільшує наявні порушення й погіршує нутритивний статус, призводячи до затримки росту і нервово-психічного розвитку. Виключення коров''ячого молока з харчування дитини або матері-годувальниці вимагає додаткового введення в раціон кальцію і вітамінів групи B.
У лікуванні гастроінтестинальних проявів харчової алергії антимедіаторна терапія дозволяє зменшити або усунути деякі симптоми хвороби. Для дітей віком до шести місяців використовуються антигістамінні препарати першого покоління: хлоропірамін і диметиндену малеат дозволені з першого місяця життя, прометазин — з двох місяців, хіфенадин — з трьох місяців. Починаючи з шести місяців можуть бути призначені препарати другого та третього поколінь (цетиризин, дезлоратадин) і кетотифен. У віці понад один рік арсенал антимедіаторних препаратів розширяється: з одного року — лоратадин, з шести років — фексофенадин, дезцетиризин, ебастин. Антигістамінні засоби першого покоління застосовуються 7–10 днів, при необхідності тривалого лікування їх чергують. Дезлоратадин, дезцетиризин, фексофенадин, ебастин можуть призначатися протягом одного місяця, якщо в цьому є необхідність. Цетиризин можна безперервно приймати протягом 2–6 міс. На тривалий період призначається також лоратадин [5, 7, 9].
Фрібріс (дезлоратадин) — антигістамінний препарат третього покоління, перший активний метаболіт лоратадину, який в 4–15 разів активніший за свого попередника. Також дезлоратадин виявляє протиалергічну та протизапальну дію в результаті блокування виділення гістаміну з тучних клітин.
Препарат пригнічує ланку цитотоксичних реакцій, на яких грунтується розвиток алергічного запалення: виділення прозапальних цитокінів (ІЛ-4, ІЛ-6, ІЛ-8, ІЛ-23), продукування супероксидного аніону, активованого поліморфноядерними нейтрофілами, адгезію та хемотаксис еозинофілів, експресію молекул адгезії, ІgЕ-залежне виділення гістаміну, простагландину D2 (ПГD2) та лейкотрієну С4 (ЛТС4).
Фрібріс не проникає через гематоенцефалічний бар''єр, не викликає седативного ефекту, добре всмоктується після прийому всередину. Не викликає побічних дій з боку травного каналу. Не потребує специфічних застережень при прийомі пацієнтами з нирковою та печінковою недостатністю.
Фрібріс має високий профіль безпечності, не викликає збільшення інтервалу QT та не має впливу на інші параметри серцевої провідності. Випускається в таблетках та сиропі, що містить виключно ареактогенні допоміжні речовини.
Фрібріс призначають дорослим та дітям від 2 років (сироп). Застосування в дорослих — 1 табл. (5 мг) 1 раз на добу до 30 днів. Застосування у дітей від 2 до 5 років (сироп) — 1/2 мірної ложечки, від 6 до 11 років — 1 мірна ложечка, від 12 років — 2 мірних ложечки 1 раз на добу до 10 днів.
Фрібріс — сучасний протиалергічний препарат, який швидко ліквідує симптоми алергічного процесу, забезпечує виражену клінічну ефективність та безпечність при лікуванні гострих та хронічних алергічних захворювань. Його застосування сприяє швидкому зникненню симптомів захворювання та підвищує якість життя пацієнтів.
Протизапальна терапія передбачає застосування всередину препаратів кромогліцієвої кислоти [40]. Проте при лікуванні ЕЕ кромоглікат натрію і кетотифен недостатньо ефективні. Відзначена позитивна динаміка ЕЕ на фоні прийому топічного кортикостероїду — флутиказону пропіонату, який звичайно використовується для корекції бронхіальної астми. На фоні його прийому у віковій дозі протягом 8 тижнів відзначається досягнення клінічної (до кінця першого тижня прийому) і морфологічної ремісії (істотно зменшується ступінь еозинофільної інфільтрації) [9]. Єдиним описаним ускладненням такої терапії був кандидоз стравоходу, що спостерігався при застосуванні флyтиказону в дозі 220 мг два рази на день [29].
Топічні кортикостероїди з успіхом застосовуються і при інших еозинофільних ураженнях травного каналу в дітей з перших місяців життя. Зокрема, відзначена позитивна динаміка на фоні прийому будесоніду при деяких формах алергічного ентероколіту й проктоколіту [27].
У ряді випадків при тяжких і рефрактерних формах харчової алергії виникає необхідність призначення системних кортикостероїдів і навіть імуносупресантів за життєвими показаннями. Liacouras застосовував метилпреднізолон у дозі 1,5 мг/кг в два прийоми протягом чотирьох тижнів. Після лікування в 19 з 20 пацієнтів відзначено значне клінічне й гістологічне поліпшення. Проте в дев''яти хворих симптоми з''явилися знов при терміні спостереження до одного року [1, 28].
У даний час активно вивчається застосування антицитокінових і антилейкотрієнових препаратів при деяких формах еозинофільного ураження органів травлення, у тому числі й при ЕЕ. Зокрема, в західних країнах активно вивчається ефективність інгібітору експресії рецептора лейкотрієну (cys-LT1) — препарату монтелукаст (montelukast) [34]. Він блокує дію лейкотрієну D4, який є специфічним еозинофільним хемоатрактантом. Показана ефективність монтелукасту як при еозинофільному езофагіті [35], так і при еозинофільному ентероколіті [33, 36]. Іншим агентом, що активно вивчається, є антиінтерлейкін-5 — препарат меполізумаб (mepolizumab) [35]. При проведенні відкритого клінічного випробування антиінтерлейкіну-5 у пацієнтів з ЕЕ показана істотна позитивна динаміка. На фоні прийому препарату меполізумаб відзначається зменшення периферичної та тканинної еозинофілії, зникають клінічна симптоматика й морфологічні зміни в стравоході. Подібні дослідження проводяться і при еозинофільному гастроентериті [14].
Симптоматична терапія з урахуванням локалізації ураження полягає в застосуванні при гастроезофагеальному рефлюксі прокінетиків, антацидів і антисекреторних препаратів, при гастродуоденіті — антацидів і антисекреторних препаратів. За показаннями проводиться антихелікобактерна терапія [1, 16, 28].
Абсолютним показанням до призначення замісної ферментотерапії при харчовій алергії є вторинна панкреатична недостатність. Замісна ферментотерапія може використовуватися в комплексній терапії уражень тонкого і товстого кишечника. Перевагу віддають ферментним препаратам, отриманим з підшлункової залози свиней. При алергії до білків коров''ячого молока ферментні препарати з підшлункової залози великої рогатої худоби протипоказані через можливу перехресну алергію [1, 16, 28].
З метою відновлення нормального мікробіоценозу кишечника застосовуються лікарські засоби п''яти основних груп: біфідовмісні препарати; препарати лактобактерій; колівмісні засоби; препарати, що містять культури бактерій з антагоністичною активністю; комплекси пробіотиків і їх метаболітів [7, 24–26]. Необхідно пам''ятати, що лікарські засоби, що містять домішки середовища культивування, можуть викликати у дітей з гастроінтестинальними проявами харчової алергії загострення патологічного процесу, а препарати, до складу яких як наповнювач входить лактоза, можуть погіршувати симптоми вторинної лактазної недостатності. У зв''язку з цим перевага віддається лікарським засобам, які позбавлені вищеназваних домішок.
Отже, різноманіття гастроінтестинальних проявів харчової алергії в дітей можливе на будь-якому рівні: у порожнині рота, стравоході, шлунку, тонкому й товстому кишечнику, спостерігається у багатьох дітей поєднане ураження різних відділів травного каналу. Залежно від віку дитини змінюється спектр харчових алергенів, відповідальних за розвиток гастроінтестинальних проявів алергії. Коров''яче молоко є одним із найчастіших алергенів у дітей грудного і раннього віку. Лікування гастроінтестинальних проявів харчової алергії повинне бути комплексним: елімінація причинного харчового продукту, застосування антимедіаторних, протизапальних, пробіотичних, ферментних препаратів.
1. Клинические рекомендации. Аллергология / Под ред. Р.М. Хаитова, Н.И. Ильиной. — М.: ГЭОТАР-Медиа, 2006.
2. Sicherer S.H. // Pediatrics. — 2003. — Vol. 111, № 6. — P. 1609-1616.
3. Пампура А.Н., Хавкин А.И. Классификация и клинические проявления пищевой аллергии // РМЖ. — 2003. — Т. 11, № 20. — С. 1126-1130.
4. Sampson H.A. Food allergy: I. Immunopathogenesis and clinical disorders // J. Allergy Clin. Immunol. — 1999. — 103. — 717-728.
5. Ревякина В.А. Пищевая аллергия и аллергические заболевания // Доктор.Ру. — 2003. — № 12.
6. Аллергические реакции пищевода. http://www.esophagealcancer.ru/allergiya/allergicheskie_re.html
7. Пампура А.Н. Пищевая аллергия у детей. — М., 2007.
8. Ревякина В.А. // Вестник педиатр., фармакол. и нутрициол. — 2007. — № 5. — С. 7-11.
9. Шумилов П.В., Дубровская М.И., Юдина О.В. и др. // Вопросы соврем. Педиатрии. — 2007. — № 4. — С. 44-53.
10. Iacono G., Carroccio A., Cavataio F.: Gastroesophageal reflux and cow''s milk allergy in infants: A prospective study // J. Allergy Clin. Immunol. — 1996. — 97. — 822-827.
11. Шумилов П.В., Дубровская М.И., Юдина О.В. и др. Поражения желудочно-кишечного тракта у детей с пищевой аллергией // Трудный пациент. — 2007. — № 10. — С. 67-75.
12. Straumann A., Simon H. Eosinophilic esophagitis: escalating epidemiology? // J. Allergy Clin. Immunol. — 2005. — Vol. 115. — Р. 418-419.
13. Richter J. The refractory GERD patient // World Gastroenterol. News. — 2007. — Vol. 12. — Р. 11-13.
14. Attwood S., Lewis C., Bronder C. et al. Eosinophilic esophagitis: a novel treatment using Montelukast // Gut. — 2003. — Vol. 52. — Р. 181-185.
15. Matysiak-Budnik T., Heyman M. // J. Ped. Gastroenterology and Nutrition. — 2002. — Vol. 34, № 1. — P. 5-12.
16. Ревякина В.А. Общие принципы диагностики и лечения пищевой аллергии // Рус. мед. журн. — 2000. — № 8. — С. 739-745.
17. Tan A.C., Kruimel J.W., Naber T.H. Eosinophilic gastroenteritis treated with non-enteric coated budesonide tablets // Eur. J. Gastroenterol. Hepatol. — 2001. — Vol. 13. — Р. 425-427.
18. Moon A., Kleinman R. Allergic gastroenteropathy in children // Ann. Allergy Asthma Immunol. — 1995. — 74. — 5-9.
19. Sicherer S. Food protein-induced enterocolitis syndrome: Clinical perspectives // J. Pediatr. Gastroenterol. Nutr. — 2000. — 30 (suppl). — 45-49.
20. Ojuawo A., St Louis D., Lindley K.J., Milla P.J. Non-infective colitis in infancy: evidence in favour of minor immunodeficiency in its pathogenesis // Arch. Dis. Child. — 1997 Apr. — 76 (4). — 345-8.
21. Poon E., Nixon R. Cutaneous spectrum of coeliac disease // Aust. J. Dermatol. — 2001. — 42. — 136-138.
22. Collin P., Kaukinen K., Maki M.: Clinical features of celiac disease today // Dig. Dis. Sci. — 1999. — 17. — 100-106.
23. Ардатская М.Д., Минушкин О.Н. // Рус. мед. журнал. — 2006. — № 1. — C. 65-70.
24. Бельмер С.В., Малкович А.В. // Лечащий врач. — 2006. — № 6. — С. 18-23.
25. Урсова Н.И. Дисбактериозы кишечника у детей: Руководство для практикующих врачей / Под ред. Г.В. Римарчук. — М.: ООО «Компания БОРГЕС», 2006.
26. Корниенко Е.А. Актуальные проблемы коррекции кишечной микрофлоры у детей: Учеб. пособие. — М.: ГОУ ВУНМЦ МЗ и СР РФ, 2006.
27. Bindslev-Jensen C., Ballmer-Weber B.K., Bengtsson U. et al. // Allergy. — 2004. — Vol. 59. — P. 690-697.
28. Жерносек В.Ф., Дюбкова Т.П. Современные подходы к диагностике и лечению гастроинтестинальных проявлений пищевой аллергии у детей // Медицинские новости. — 2008. — № 6. — С. 33-40.
29. Жерносек В.Ф., Дюбкова Т.П. Пищевая аллергия у детей первого года жизни: Учеб.-метод. пособ. — 2-е изд., перераб. и доп. — Минск: Эдит ВВ, 2007.
30. Sampson H.A. // Allergy. — 2005. — Vol. 60 (Suppl. 79). — P. 19-24.
31. Hypoallergenic infants formulas / Committee on Nutrition AAP // Pediatrics. — 2000. — Vol. 106, № 2. — P. 346-349.
32. Zeiger R.S. // Pediatrics. — 2003. — Vol. 111, № 6. — P. 1662-1671.
33. Coplementary feeding: a commentary by the ESPGHAN Committee on Nutrition // J. Ped. Gastroenterology and Nutrition. — 2008. — Vol. 46, № 1. — P. 99-110.
34. Neustrom M.R., Friesen C. Treatment of eosinophilic gastroenteritis with montelukast // J. Allergy Clin. Immunol. — 1999. — Vol. 104. — Р. 506.
35. Garrett J., Jameson S., Thomson B. et al. Anti-interleukin-5 (mepolizumab) therapy for hypereosinophilic syndromes// J. Allergy Clin. Immunol. — 2004. — Vol. 113. — P. 115-119.
36. Eigenman P.A. // Ped. Allergy and Immunol. — 2007. — Vol. 18. — P. 265-271.
37. Hypoallergenic infants formulas / Committee on Nutrition AAP // Pediatrics. — 2000. — Vol. 106, № 2. — P. 346-349.
38. Sampson H. Diagnosing food allergy // Provocation Testing in Clinical Practice / Ed. by Spector S. — NewYork: MarcelDekker, 1995. — Р. 623.
39. Sampson H.A., Mendelson L.M., Rosen J.P. Fatal and near-fatal anaphylactic reactions to food in children and adolescents // N. Engl. J. Med. — 1992. — 327. — 380-384.
40. Suzuki J., Kawasaki Y., Nozawa R. et al. Oral disodium cromoglycate and ketotifen for a patient with eosinophilic gastroenteritis, food allergy and protein-losing enteropathy // Asian Pac. J. Allergy Immunol. — 2003. — Vol. 21. — Р. 193-197.