Газета «Новости медицины и фармации» Кардиология (327) 2010 (тематический номер)
Вернуться к номеру
Как улучшить прогноз больных ИБС после реваскуляризации миокарда?
Авторы: В.А. Бобров, И.В. Давыдова, А.И. Макаревский, Кафедра кардиологии и функциональной диагностики НМАПО им. П.Л. Шупика, г. Киев
Версия для печати

Основными целями лечения больных со стабильной стенокардией, согласно рекомендациям Европейского кардиологического общества, являются улучшение прогноза пациента путем предупреждения развития инфаркта миокарда (ИМ) и внезапной смерти, а также минимизация или устранение клинических проявлений заболевания [21].
В клинической практике для этого сочетают меры немедикаментозного воздействия, направленные на коррекцию имеющихся факторов риска, медикаментозное лечение и методы интервенционной кардиологии (баллонная ангиопластика, стентирование) и коронарной хирургии (шунтирование, трансмиокардиальная лазерная реваскуляризация).
В последние годы реваскуляризация миокарда как метод хирургического лечения ишемической болезни сердца (ИБС) получила широкое распространение.
Выбор конкретного метода реваскуляризации основывается на таких факторах, как риск развития осложнений и смерти после вмешательства, вероятность успеха, включая техническую возможность выполнения ангиопластики или шунтирования, риск рестеноза или окклюзии шунта, полнота реваскуляризации, наличие сахарного диабета, опыт лечебного учреждения и желание пациента.
Основное преимущество методов интервенционной кардиологии очевидно — более эффективное уменьшение симптомов ишемии миокарда, но (!) по данным G.W. Vetrovec и соавторов, в течение 6 месяцев после коронарной ангиопластики у 90 % больных был хотя бы один приступ стенокардии в неделю, а у 30 % пациентов — несколько приступов в неделю [43]. Действительно, в реальной практике выполнение реваскуляризации миокарда не становится автоматически гарантией полного устранения стенокардии, а также не исключает возможности возобновления приступов после первоначально успешной реваскуляризации миокарда, что отмечается не так редко и может увеличивать смертность и частоту развития осложнений у таких больных.
Каковы причины возобновления приступов стенокардии после реваскуляризации миокарда?
В случае возобновления симптоматики у реваскуляризированных больных отмечаются типичные приступы стенокардии, причем во время выполнения нагрузочной пробы признаки ишемии миокарда могут как обнаруживаться, так и отсутствовать. Основными причинами возобновления стенокардии после чрескожного вмешательства на коронарных артериях могут быть как структурные, так и функциональные изменения коронарных артерий.
Структурные изменения включают: развитие рестеноза в стентированном участке артерии, прогрессирование атеросклеротического поражения коронарных артерий или неполную реваскуляризацию. Ранняя непроходимость шунта обычно бывает следствием осложнений, связанных с вмешательством, и отмечается примерно в 15 % случаев. Поздняя несостоятельность шунтов обычно обусловлена дегенеративными изменениями в тканях шунтов.
К функциональным причинам относят: дисфункцию микрососудистого коронарного русла, спазм эпикардиальных артерий и спазм коронарной артерии в участке, примыкающем к стенту. Но функциональные причины рецидива стенокардии после реваскуляризации установить значительно труднее [27, 37].
«Подводные камни»
В 1977 г . B. Bulkely и G. Hutchins, изучив состояние миокарда у 58 больных, подвергнутых коронарному шунтированию (все пациенты погибли в сроки не позднее чем через 1 месяц после оперативного вмешательства), впервые сообщили о «парадоксе повреждения миокарда», имевшем место, несмотря на успешное выполнение реваскуляризации миокарда [11]. Этот парадокс получил название «ишемическое реперфузионное повреждение», в возникновении и прогрессировании которого важную роль играет образование реактивных радикалов кислорода в ответ на реперфузию ишемизированного миокарда, приводящее к перегрузке кардиомиоцитов кальцием и в итоге вызывающее повреждение и гибель клеток сердца. Установлено, что в формирование ишемического реперфузионного повреждения включаются агрегация и активация лейкоцитов, агрегация тромбоцитов, активация апоптоза, кардиотоксический эффект ангиотензина II и активация системы комплемента [3–5]. Указанные нарушения проявляются феноменом невосстановления кровотока (no-reflow phenomenon), микроваскулярной и эндотелиальной дисфункцией, «оглушением» миокарда, реперфузионными аритмиями и необратимым реперфузионным повреждением миокарда.
Реперфузионные осложнения, возникающие при проведении хирургических вмешательств на коронарных сосудах при тяжелой ИБС, по-прежнему серьезно ухудшают прогноз этого наиболее современного и перспективного вида лечения.
Функциональное восстановление миокарда после операции не происходит сразу же. Известно, что в начальный период восстановления коронарного кровотока после длительного существования тяжелой ишемии миокарда могут возникать повреждения коронарных сосудов, серьезные аритмии, новые очаги некроза сердечной мышцы, состояние «оглушенности» миокарда и синдром постишемической сократительной дисфункции с низким сердечным выбросом. Эти осложнения носят название «реперфузионный синдром» [9]. Период послеоперационного снижения сократительной способности миокарда сохраняется у многих больных в течение нескольких часов и даже дней после восстановления коронарного кровотока.
Можно ли противостоять гибели кардиомиоцитов, возникающей во время восстановления коронарного кровотока?
Предотвращение поражения миокарда во время процедур реваскуляризации (ангиопластика, стентирование, аортокоронарное шунтирование) — крайне важная задача, решение которой будет способствовать более благоприятному прогнозу у больных с ИБС. Обратимся к возможностям терапии, корригирующей метаболические нарушения в миокарде. Речь идет об оригинальном триметазидине модифицированного высвобождения (Предуктал МR ® , «Сервье»).
Поскольку Предуктал МR ® влияет непосредственно на метаболизм миокарда, обеспечивая оптимальный синтез энергии в условиях ишемии-реперфузии, он является патогенетическим лечением ИБС. Как известно, механизм действия триметазидина связан с подавлением метаболизма жирных кислот, сопровождающегося стимуляцией метаболизма глюкозы [6]. Именно восстановление регуляции между двумя основными путями обмена энергетических субстратов в миокарде в условиях ишемии обеспечивает уменьшение внутриклеточного ацидоза и избыточного содержания ионов кальция, а также предупреждение накопления жирных кислот и их недоокисленных продуктов в цитоплазме кардиомиоцитов. Это действие становится особенно полезным и во время реперфузии, когда вследствие восстановления притока окисленной крови в прежде ишемизированные участки миокарда стремительно нарастает процесс окисления жирных кислот и парадоксально уменьшается процесс окисления пирувата, образовавшегося из глюкозы или лактата. В экспериментальных исследованиях показано, что оригинальный триметазидин в условиях ишемии-реперфузии препятствует резкому увеличению проницаемости митохондрий, снижает активацию нейтрофилов, а также уменьшает выраженность апоптоза кардиомиоцитов [7–10].
Таким образом, Предуктал МR ® , эффект которого связан с непосредственным влиянием на кардиомиоциты, способствует их выживаемости в условиях ишемии-реперфузии.
Итак, исходя из понимания механизмов развития повреждения миокарда, связанного с реперфузией, назначение Предуктала МR ® перед процедурой реваскуляризации миокарда играет важную роль в защите миокарда от повреждений вследствие ишемии-реперфузии.
Имеет ли эта концепция подтверждение в рандомизированных клинических исследованиях?
Проведенные исследования и доказательства были получены только с оригинальным триметазидином и триметазидином MR (Предуктал МR ® , «Сервье»). Это принципиально важное замечание, так как попытки получить доказательства терапевтической эквивалентности оригинальной и генерической форм препарата пока не дали положительного результата [22].
Еще в 1995 г . Fabiani и соавт. показали, что у лиц, получавших 60 мг оригинального триметазидина в течение 3 нед. до проведения аортокоронарного шунтирования, наблюдалось снижение уровня повреждения кардиомиоцитов во время ишемии-реперфузии под воздействием препарата, что свидетельствует о его специфическом защитном эффекте [19, 20, 23].
В открытом контролируемом рандомизированном клиническом исследовании (РКИ) L. Polonski и соавт., включившем 44 пациента с однососудистым поражением, Предуктал МR ® назначался по крайней мере за 4 дня до выполнения транслюминальной баллонной коронарной ангиопластики (ТБКА). Авторы установили, что применение оригинального триметазидина обеспечивает достоверно меньшую элевацию сегмента ST при проведении ТБКА. Кроме того, у пациентов, получавших Предуктал МR ® , отмечено достоверное увеличение времени от раздувания баллона до появления стенокардии и, соответственно, уменьшение времени от сдувания баллона до исчезновения боли [32].

В самое крупное РКИ, посвященное изучению протективных эффектов оригинального триметазидина в отношении повреждения миокарда после ТБКА, L. Bonello и соавт. включили 266 больных со стабильной стенокардией и однососудистым поражением коронарных артерий. Установлено, что по сравнению с контрольной группой однократный прием Предуктала МR ® перед выполнением ТБКА обеспечивает достоверное снижение уровня тропонина I во все сроки после чрескожного коронарного вмешательства [10].
К заключению о защитном воздействии оригинального триметазидина пришли в 2000 г . Тunerir и соавт., обнаружившие снижение реперфузионных повреждений миокарда у 30 больных, получавших Предуктал МR ® до проведения им аортокоронарного шунтирования [12].
В 2001 г . в исследовании LIST (Limitation of Infarct Size with Trimetazidine) проф . Р.G. Steg и соавт. [38] изучили результаты внутривенной инфузии оригинального триметазидина до пероральной терапии препаратом после проведения чрескожной транслюминальной коронарной ангиопластики у 94 больных с острым инфарктом миокарда. Это было рандомизированное двойное слепое плацебо-контролируемое многоцентровое исследование. В качестве группы сравнения ученые использовали 50 больных, подвергшихся подобному вмешательству без применения триметазидина. По данным исследователей, у лиц, получавших оригинальный триметазидин, уменьшение ишемии миокарда протекало более интенсивно, и реперфузионный синдром был менее выражен, чем у больных контрольной группы.
Основной вывод, который можно сделать по результатам РКИ, в которых Предуктал МR ® назначался больным ИБС перед выполнением процедур по реваскуляризации миокарда, заключается в том, что применение препарата значительно уменьшает повреждение миокарда, вызванное этими вмешательствами.
Нужна ли противоишемическая терапия после выполнения реваскуляризации миокарда?
Да, поскольку даже после реваскуляризации у пациента может наблюдаться прогрессирование ИБС. Причиной тому служит атеросклеротическое поражение и/или рестеноз подвергшихся эндоваскулярному вмешательству сосудов.
Тактика ведения пациентов в подобной клинической ситуации предусматривает воздействие на все звенья патогенеза и прогрессирования ИБС: антитромбоцитарные препараты, статины, ингибиторы ангиотензинпревращающего фермента, антиишемические средства, в том числе Предуктал МR ® .
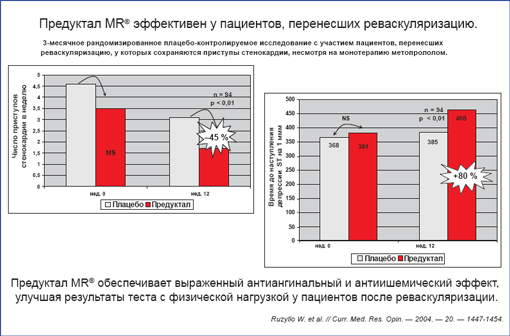
Доказательством эффективности данного подхода является вторичный анализ данных 3-месячного рандомизированного плацебо-контролируемого исследования TRIMPOL II с участием пациентов, перенесших реваскуляризацию, у которых сохраняются приступы стенокардии, несмотря на монотерапию метопрололом. Назначение оригинального триметазидина обеспечило выраженный антиангинальный и антиишемический эффект, улучшая результаты теста с физической нагрузкой по сравнению с монотерапией бета-блокатором [41].
Интересные данные были получены A. Labrou и соавт. при оценке влияния терапии с Предукталом МR ® на повреждения миокарда, связанные с процедурой чрескожного вмешательства на коронарных артериях, а также на функцию сердца через 1–3 месяца после процедуры. Согласно дизайну этого исследования, пациенты начинали прием Предуктала МR ® дополнительно к традиционной терапии за 15 дней до процедуры и продолжали его все 3 месяца наблюдения. У пациентов контролировали уровень тропонина I, МВ-КФК как маркеры повреждения миокарда, а также параметры ЭхоКГ для оценки сократительной функции сердца. Терапия с Предукталом МR ® позволила не только минимизировать повреждения миокарда, связанные с самой процедурой реваскуляризации [25], но и получить достоверное улучшение как региональной сократимости, так и функции сердца в целом у реваскуляризированных коронарных пациентов при наблюдении в течение длительного времени после процедуры.
Итак, нужна ли противоишемическая терапия после выполнения реваскуляризации миокарда? Ответ: несомненно, да, особенно если у пациента с ИБС после проведения реваскуляризации миокарда сохраняются приступы стенокардии или имеет место систолическая дисфункция левого желудочка.
Нужна ли противоишемическая терапия при бессимптомной ишемии миокарда?
Безболевая ишемия миокарда, как и болевая ее форма, может приводить к тяжелым последствиям — внезапной смерти, инфаркту миокарда, тяжелым нарушениям функции сердца и сердечной недостаточности. Имеются данные о прогностической значимости бессимптомной ишемии миокарда у больных, перенесших коронарное шунтирование или чрескожное вмешательство на коронарных артериях, а также у больных ИБС и сопутствующим сахарным диабетом. Известно, что пациенты с сочетанием ИБС и сахарного диабета — это пациенты высокого риска, нуждающиеся в наиболее тщательном подборе терапии [3].
G. Rosano и соавт. изучили путем ЭКГ-мониторинга влияние терапии с Предукталом МR ® и без него на частоту возникновения немой ишемии миокарда у пациентов с ИБС и диабетом. Было показано, что включение Предуктала МR ® ведет к достоверному уменьшению как числа, так и общей длительности безболевой ишемии миокарда, обеспечивая надежную защиту кардиомиоцита от ишемии на протяжении суток [35].
И еще один вопрос, который всегда волнует врача: когда пациенту назначить Предуктал МR ® и как долго его принимать? Ответ на этот вопрос был получен в недавно закончившемся исследовании METRO (Management of angina: a retrospective cohort). Авторы изучили независимые эффекты применения антиангинальной терапии на риск развития смерти пациентов со стабильной стенокардией, которые на фоне проводимой терапии перенесли инфаркт миокарда. Полученные результаты свидетельствовали о том, что выживаемость больных после ИМ зависит от предыдущего лечения стабильной стенокардии. У пациентов, принимавших в составе антиангинальной терапии до развития ИМ Предуктал МR ® , риск смерти на протяжении 6 мес. был достоверно ниже (на 64 %), тогда как использование только традиционных антиангинальных препаратов не обеспечивает подобного результата [24].
Антиангинальный эффект препаратов, которые рекомендованы для лечения ИБС, сохраняется в течение того времени, пока больной принимает препарат. Тот же эффект присущ и Предукталу МR ® . Поэтому для достижения стабильного антиишемического эффекта и устойчивого улучшения контроля приступов стенокардии оправданным является длительное применение препарата, в том числе в период после реваскуляризации.
Итак, в настоящее время аортокоронарное шунтирование и коронарная ангиопластика становятся более доступными для больных ИБС, поэтому оптимизация медикаментозного лечения такой категории пациентов является актуальной задачей. Ишемия миокарда, возникающая во время проведения баллонной ангиопластики и стентирования коронарных артерий, не только приводит к ухудшению качества жизни, но может считаться фактором риска развития неблагоприятных клинических исходов, связанных с ИБС. Поэтому роль противоишемической терапии в лечении такого контингента больных может иметь большее значение для улучшения прогноза больных, чем считалось ранее. Традиционные подходы к лечению пациентов с ишемической болезнью сердца (блокаторы b -адренорецепторов, антагонисты кальция, нитраты) и применение Предуктала МR ® позволяет обеспечить оптимальную антиишемическую эффективность проводимой терапии. Кроме того, Предуктал МR ® должен быть назначен как можно раньше перед планируемой процедурой реваскуляризации и длительно после нее для ограничения реперфузионного повреждения, что проявляется в меньшей частоте осложнений в послеоперационном периоде. Такое благоприятное влияние на энергетический метаболизм сердца не только обеспечивает эффективную протекцию от повреждения при ишемии-реперфузии, повышение толерантности к физической нагрузке и улучшение систолической функции левого желудочка, но и приводит к меньшим затратам при лечении данной категории больных.
Список литературы находится в редакции
