Газета «Новости медицины и фармации» 20 (346) 2010
Вернуться к номеру
Послеродовой мастит и лактостаз: тактика ведения
Авторы: С.А. Ласачко, О.Н. Долгошапко, Донецкий региональный центр охраны материнства и детства
Версия для печати
 Мастит — воспаление паренхимы и интерстициальной ткани молочной железы (МЖ). Мастит следует отличать от других воспалительных заболеваний кожи, подкожной клетчатки МЖ (фурункул, карбункул, абсцесс, флегмона, рожистое воспаление), объединяемых понятием парамастита.
Мастит — воспаление паренхимы и интерстициальной ткани молочной железы (МЖ). Мастит следует отличать от других воспалительных заболеваний кожи, подкожной клетчатки МЖ (фурункул, карбункул, абсцесс, флегмона, рожистое воспаление), объединяемых понятием парамастита.
Острые маститы в основном (82– 87 % случаев) встречаются в послеродовом периоде у кормящих женщин. Несмотря на значительные успехи профилактической медицины в борьбе с неспецифической хирургической инфекцией, лактационный мастит (ЛМ) продолжает занимать видное место как в гнойной хирургии, так и в практике акушера-гинеколога.
Проблема лактационных маститов в некоторой мере является скрытой, так как данные о частоте этого заболевания значительно расходятся в различных источниках. В официальной статистике проблема практически отсутствует как таковая: например, по всей Украине за 2004 год в акушерских стационарах зарегистрировано всего 3 случая гнойного мастита. По данным специальной хирургической литературы, лактационные маститы составляют 77–99 % случаев неспецифического мастита, а все формы ЛМ — от серозной до деструктивных — имеют место у 2 % женщин за период беременности и кормления грудью. Чаще официально регистрируются гнойные формы маститов, требующие специального хирургического лечения. Инфильтративный и серозный мастит, который в большинстве случаев успешно лечится консервативно, зачастую даже не регистрируется. По данным Оскреткова (2001), острый ЛМ в 84 % случаев возникает у пациенток в возрасте 17–30 лет, причем 80 % из них — первородящие.
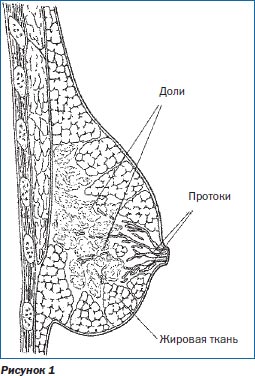
При диагностике и выборе лечения при мастите необходимо учитывать анатомию молочной железы (рис. 1). Форма, размер, положение МЖ широко варьируют в пределах физиологической нормы и зависят от возраста женщины, фазы менструального цикла, телосложения, состояния репродуктивного здоровья, изменяются во время беременности и лактации. МЖ имеют дольчатое строение: доли, разделенные междольковыми соединительнотканными промежутками, состоят из 20–40 долек, каждая из которых, в свою очередь, состоит из нескольких десятков альвеол; пузырек альвеолы выстлан однослойным железистым эпителием и имеет выводной проток. Выводные протоки альвеол, соединяясь в более крупные, долевые, протоки, открываются на вершине соска. Приблизительно в области границы ареолы протоки имеют расширения (млечные синусы). Кроме того, как в подкожной жировой клетчатке, так и вокруг железистой ткани располагается жировая ткань, количество которой в МЖ индивидуально и в большой степени наряду с развитием железистых долек определяет размер и форму МЖ. Соединительнотканные тяжи, поддерживающие МЖ (связки Купера), являются продолжением междольковых перегородок. Они проходят от передней поверхности МЖ к поверхностной фасции, глубоким слоям кожи и ключице.
Основные регионарные группы лимфатических узлов (ЛУ): аксиллярные, подключичные, окологрудные (по ходу внутренней грудной артерии), грудные (между большой и малой грудными мышцами), надключичные. Возможен также отток лимфы в противоположную МЖ, к ЛУ верхнего отдела влагалища прямой мышцы живота, к диафрагмальным ЛУ, поверхностным парастернальным и поддиафрагмальным ЛУ.
Физиология лактации. Основная физиологическая функция МЖ — синтез и выделение молока для кормления ребенка. Со второго триместра беременности начинается секреция молозива, представляющего собой мутноватую жидкость, богатую белками и бедную жирами. В нем отмечается наличие клеток, называемых тельцами Донне. По своему составу молозиво больше походит на сыворотку, чем на молоко. Продолжительность лактации у женщины колеблется в норме от пяти до двадцати четырех месяцев, а продуцируемое количество молока колеблется от 600 до 1300 мл в сутки. Максимальная секреция молока достигается к 6–12-му дням послеродового периода, затем отмечается период стабилизации, в течение которого количество выделяемого молока может обеспечить адекватное питание новорожденного в первые 3–6 месяцев послеродового периода.
Процесс подготовки МЖ к выработке молока называется лактогенезом, а процесс поддержания лактации у кормящей женщины — лактопоэзом. Процесс лактопоэза поддерживается во время кормления грудью посредством нейрогормональных рефлексов, приводимых в действие сосанием. Рефлекторная дуга начинается в чувствительных рецепторах сосков и ареол, откуда по спинномозговым путям сигнал поступает в гипоталамус. В гипоталамусе индуцируется продукция октапептидов (в основном окситоцина) и адено- и внегипофизарных гормонов, которые поддерживают лактацию. Выделение молока — процесс, обусловленный описанным выше нейроэндокринным рефлексом, в рамках которого ведущая роль принадлежит окситоцину и вазопрессину.
Эпидемиология маститов
Исторически послеродовой, или лактационный, мастит был разделен на эпидемиологические и спорадические формы. В более ранней литературе мастит характеризовался как острый грудной aденит, в котором первичное инфицирование происходит в лактационных протоках. В этом случае возможно получение гнойного материала из протоков. Иногда несмежные доли в той же самой груди или доли в обеих МЖ инфицируются одновременно. Этот тип инфекции является эпидемическим и связан со стафилококковыми вспышками новорожденных.
Спорадический послеродовой мастит характеризовался как острый грудной целлюлит. Эта инфекция отличается интенсивным воспалением междолевой соединительной ткани. Получение гноя из протоков обычно невозможно. Входными воротами для бактерий, как предполагалось, являются трещины сосков. Эта форма мастита — наиболее частая, с которой мы сталкиваемся сегодня.
Мастит развивается у 2–5 % лактирующих женщин. Точно определить причину мастита трудно по двум причинам. Во-первых, данные о частоте мастита различные у разных исследователей. Частота, кажется, недооценена, потому что 50 % женщин с очевидной грудной инфекцией не обращаются за медицинской помощью. По данным маммологического кабинета ДРЦОМД зарегистрировано (по обращаемости): 2007 г. — 40 случаев лактационного мастита; 2008 г. — 143 случая.
Во-вторых, некоторые авторы в пределы этого определения включают застой молока и другие неинфекционные состояния, чего другие не делают. Согласно Х Международной классификации болезней, различают следующие нарушения лактации (О91–92):
О91 — лактационный мастит;
О92.1 — трещина соска;
О92.2 — другие и неуточенные нарушения;
О92.3 — агалактия первичная;
О92.4 — гипогалактия;
О92.5 — агалактия вторичная и по медпоказаниям;
О92.6 — галакторея послеродовая;
О92.7 — лактостаз, полигалактия и др.
Хотя острый мастит может развиться в любое время в течение кормления грудью, но в основном это происходит в течение первого месяца постнатального периода. Средний интервал между заболеванием и инфицированием, согласно данным литературы — 5,5 недели, с диапазоном от 5 дней до 1 года. Большинство исследователей указывают на пик проявления инфекции во время 2–3-й недели постнатального периода.
Острый мастит — это прежде всего болезнь постнатального периода, но может происходить и в aнтенатальном периоде. Это объясняется значительными анатомическими и физиологическими изменениями, происходящими в МЖ во время беременности, описанными выше, и началом секреции молозива уже в этот период. Основным условием развития мастита, безусловно, является инфицирование. Клинически мастит беременных отличается от лактационного не столь быстрым развитием и отсутствием зависимости от регулярного опорожнения МЖ.
Многие факторы рассматриваются как предрасполагающие к маститу, но только два из них, по нашему мнению, являются ведущими: застой молока и инфекция. Thomsen и другие изучили причины лактостаза и неинфекционные воспалительные заболевания МЖ и пришли к выводу о необходимости продолжения грудного вскармливания при лактостазе и начальных стадиях мастита. Неинфекционный мастит прогрессировал в инфекционный или абсцесс только в 4 % случаев, если регулярное опорожнение МЖ продолжалось. Прогрессия в инфекционный мастит была замечена в 79 % случаев при отказе от грудного вскармливания. Возможно, этот эффект предрасположенности к лактостазу объясняет высокую заболеваемость маститом в первые недели после родов, когда отток молока особенно затруднен.
Источником инфекции при маститах являются бациллоносители, больные со стертыми формами гнойно-воспалительных заболеваний, резервуаром инфекции служат воздух лечебных учреждений, предметы ухода, белье, верхние дыхательные пути обслуживающего персонала. Следует отметить, что прогноз при внутрибольничном заражении тяжелее, чем при внебольничном, что связано с повышенной резистентностью и вирулентностью больничных штаммов стафилококков.
Схема эпидемической цепи внутрибольничной инфекции в родильных стационарах следующая: источник инфекции — пути передачи — восприимчивый организм. Предлагаемая схема распространения внутрибольничной инфекции, инфицирования МЖ родильниц и развития мастита довольно четко и убедительно с учетом количественных характеристик демонстрирует роль госпитальной инфекции в развитии мастита.
Интересные и очень важные с эпидемиологической точки зрения данные приводит Л.Н. Гранат еще в 1977 году. Методом фаготипирования доказано различие штаммов стафилококков, вызывающих послеродовые воспалительные заболевания и мастит. Но при сравнительном бактериологическом анализе возбудителей гнойничковых заболеваний новорожденных (пиодермия, конъюнктивит) и мастита родильниц выявлена полная идентичность штаммов стафилококков — основных возбудителей неспецифических воспалительных заболеваний новорожденных и родильниц. Обнаружена идентичность стафилококков, высеянных из полости рта, носа новорожденных и выделенных из сосков матери. При этом установлено увеличение степени бактериальной обсемененности сосков после кормления. Сроки внутрибольничного инфицирования новорожденных и возникновения мастита различны. Данный факт также говорит о том, что непосредственным источником инфекции при мастите является новорожденный, который может быть как бациллоносителем, так и больным с теми или иными воспалительными заболеваниями полости рта, зева, носоглотки.
Входными воротами для микроорганизмов служат чаще всего трещины сосков, возможно и интраканаликулярное проникновение инфекции при кормлении грудью или сцеживании молока, реже — распространение инфекции гематогенным и лимфогенным путями из эндогенных очагов инфекции. От 25 до 31 % всех маститов развиваются при наличии трещин сосков. Число случаев обнаружения трещин сосков у кормящих составляет 23–65 %, тогда как мастит у родильниц возникает в 3–6 % случаев. Тем не менее профилактика трещин сосков у родильниц служит одновременно профилактикой ЛМ.
Чрезвычайно важным фактором в возникновении ЛМ, как уже говорилось выше, является застой молока с инфицированием его патогенными микроорганизмами. При застое увеличивается число бактерий в молоке и молочных ходах. Свернувшееся молоко подвергается молочнокислому брожению, что приводит к разрушению эпителия, выстилающего молочные ходы и альвеолы. При повышении давления в МЖ в ней нарушается кровообращение, возникает венозный застой. С развитием отека межуточной ткани понижается ее устойчивость к патогенным микроорганизмам, что создает хорошие условия для развития инфекции.
Снижение устойчивости тканей к инфекции в силу указанных выше причин и снижения общей сопротивляемости организма женщины, ослабленной родами, авитаминозами, сопутствующими воспалительными заболеваниями, создают благоприятные условия для развития мастита.
Микробиология
Основной микроорганизм, вызывающий послеродовой мастит, — это Staphylococcus aureus. Эта бактерия может быть обнаружена у приблизительно 70 % женщин с маститом. Следующий наиболее часто встречаемый инфекционный агент — Staphylococcus epidermidis, который можно высеять приблизительно в 25 % случаев. Большинство этих инфекций устойчивы к пенициллину.
Менее часто встречаемые — beta-hemolytic streptococci, Enterococcus faecalis, Escherichia coli, Klebsiella pneumoniae, Pseudomonas picetti, Bacteroides, mycobacteria, Actinomyces. Анаэробы определяются более часто у пациенток с гнойным процессом. Однако даже в этой ситуации staphylococci преобладает.
Новорожденный обсеменяется staphylococci сразу после рождения в результате близкого контакта с матерью или взаимным загрязнением в помещениях послеродового отделения. Некоторые исследователи демонстрировали инфицирование стафилококком новорожденных персоналом детского отделения.
Хирургическая классификация маститов:
I. По причине заболевания:
1. Неспецифический.
2. Специфический.
II. По функциональному состоянию МЖ:
1. Лактационный.
2. Нелактационный.
III. По течению воспалительного процесса:
1. Острый.
2. Хронический.
IV. По распространенности процесса:
1. Ограниченный.
2. Диффузный.
V. По характеру воспаления:
1. Серозный.
2. Инфильтративный.
3. Гнойный:
а) абсцедирующий;
б) инфильтративно-абсцедирующий;
в) флегмонозный;
г) гнойно-некротический.
4. Гангренозный.
VI. По локализации и глубине поражения:
1. Поверхностный:
а) подкожный;
б) субареолярный.
2. Глубокий:
а) интрамаммарный;
б) ретромаммарный.
Клиника, диагностика
Диагноз мастита, казалось бы, не представляет затруднений. Но это касается процесса как такового, а лечебная тактика при различных фазах течения воспалительного процесса строго дифференцирована. Своевременная диагностика ранних форм мастита и своевременно начатое лечение позволяют в большинстве случаев добиться обратного развития процесса, предупреждают его переход в гнойную, деструктивную фазу.
Маститы классифицируют по патологоанатомическим и клиническим признакам. Патологоанатомическая классификация предусматривает выделение галактофорита, паренхиматозного и интерстициального мастита. Две последние формы, встречающиеся только в комбинации друг с другом, разграничить на основании клинических данных не представляется возможным.
Острый воспалительный процесс в МЖ необходимо отличать от острого застоя молока. Причинами последнего являются аномальное строение соска, неправильное прикладывание ребенка, недостаточное развитие молочных протоков у первородящих женщин. При остром застое молока опухолевидное образование соответствует контурам долек МЖ, уплотнение в МЖ достаточно подвижное, с четкими границами, бугристой поверхностью, безболезненное. При надавливании на это образование молоко выделяется свободно, сцеживание его безболезненно. Уплотнение определяется на фоне болезненности и напряженности всей железы. После сцеживания женщина ощущает облегчение.
Общее состояние организма женщины при остром застое молока ухудшается незначительно. Температура тела, клинические анализы крови чаще остаются нормальными, при исследовании секрета МЖ изменений не определяется. Как правило, при лактостазе отсутствуют два основных признака воспалительного процесса: гиперемия и гипертермия. Однако в ряде случаев острый застой молока может сопровождаться лихорадкой, значительным повышением температуры. Очень важно, что после сцеживания температура нормализуется и женщина ощущает облегчение. Острый лактостаз — процесс, как правило, двусторонний и развивается в период между 3–5-м днями после родов, т.е. в сроки прилива молока.
Особенно трудно дифференцировать от острого застоя молока начальные формы мастита. При проникновении в ткань молочной железы гноеродной микрофлоры застой молока через 2–4 дня, а иногда и в течение одного дня, переходит в серозную стадию мастита. Заболевание начинается остро, с озноба, повышения температуры, потливости, слабости, ощущения разбитости, резких болей в железе. Грудь увеличивается в размере, пальпация ее становится болезненной, инфильтрат определяется нечетко. Сцеживание молока болезненно и не приносит облегчения. В крови наблюдается лейкоцитоз до 10–12 тыс., СОЭ увеличена до 20–30 мм/ч. При несвоевременно начатом лечении через 2–3–6 дней процесс может перейти в инфильтративную фазу, которая характеризуется большей выраженностью клинических признаков воспаления, тяжестью общего состояния больной. Пальпируемое опухолевидное образование приобретает более четкие контуры. В крови наблюдается тенденция к моноцитозу и эозинофилии. У 80 % больных температура тела повышается до 38,0–41,0 °С. Контактная термометрия выявляет повышение локальной температуры в МЖ у 78,8 % больных от 35,7 до 36,9 °С (средняя температура кожи МЖ у здоровых женщин 38,3 °С).
Переход начальной формы мастита в гнойную характеризуется усилением общих и местных симптомов воспаления, при этом выражены признаки гнойной интоксикации. Температура держится постоянно на высоких цифрах или приобретает гектический характер. Инфильтрат в железе увеличивается, гиперемия кожи нарастает, в одном из участков железы появляется флюктуация, которая еще раньше возникает при поверхностно расположенных гнойниках. В ряде случаев присоединяются явления лимфангоита, регионального лимфаденита. Абсцессы могут локализовываться в поверхностных или глубоких отделах железы с распространением в ретромаммарное пространство. Крайне тяжелое состояние больных наблюдается при гангренозной форме мастита: температура тела до 40–41 °С; тахикардия — пульс до 120–130 уд/мин; МЖ резко увеличена в объеме, кожа ее отечная, с пузырями, наполненными геморрагическим содержимым, с участками некроза; отечность распространяется на окружающие ткани; в крови высокий лейкоцитоз со сдвигом лейкоцитарной формулы влево и токсической зернистостью лейкоцитов; в моче определяется белок.
Наряду с выявлением клинических симптомов диагностики начальных форм мастита используют лабораторные методы исследования секрета МЖ. Секрет МЖ в норме характеризуется слабокислой реакцией (pH = = 6,8). Воспалительный процесс приводит к изменению кислотности молока в сторону увеличения pH, что связано с повышением активности щелочной фосфатазы.
Также для распознавания ранних и стертых форм ЛМ применяют УЗИ, тепловидение, термографию, а в отдельных случаях (в настоящее время крайне редко) — маммографию.
Лечение
Главным залогом успешного лечения является, конечно же, качественная диагностика. Подходы к лечению лактостаза, ранней стадии мастита (серозная, инфильтративная) и при гнойно-деструктивных формах имеют принципиальные отличия.
При лактостазе прежде всего необходимо провести мероприятия, направленные на устранение его причины. Необходимо выяснить режим кормления, провести консультирование кормящей для обеспечения кормления по требованию, только грудного вскармливания без дополнительного применения смесей, сосок, бутылочек и т.д., проконтролировать правильность прикладывания новорожденного к груди. Женщине рекомендуется соблюдать определенную диету, которая не провоцирует задержку жидкости, отечность, т.е. исключить сладкие, жирные, соленые продукты. При явном избытке молока в первые дни становления лактации можно перед кормлением новорожденного излишки молока сцедить.
Для профилактики и лечения лактостаза хорошо зарекомендовало себя натуральное масло Weleda Stillol (Германия), которое содержит эфирные масла фенхеля и тмина, обладает противовоспалительным и противоотечым действием, улучшает микроциркуляцию и отток молока.
«…Грудница стара, как человеческий род; многие миллионы женщин болеют ею, и с незапамятных времен врачи изощрялись в лечении ее, но в наше время, при блестящем рассвете хирургии, мы не можем похвалиться полным умением лечить мастит» (Войно-Ясенецкий, 1956). Впервые высказанная 50 лет назад, эта мысль не утратила своей актуальности и в наше время. Проблема лечения мастита по-прежнему представляется сложной и не решенной до конца. Несмотря на простоту лечебных мероприятий и техники оперативного вмешательства, ошибки в лечении больных встречаются довольно часто.
Основные принципы лечения мастита:
1. Продолжение грудного вскармливания.
2. Своевременная регулярная эвакуация молока.
3. Элиминация возбудителя (антибактериальная терапия).
4. Лечение трещин сосков.
5. Раннее начало лечения.
6. Лечение проводится с учетом формы и фазы процесса.
Как только диагноз послеродового мастита уточнен, терапия антибиотиками должна быть начата, чтобы гарантировать оптимальный результат. Задержка лечения значительно увеличивает частоту формирования абсцесса.
Какие бы лечебные методы ни применялись, необходимо соблюдать основной принцип: проводить лечение мастита с учетом фазности, стадийности процесса: на начальных стадиях показана комплексная консервативная терапия, в деструктивную фазу процесса — хирургическая операция с последующим лечением гнойной раны.
Лечение может проводиться или в амбулаторных условиях, или в стационаре, в зависимости от серьезности состояния пациентки. Системные признаки должны быть ограничены лихорадкой и умеренным недомоганием. В случае амбулаторного лечения повторный осмотр и оценка состояния пациентки обязательны в течение 24–48 часов. Если отсутствует положительная динамика как ответ на терапию антибиотиками, женщина должна быть госпитализирована.
Удалению из МЖ микроорганизмов и продуктов их жизнедеятельности, уменьшению застоя молока способствует продолжение кормления грудью.
Лечение послеродового мастита должно быть этиотропным, комплексным, специфическим и активным. Оно должно включать антибактериальные препараты, дезинтоксикационные и десенсибилизирующие средства, методы повышения специфической иммунологической реактивности и неспецифической защиты организма, при гнойном мастите — своевременное оперативное вмешательство.
Антибиотики являются основным компонентом в комплексной терапии послеродового мастита. Основные требования к антибиотикам, применяемым во время лактации:
— безвредность для матери и новорожденного;
— широкий спектр действия (прежде всего против грамположительных кокков и грамотрицательных палочек);
— достаточная концентрация и тропность к ткани молочной железы;
— комплайентность (удобный для пациентки способ и режим применения).
Выделение антибактериальных препаратов с женским молоком
При выделении антибиотиков с женским молоком они попадают в организм ребенка и могут оказывать на него неблагоприятное действие, которое, в свою очередь, проявляется в виде токсических и аллергических реакций. Весьма существенные изменения может претерпевать нормальная микрофлора организма матери и ребенка.
Неблагоприятному воздействию антибиотиков, попавших в организм новорожденного с молоком матери, способствует незрелость печени и почек, свойственная этому периоду развития. У новорожденных отмечается замедленное всасывание препаратов из желудочно-кишечного тракта, более низкий метаболизм по сравнению со взрослым организмом, главным образом за счет снижения метаболической активности печени, более медленное выведение препаратов почками.
Низкое связывание антибиотиков белками сыворотками крови, отмечающееся у новорожденных по сравнению с кровью взрослых, приводит к более полной диффузии их из крови в ткани, где создается высокий уровень препаратов. Указанные особенности циркуляции антибиотиков у новорожденных приводят к более длительному их пребыванию в организме, обусловливают кумуляцию препаратов и таким образом повышают возможность вредного воздействия на организм ребенка.
Практически все антибактериальные препараты, вводимые лактирующей женщине, проникают в молоко. Однако степень их перехода существенно отличается для препаратов разных групп. Одни антибиотики легко проникают в молоко и создают в нем сравнительно высокий уровень, другие переходят в молоко в малых количествах и не представляют реальной опасности для ребенка. Антибиотики попадают в молоко преимущественно путем диффузии, определяющейся такими же факторами, что и диффузия через плацентарный барьер и другие биологические мембраны. На степень диффузии в молоко влияют молекулярная масса препарата, степень ионизации, связывание белками крови, растворимость в липидах. По сравнению с плазмой крови молоко имеет более низкий pН (7,4 и 6,8 соответственно), вследствие чего препараты с кислотными характеристиками проходят в молоко труднее, чем со щелочными. Для оценки степени диффузии лекарственных веществ в молоко предложен индекс М/П, представляющий собой соотношение концентрации препарата в молоке и плазме крови. Величина индекса меньше 1 свидетельствует о низкой степени перехода вещества в молоко, индекс больше 1 характеризует высокую степень перехода.
Ниже приведены сведения о переходе в грудное молоко антибактериальных препаратов, наиболее часто используемых при лечении послеродовых инфекций.
Пенициллины. Антибиотики этой группы в ограниченном количестве переходят в молоко при введении кормящим родильницам. Бензилпенициллин содержится в грудном молоке в концентрации в 20–30 раз меньше по сравнению с уровнем его в сыворотке крови при введении женщинам терапевтических доз. Такая же закономерность отмечается и для полусинтетических пенициллинов. Максимальная концентрация метициллина в молоке здоровых родильниц составляет 0,45 мкг/мл, что в 12–13 раз ниже максимальной концентрации в сыворотке крови. Содержание оксацилина в молоке в 19 раз ниже, чем в крови. При воспалительном процессе молочной железы переход этих антибиотиков в молоко уменьшается. При этом оксациллин переходит в грудное молоко больных в большем количестве, чем метициллин, что свидетельствует о более высокой способности этого антибиотика проникать в очаг воспаления.
Сравнительно низкая степень перехода в молоко характерна и для пенициллинов широкого спектра действия (ампицилин, амоксициллин, пиперациллин и др.), низкая экскреция пенициллинов с молоком связана с высокой степенью их связывания белками плазмы крови (кроме ампициллина) и интенсивным выведением почками. Индекс М/П для пенициллинов существенно меньше 1.
Цефалоспорины. Ряд данных свидетельствует об ограниченном переходе в молоко цефалоспориновых антибиотиков. Так, максимальная концентрация цефуроксима здоровых родильниц наблюдается через 1 ч после его введения и составляет 2,6 % от максимального уровня в крови. При воспалительном процессе в молочной железе отмечается увеличение перехода антибиотика в молоко по сравнению со здоровыми родильницами.
Цефрадин также проникает в материнское молоко в незначительном количестве. Воспалительный процесс в грудной железе увеличивает прохождение антибиотика в молоко, однако его количество не превышает 0,5–0,6 мкг/мл. Имеются сведения о плохом выделении с молоком цефалоспоринов второго и третьего поколений. Так, при внутривенном введении цефотаксима концентрация его в молоке была минимальна: концентрационный градиент составлял всего 0,035.
Таким образом, цефалоспориновые антибиотики, как и пенициллины, плохо проникают в молоко. Соотношение М/П для этих препаратов ниже 1, однако их максимальная концентрация в молоке несколько выше, чем для пенициллинов.
Макролиды. Проникают в грудное молоко в сравнительно высоких концентрациях, достигая в среднем 50 % от уровня в крови матери. Наиболее низкие концентрации отмечаются при введении эритромицина. Такие антибиотики, как кларитромицин, спирамицин, создают в молоке высокие концентрации. Что касается азитромицина, то до настоящего времени нет достоверных данных о его уровне в грудном молоке. Отрицательного влияния на ребенка, получающего молоко матери, леченной макролидами, не отмечается. Поэтому при необходимости эти препараты могут быть использованы для лечения женщины во время лактации.
Аминогликозиды. Большинство антибиотиков этой группы проникает в грудное молоко в низких концентрациях. Однако адекватных и строго контролируемых исследований не проводилось, так как аминогликозиды не рекомендуется применять во время беременности и лактации из-за их ото- и нефротоксичности. Известно, что максимальная концентрация гентомицина составляет 30 % от его уровня в крови матери и создается через 1 ч после введения антибиотика. Аминокацин, тобрамицин, канамицин, стрептомицин проникают в молоко в низких концентрациях. Возможен ототоксический эффект и влияние на микрофлору кишечника новорожденных.
Тетрациклины. Тетрациклины (доксициклин, тетрациклин) хорошо проникают в грудное молоко. Их уровень составляет 50–70 % от уровня в крови матери. Индекс проницаемости — 1,2–1,6. Тетрациклины вызывают нарушение развития зубных зачатков, роста костей, образуя комплексные соединения с кальцием. Вследствие этого тетрациклины при грудном вскармливании применять не рекомендуется.
Клиндамицин, линкомицин. Клиндамицин обнаруживается в молоке в сравнительно небольшой концентрации. Применять его в период лактации не рекомендуется из-за возможности развития псевдомембранозного колита. Линкомицин проникает в молоко в большом количестве: его концентрация составляет 50–90 % от уровня в крови матери. Применение препарата во время лактации запрещено из-за возможности изменения кишечной микрофлоры ребенка и его сенсибилизации.
Фторхинолоны. Известно, что все фторхинолоны проникают в грудное молоко. Наиболее высокие концентрации отмечены у ципрофлоксацина. Но адекватных и строго контролируемых исследованний не проводилось. Применять препараты этой группы во время лактации не рекомендуется из-за высокого риска артротоксичности.
Сведений о проникновении в молоко других антибиотиков недостаточно, и они часто противоречивы.
Антибиотики, безопасные при кормлении грудью: пенициллины (бензилпенициллин, амоксициллин, амоксициллин/клавуланат, ампициллин); макролиды (азитромицин, джозамицин, кларитромицин); цефалоспорины (цефазолин, цефокситин, цефуроксим, цефметазол, цефтриаксон).
Недопустимы к применению при кормлении грудью: сульфаниламиды, линкозамины (клиндамицин, линкомицин — только в крайних случаях), производные имидазола (при назначении метронидазола прекратить кормление грудью на 12–24 ч), тетрациклины, фторхинолоны, левомицетин.
Препаратами выбора следует считать полусинтетические пенициллины: оксациллин, амоксициллин (например, амофаст, флемоксин солютаб, флемоклав). При наличии перекрестной аллергии назначаются макролиды, цефалоспорины (цефазолин, цефалексин, цефтриаксон (лендацин), цефотаксим). Лендацин, который относится к парентеральным цефалоспоринам III поколения, выделяется необычными фармакокинетическими свойствами, в первую очередь длительным периодом полувыведения (8,5 ч), что позволяет использовать его в удобном режиме — 1 раз в сутки. Так же как и другие цефалоспорины, лендацин хорошо переносится и используется во время беременности и лактации без каких-либо ограничений. Макролиды считаются сравнительно безопасными при беременности (за исключением рокситромицина), но в связи с проникновением в грудное молоко и отсутствием данных о влиянии на новорожденного их с осторожностью следует использовать в период лактации. Препараты обладают эффектом в отношении широкого спектра грамположительных и грамотрицательных бактерий, проникают внутрь фагоцитов и переносятся в очаг инфекции этими клетками. Макролиды создают высокие концентрации в тканях, намного превышающие концентрации в плазме. К макролидам малочувствительны энтеробактерии и синегнойная палочка. Интерес к макролидам возрос в связи с введением новых препаратов, таких как азитромицин (сумамед), характеризующихся улучшенной фармакокинетикой, расширенным спектром действия и повышенной безопасностью по сравнению с эритромицином.
Необходимая продолжительность терапии антибиотиками не была установлена точно. Большинство исследователей рекомендуют лечение от 5 до 10 дней. После клинического выздоровления необходимо продолжить лечение еще 48 часов. Пациентки со стафилококковой бактериемией нуждаются в более длительном лечении. Распространение staphylococci может вести к формированию абсцессов в почках, костях и других осложнений. Кроме того, S.aureus — один из немногих организмов, способных к инфицированию нормальных сердечных клапанов, с развитием разрушительного острого бактериального эндокардита. Ввиду особой серьезности стафилококковая бактериемия требует курс лечения от 10 до 14 дней. Если есть любое свидетельство метастазирования абсцесса или бактериального эндокардита, необходим более длительный курс терапии.
Рекомендуется использование стафилококкового бактериофага. Широко назначаются средства, повышающие иммунореактивность организма, витамины. Местное лечение проводится не «компрессами», а в виде аппликаций с гелями и мазями, улучшающими микроциркуляцию и обладающими противовоспалительным эффектом. Хорошо зарекомендовали себя аппликации с маслом камфоры, разведенным в соотношении 1 : 1 с любым очищенным маслом, полуспиртовые аппликации. Физиопроцедуры широко применяются при лактостазе (ультразвук), трещинах сосков (терапевтический лазер). Не рекомендуется применять физиолечение в остром периоде мастита, при гнойных и деструктивных формах оно категорически противопоказано.
Несмотря на соответствующее управление маститом, переход в гнойно-деструктивные формы происходит в 4–10 % случаев. Это осложнение требует незамедлительного хирургического вмешательства в хирургическом стационаре. Хирургический разрез и дренирование осуществляются в операционной под наркозом. Разрезы должны быть выполнены по естественным линиям кожи, радиально или параллельно ареолярному краю. Это учитывает адекватный дренаж и лучший косметический результат. Дополнительно с целью дифференциальной диагностики часть стенки абсцесса должна быть отправлена на патогистологическое исследование, так как формирование абсцесса может происходить параллельно с развитием злокачественного новообразования. После дренирования абсцесса рана должна быть хорошо промыта антисептиками и оставаться открытой. Разрезы, выполненные параллельно ареолярному краю по естественной линии кожи, обычно заживают с минимальным рубцеванием, даже когда заживление происходит вторичным натяжением.
Ранняя диагностика послеродового мастита позволяет быстро начать противовоспалительную терапию и минимизирует воздействие на мать и младенца. В послеродовом периоде должно быть тщательное наблюдение за кормящими, и начинающийся мастит и лактостаз должны диагностироваться как можно раньше. Мерами и обязательными условиями профилактики являются соблюдение санитарно-гигиенического режима, своевременное выявление и санация очагов инфекции, соблюдение режима естественного грудного вскармливания, правильное прикладывание новорожденного к груди, внимательное и доброжелательное отношение медицинского персонала.
Выводы
1. Острые маститы в основном (82–87 % случаев) встречаются в послеродовом периоде у кормящих женщин. Несмотря на значительные успехи профилактической медицины в борьбе с неспецифической хирургической инфекцией, лактационный мастит продолжает оставаться актуальной проблемой как в гнойной хирургии, так и в практике акушера-гинеколога.
2. Мастит развивается у 2–5 % лактирующих женщин. Точно определить причину мастита трудно. Входными воротами для бактерий чаще всего являются трещины сосков.
3. Острый мастит может развиться в любое время в течение кормления грудью, но в основном это происходит в течение первого месяца постнатального периода. Возможно, предрасположенность к лактостазу в первые недели после родов объясняет высокую заболеваемость маститом в этот период.
4. Основными причинами лактационного мастита являются застой молока и госпитальная инфекция. Прекращать кормление грудью не рекомендуется, т.к. важен регулярный отток молока. При сохранении грудного вскармливания мастит прогрессирует в гнойный или абсцесс только в 4 % случаев. При гнойно-деструктивных формах, требующих обязательного хирургического лечения, вопрос о сохранении грудного вскармливания решается индивидуально. Лактация сохраняется во всех случаях, когда это возможно.
5. Ранняя диагностика послеродового мастита позволяет быстро начать противовоспалительную терапию и минимизирует воздействие на мать и младенца. В послеродовом периоде должно быть тщательное наблюдение за кормящими, и начинающийся мастит и лактостаз должны диагностироваться как можно раньше.
6. Мерами и обязательными условиями профилактики являются соблюдение санитарно-гигиенического режима, своевременное выявление и санация очагов инфекции, соблюдение режима естественного грудного вскармливания, правильное прикладывание новорожденного к груди, внимательное и доброжелательное отношение медицинского персонала.
1. Абрамченко В.В., Башмакова М.А., Корхов В.В. Антибиотики в акушерстве и гинекологии. Руководство. — СПб.: СпецЛит, 2001. — 239 с.
2. Бiлоненко Г.А. Малоiнвазивнi втручання пiд контролем сонографii при гнiйному пiсляпологовому маститi // Вестник неотложной и восстановительной медицины. — 2001. — Т. 2, № 2–3. — С. 144-147.
3. Карпов О.И., Зайцев А.А. Риск применения лекарственных препаратов при беременности и лактации. — СПб.: Издательство «Диля», 2003. — 352 с.
4. Куприненко Н.В. Фармакокинетика антимикробных препаратов во время беременности и их действие на плод // Новости медицины и фармации. — 2010. — № 310. — С. 50-57.
5. Ласачко С.А. Диагностика и лечение диффузных доброкачественных заболеваний молочной железы // Современные направления амбулаторной помощи в акушерстве и гинекологии. — Донецк: ООО «Лебедь», 2003. — С. 195-203.
6. Ласачко С.А., Морозова Н.А. Деякі особливості лактації серед породіль, які раніше вживали різні методи контрацепції // Вісник проблем біології і медицини. — 1999. — № 4. — С. 26-29.
7. Оскретков В.И., Кокин Е.Ф. Хирургическое лечение больных с острым абсцедирующим и флегмонозным лактационным маститом // Вестник хирургии. — 2001. — Т. 160, № 2. — С. 70-76.
8. Стан здоров’я жiночого населення в Українi за 2003 рiк // МОЗ України, Центр медичної статистики. — Київ, 2004. — 216 с.
9. Усов Д.В. Избранные лекции по общей хирургии. — Тюмень, 1995.
10. Чайка В.К., Ласачко С.А., Квашенко В.П. Роль акушера-гинеколога в выявлении и профилактике заболеваний молочных желез // Новости медицины и фармации. — 2004. — № 7(май). — С. 14-15.
11. Частная хирургия / Под ред. Ю.Л. Шевченко. — СПб.: СпецЛит, 2000. — Т. 1. — С. 129-142.
12. Юхтин В.И., Чадаев А.П., Хуторянский И.Н. О хирургической классификации мастита // Мед. помощь. — 1995. — № 2. — С. 21-23.
13. Duff P. Staphylococcal infections // Principles of medical therapy in pregnancy / Ed. by N. Gleicher. — New York: Plenum, 1985. — 437-41.
14. Douglas A. Milligan and Patrick Duff. Puerperal Mastitis. Obstetric and Gynecologic Infectious Disease / Ed. by Joseph G. Pastorek // II. Raven Press, Ltd. — New York, 1994.
15. Оgle K.S., Davis S. Mastitis in lactating women // J. Fam. Pract. — 1988. — 26(2). — 139-44.
16. Riddick D.H. The nonlactating human breast // Gynecology and obstetrics / Ed. by J.J. Sciarna, J.L. Simpson, L. Speroff. — Philadelphia: Lippincott; 1989. — (5). — 1-9.
17. Thomsen A.C., Espersen T., Maigaard S. Course and treatment of milk stasis, nonifectious inflammation of the breast, and infectious mastitis in nursing women // Am. J. Obstet. Gynecol. — 1984. — 149(5). — 492-5.
