Газета «Новости медицины и фармации» 21 (349) 2010
Вернуться к номеру
Что может Церебролизин при сосудистых деменциях?
Авторы: А.В. Савустьяненко, к.м.н., Донецкий национальный медицинский университет им. М. Горького
Версия для печати
Многие ученые считают, что XXI век можно назвать веком моделирования. В самом деле, можно зайти в Интернет и найти девушку, дающую интервью. Вы ее слушаете, вас ничего не настораживает, пока на сайте не появляется надпись, что это всего лишь фантазия программиста... Аналогичным образом можно пообщаться с Джоном Ленноном, некогда легендарным солистом группы «Битлз», — вы ему зададите вопрос, а он вполне здраво ответит на него…
Можно много говорить о том, полезны подобные модели или нет. Но одно бесспорно: если мы можем создать реалистичную модель — значит, мы владеем всей информацией об объекте, который моделируем.
Сегодня, говоря о пользе Церебролизина при сосудистых деменциях, мы тоже применили принцип моделирования. Церебролизин — ноотропный препарат, действующий подобно факторам роста нервной ткани. Он достаточно долго находится на рынке, хорошо исследован и потому может претендовать на то, чтобы участвовать в модели. Ниже вашему вниманию будет предложена беседа трех виртуальных собеседников: пациента, доктора и научного консультанта, посвященная аспектам применения Церебролизина при сосудистых деменциях…
Пациент. Доктор, не могу понять, что со мной происходит. В последнее время появилась какая-то забывчивость — не всегда сразу могу вспомнить фамилию или имя хорошо знакомого мне человека, не помню, куда кладу лекарства… Мне трудно удерживать свое внимание на чем-либо, например на сюжете просматриваемого фильма. Я уже несколько раз замечал, что иногда мне трудно ориентироваться в тех частях города, которые я хорошо знаю. Покупки в магазине и вовсе сбивают меня с толку. Я на пенсии, но продолжаю работать. И в последнее время задачи, связанные с планированием или проработкой новой информации, стали мне очень сложно даваться. Каким бы видом деятельности я ни занимался дома и на работе, быстро устаю. Иногда меня беспокоят приступы головокружения, бывает, я слышу шум в ушах.
Доктор. Учитывая ваш возраст, ухудшение памяти, внимания и мышления, нарушение ориентации в знакомой обстановке, повышенную утомляемость, головокружение, шум в ушах, а также данные объективного обследования и дополнительных методов исследования — ЭЭГ и МРТ, следует признать, что работа вашего мозга ухудшилась из-за нарушения его кровоснабжения. Более строго это называется сосудистой деменцией.
Научный консультант. Сосудистые поражения головного мозга считаются второй по частоте причиной деменции у лиц пожилого и старческого возраста после болезни Альцгеймера. Однако в славянских и азиатских странах сосудистая деменция встречается чаще, чем болезнь Альцгеймера. Сосудистая деменция — это не единое состояние, а несколько клинико-патоморфологических и клинико-патогенетических синдромов, общей для которых является взаимосвязь цереброваскулярных расстройств с когнитивными нарушениями [1].
Множество причин может приводить к развитию сосудистой деменции. Это могут быть поражения самих сосудов головного мозга (атеросклероз, аномалии сосудов), патология сердца (кардиомиопатии), патология системы крови (гемоглобинопатии). При этом какими бы ни были этиологические факторы, повреждение головного мозга обычно протекает либо по механизму ишемии, либо по механизму геморрагии.
К основным факторам риска, увеличивающим вероятность развития сосудистой деменции, относят артериальную гипертензию, сахарный диабет, ожирение, курение и злоупотребление алкоголем.
Клиническая картина сосудистой деменции может быть разнообразной и включает обычно совокупность когнитивных и двигательных нарушений. Когнитивные процессы характеризуются быстрой истощаемостью и включают ухудшение памяти, внимания, мышления (нарушение процессов обобщения понятий и др.), появление апатии, депрессии. В клинической картине могут появиться такие расстройства высших мозговых функций, как апраксия и агнозия. Спектр двигательных расстройств также довольно широк — от минимально выраженных признаков пирамидной недостаточности до выраженной атаксии либо плегии [1].
Пациент. Доктор, вы могли бы предложить эффективное лечение той патологии, которую вы обнаружили у меня?
Доктор. К сегодняшнему дню медицине известна целая группа лекарственных средств, называемых ноотропами, которые улучшают функцию мозга при сосудистой деменции. Чтобы ответить на вопрос о том, какое же средство является лучшим, необходимо посмотреть, как поддерживается функция мозга в здоровом организме человека. Ученым удалось выяснить, что целостность нервных клеток поддерживается за счет специальных регуляторных молекул, называемых факторами роста. Если эти молекулы присутствуют в достаточном количестве, то нервные клетки хорошо питаются, делятся, устойчивы к разрушительным воздействиям. Отсюда следует, что идеальное ноотропное средство должно «имитировать» эти процессы, то есть действовать так же, как природные факторы роста. И, к счастью, на рынке присутствует такой препарат под названием Церебролизин. Его мы вам и назначим. Вы получите курс лечения Церебролизином в течение 4 недель. Каждую неделю в течение 5 дней (понедельник — пятница) вам будут вводить внутривенно 20 мл Церебролизина один раз в день, 2 дня (суббота, воскресенье) будут перерывом между приемами препарата. Мы с вами будем регулярно видеться по ходу лечения, а по окончании курса терапии встретимся еще раз и посмотрим, насколько эффективной она была.
Научный консультант. Рекомендуемая доза Церебролизина при лечении сосудистой деменции составляет 10–30 мл/сут (зависит от тяжести деменции). Курс лечения составляет 5 дней в неделю в течение 4 недель. Для поддержания достигнутого эффекта терапии рекомендуется проводить 2–4 курса лечения в год [2].
Церебролизин является ноотропным средством природного происхождения, получаемым из головного мозга молодых свиней [3]. В состав Церебролизина входят нейропептиды (фрагменты фактора роста нервов, тиролиберин, глутатион), аминокислоты, макро- и микроэлементы, витамины и некоторые другие вещества [3–5].
Под фармакологической нейропротекцией в широком смысле понимают комплекс фармакокинетических и фармакодинамических влияний, направленных на улучшение питания нервных клеток (нейротрофическое действие), защиту их от повреждающих факторов (собственно нейропротекция), повышение выживаемости нейронов, стимуляцию нейропластичности и нейрогенеза. Данные, накопленные к сегодняшнему дню, свидетельствуют о том, что Церебролизин в значительной мере проявляет каждый из перечисленных компонентов нейропротекции.
Нейротрофическое действие Церебролизина связано с тем, что он усиливает микроциркуляцию в тканях мозга [6, 7]. Кроме того, данный препарат усиливает потребление кислорода и доставку глюкозы к нервным клеткам. В частности, Церебролизин усиливал потребление кислорода гомогенатами из мозга крыс, причем эффект был особенно хорошо выражен у самых молодых и старых особей [8].
Нейропротективное действие Церебролизина включает в себя комплекс фармакологических эффектов, направленных на борьбу с перекисным окислением липидов, эксайтотоксичностью и повышением внутриклеточной концентрации кальция, активацией микроглии и иммунным дисбалансом.
В частности, было показано, что Церебролизин тормозит образование супероксидного анион-радикала, монооксида азота и конечных продуктов деградации жирных кислот [9]. Кроме того, было продемонстрировано, что данный препарат снижает уровни каталазы и супероксиддисмутазы в плазме крови интактных крыс и после повреждения септогиппокампального пути [10].
В доступной литературе нет сведений о том, что Церебролизин способен угнетать высвобождение возбуждающих нейромедиаторов или уменьшать поступление ионов Ca2+ внутрь нейронов. Однако в ряде исследований была продемонстрирована способность данного препарата защищать клетки от эксайтотоксичности. Например, в одной из более ранних работ было показано, что предварительное введение Церебролизина защищает мозг мышей от эксайтотоксичности, вызванной интраперитонеальным введением каиновой кислоты [11].
При повреждении нервной системы разнообразными острыми и хроническими заболеваниями наблюдается активация микроглии, что инициирует течение местного нейровоспаления и приводит к формированию синдрома системного воспалительного ответа (ССВО). В связи с этим представляет интерес исследование, в рамках которого Церебролизин добавляли к культуре глиальных клеток, обработанных бактериальным полисахаридом. Было обнаружено, что препарат эффективно тормозит активацию микроглии и высвобождение ею интерлейкина-1β (IL-1β) [12].
Церебролизин также обладает выраженным иммуномодулирующим действием, что важно для борьбы с заболеваниями нервной системы [13, 14].
Церебролизин повышает выживаемость нейронов путем повышения их способности переживать гипоксию и аноксию, а также проявлять устойчивость к развитию апоптоза и некроза.
Например, в одном из исследований было выяснено, что однократная инъекция Церебролизина не влияет на устойчивость крыс к аноксии. В то же время повторное введение данного препарата увеличивает устойчивость к аноксии как у молодых, так и у старых крыс [15].
В большом количестве исследований было показано, что Церебролизин препятствует развитию апоптоза и некроза. Так, при введении Церебролизина крысам с экспериментальным ишемическим инсультом было отмечено повышение устойчивости нейронов к ишемическому повреждению и замедление развития апоптоза. В клетках наблюдались морфологические изменения, однако они отражали адаптивные и репаративные процессы. Например, имели место фолдинг ядерной мембраны, накопление полирибосом, гипертрофия эндоплазматического ретикулума и комплекса Гольджи. В целом Церебролизин сохранял структуру ядерных мембран и большинства внутриклеточных органоидов [16].
Церебролизин способен поддерживать нейропластичность. В нескольких исследованиях было показано, что при острых повреждениях мозга (например, ишемии) Церебролизин ингибирует кальпаин, что препятствует процессу распада МАР2 (белок, входящий в состав микротрубочек цитоскелета). При хронических повреждениях мозга, таких как нейродегенеративные заболевания, Церебролизин увеличивает экспрессию гена, ответственного за синтез МАР2. В конечном счете все описанные механизмы приводят к сохранению целостности цитоскелета и нормализации ветвления дендритов, что способствует сохранению пластичности. Одновременно увеличивается выживаемость нейронов [17–19].
Под нейрогенезом понимают способность к образованию новых нервных клеток. В связи с открытием того факта, что нейрогенез протекает не только в развивающемся, но и во взрослом мозге, особый интерес представляет способность тех или иных ноотропных средств влиять на этот процесс. Результаты исследований свидетельствуют о том, что Церебролизин способен усиливать нейрогенез, причем усиление образования новых нейронов наблюдалось в основном в зубчатой извилине гиппокампа. Однако тонкие механизмы подобного действия пока не ясны и требуют дальнейшего изучения [20–22].
Прошло 4 недели…
Доктор. Итак, прошло 4 недели, и курс лечения закончен. Изменилось ли за это время как-то ваше состояние?
Пациент. Доктор, безусловно, да! Значительно уменьшилась моя забывчивость — вот, например, читаю газету, и те новости, которые почерпнул оттуда, могу пересказать другим людям даже через несколько дней. Мне легче концентрировать внимание при просмотре фильма или во время выполняемой деятельности. У меня больше не возникает проблем с перемещением по городу, посещением магазинов… Качество моей жизни настолько улучшилось, что мне хочется жить и я с оптимизмом смотрю в будущее. Меня, правда, все еще беспокоят головокружение и шум в ушах, однако происходит это значительно реже, чем раньше.
Научный консультант. Способность Церебролизина уменьшать выраженность когнитивных нарушений была показана во многих исследованиях.
Например, в двойное слепое плацебо-контролируемое исследование, выполненное Guekht и соавт. [23, 24], были включены 242 пациента с сосудистой деменцией. Всех пациентов рандомизировали на две группы: 1) получавшие лечение ацетилсалициловой кислотой 100 мг/день + + Церебролизин 20 мл/день; 2) получавшие лечение ацетилсалициловой кислотой 100 мг/день + плацебо. Пациенты принимали Церебролизин и плацебо 5 дней в неделю в течение первых 4 недель. Затем был сделан перерыв в лечении на 2 месяца. После этого курс лечения повторили (прием препаратов 5 дней в неделю в течение 4 недель), и за больными наблюдали еще 2 месяца. Таким образом, исследование было завершено через 6 месяцев после его начала. Эффективность лечения оценивали в основном по двум шкалам: ADAScog+ и CIBIC+. Шкала ADAScog+ отражает состояние когнитивных функций, в то время как шкала CIBIC+ характеризует общий уровень функционирования пациентов (помимо когнитивных функций оценивается поведение пациентов, активность в повседневной жизни и т.д.).
В результате было обнаружено, что Церебролизин эффективнее плацебо (p < 0,0001) изменял значения по шкале ADAScog+ в лучшую сторону во всех контрольных точках времени по сравнению с исходным состоянием (рис. 1). К 6-му месяцу (8-я неделя после окончания второго курса лечения) разница средних наименьших квадратов между Церебролизином и плацебо составила –6,17 балла (95% ДИ –8,22, –4,13; p < 0,0001).
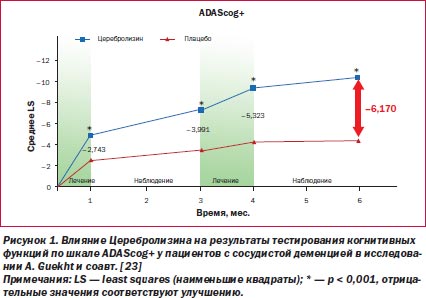
Другой первичной конечной точкой исследования было изменение значений по порядковой шкале CIBIC+ (1–3 — улучшение, 4 — нет изменений, 5–7 — ухудшение) к 6-му месяцу по сравнению с исходными условиями. По этому параметру Церебролизин также превосходил плацебо (p < 0,0001). Дополнительно с помощью шкалы CIBIC+ было выявлено, что в группе Церебролизина клинически значимые улучшения наблюдались у 75,2 % больных, в то время как в группе плацебо — только у 37,4 % больных (отношение шансов 5,081; 95% ДИ 2,889, 8,936; p < 0,05) (рис. 2).
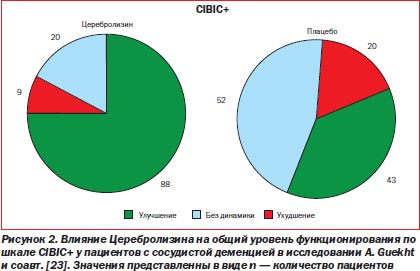
В другое рандомизированное двойное слепое плацебо-контролируемое многоцентровое исследование, выполненное Xiao и соавт. [24, 25], было включено 147 пациентов с сосудистой деменцией легкой и умеренной степени тяжести. В ходе исследования было обнаружено, что короткий курс лечения Церебролизином в дозе 30 мл/день (5 дней в неделю в течение 4 недель) приводил к улучшению когнитивной деятельности, о чем свидетельствовали изменения шкалы MMSE в конце лечения по сравнению с исходным уровнем (первичная конечная точка исследования; шкала MMSE позволяет оценить состояние когнитивных функций у пациентов). Среднее увеличение по шкале MMSE к 4-й неделе по сравнению с исходными значениями составило 2,7 балла в группе Церебролизина и 1,7 балла в группе плацебо (р = 0,028) (рис. 3).
Пациент. Доктор, скажите, а изменились ли на фоне лечения Церебролизином результаты инструментальных обследований моего головного мозга?

Доктор. Да, действительно, есть некоторые улучшения. Дело в том, что при нарушении кровоснабжения головного мозга ухудшается работа нейронов, что проявляется увеличением так называемой медленноволновой активности на ЭЭГ. После лечения Церебролизином работа нейронов восстанавливается, что проявляется увеличением доли быстроволновой активности. Именно этот феномен наблюдается и в вашем случае.
Научный консультант. В исследование Muresanu и соавт. [26] был включен 41 пациент с легкой и умеренной сосудистой деменцией. Пациенты получали внутривенные инфузии Церебролизина (10 или 30 мл) или плацебо (физиологический раствор) 5 дней в неделю в течение 4 недель. В исходных условиях (до лечения) значения по шкале ADAScog+ положительно коррелировали с мощностью дельта-ритма, тета-ритма и отношением мощности медленного ритма к быстрому ритму, но отрицательно коррелировали с альфа-ритмом (по данным количественной ЭЭГ). Подобный характер корреляций свидетельствовал о том, что замедление ЭЭГ было связано с ухудшением когнитивных функций у пациентов. Однако спустя 4 недели на фоне лечения Церебролизином в дозе 10 мл улучшались когнитивные функции, а в дозе 10 и 30 мл уменьшалась выраженность медленных волн на ЭЭГ. Интересно, что между изменением двух показателей — значений по шкале ADAScog+ и отношения мощности медленного ритма к быстрому ритму — наблюдалась положительная корреляция.
Авторы повторно оценили вышеупомянутые показатели спустя 16 недель после начала терапии (4 недели — лечение Церебролизином, 12 недель — наблюдение за больными) [27]. К этому времени Церебролизин в дозе 10 и 30 мл улучшал когнитивные функции, а в дозе 30 мл уменьшал выраженность медленных волн на ЭЭГ по сравнению с плацебо. В эти сроки снова наблюдалась положительная корреляция между изменением тех же двух показателей — значений по шкале ADAScog+ и отношения мощности медленного ритма к быстрому ритму — относительно исходного (до лечения) уровня. Авторы пришли к выводу, что положительные эффекты Церебролизина на когнитивные функции и ЭЭГ удерживаются не менее 12 недель после окончания курса лечения препаратом. Кроме того, количественную ЭЭГ предложено использовать в качестве биомаркера тяжести сосудистой деменции.
Пациент. Доктор, я очень доволен полученным лечением. Скажите, а каково ваше мнение об эффективности проведенного курса терапии? Не считаете ли вы, что, выбрав другое средство, можно было бы достичь гораздо большего эффекта?
Доктор. Нет, я с вами полностью согласен. Налицо положительный эффект от лечения, что во многом связано с патогенетически правильным подходом к выбору лекарственного средства. Как клиницист я удовлетворен. Вряд ли мы достигли бы того же результата, выбрав любое другое из альтернативных средств.
Научный консультант. В исследование Rainer и соавт. [24, 28] были включены 645 пациентов с деменцией, получавших Церебролизин в дозе 10–50 мл в день курсом ≥ 7 дней (средняя длительность 17,8 дня). Среди пациентов 53 % имели сосудистую деменцию, 24 % — болезнь Альцгеймера и 23 % — смешанные формы деменции. Оценку эффективности лечения производили по нескольким шкалам, включая CGI — шкалу, в которой пункты эффективности отмечает врач. В результате этого исследования оказалось, что улучшение по шкале CGI наблюдалось примерно у 80 % пациентов.
Пациент. Доктор, я вам очень благодарен за проведенное лечение и за то, что вы нашли время позаниматься мной.
Доктор. Рад был помочь вам. И помните о том, что через полгода вам нужно пройти повторный курс лечения, чтобы поддержать достигнутый эффект.
1. Дамулин И.В. Сосудистая деменция // Рус. мед. журн. — 2007. — Т. 15, № 28. — С. 2118-2123.
2. http://cerebrolysin.com.ua
3. Громова О.А., Катаев А.С., Третьяков В.Е. и др. Олигопептидная мембранная фракция Церебролизина® // Международный неврологический журнал. — 2006. — № 2. — www. neurology.mif-ua.com.
4. Заваденко Н.Н. Церебролизин: данные новых зарубежных и отечественных исследований // Психиатрия и психофармакология. — 1999. — № 2. — www.consilium-medicum.com.
5. Торшин И.Ю., Громова О.А., Гусев Е.И. и др. Идентификация и анализ пептидов в составе церебролизина: пептиды фактора роста нервов // www. cerebrolysin.com.ua
6. Серкина Е.В., Громова О.А., Торшин И.Ю. и др. Церебролизин облегчает состояние больных с перинатальным поражением ЦНС через модуляцию аутоиммунитета и антиоксидантную защиту // Журнал неврологии и психиатрии. — 2008. — Т. 108, № 11. — С. 62-66.
7. Белокоскова С.Г., Цикунов С.Г. Дозозависимое влияние церебролизина на мозговой кровоток у постинсультных больных // Регионарное кровообращение и микроциркуляция. — 2009. — № 1. — С. 4-7.
8. Windisch M., Piswanger A. The effect and changes in oxygen consumption of rat brain homogenates: in vitro effect of a peptide derivative // Arzneimittelforschung. — 1985. — V. 35, № 8. — P. 1225-1227.
9. Гайнетдинова Д.Д., Семенов В.В., Исмагилов М.Ф., Харитонов B.C. Кластогенные, анеугенные, прооксидантные и антиоксидантные свойства некоторых нейротропных препаратов // Экспериментальная и клиническая фармакология. — 2006. — Т. 69, № 3. — С. 58-62.
10. González M.E., Francis L., Castellano O. Antioxidant systemic effect of short-term Cerebrolysin administration // J. Neural. Transm. (suppl.). — 1998. — V. 53. — P. 333-341.
11. Veinbergs I., Mante M., Mallory M., Masliah E. Neurotrophic effects of Cerebrolysin in animal models of excitotoxicity // Neural Transm. (suppl.). — 2000. — V. 59. — P. 273-280.
12. Lombardi V.R., Windisch M., García M., Cacabelos R. Effects of Cerebrolysin on in vitro primary microglial and astrocyte rat cell cultures // Methods Find Exp. Clin. Pharmacol. — 1999. — V. 21, № 5. — P. 331-338.
13. Сотникова Н.Ю., Громова О.А., Новикова Е.А. Нейроиммуномодулирующие свойства церебролизина // Цитокины и воспаление. — 2004. — Т. 3, № 2. — С. 34-39.
14. Гарманчук Л.В., Перепелицына Е.М., Сидоренко М.В. Цитопротекторное действие нейропептидов на иммунокомпетентные клетки (исследование in vitro) // Экспериментальная и клиническая фармакология. — 2009. — Т. 72, № 4. — С. 28-32.
15. Trojanová M., Karásek F., Pruzková V., Mourek J. Influence of cerebrolysin(r) on the resistance of rats to anoxia // Physiol. Bohemoslov. — 1976. — V. 25, № 4. — P. 319-323.
16. Onishchenko L.S., Gaikova O.N., Yanishevskii S.N. Changes at the focus of experimental ischemic stroke treated with neuroprotective agents // Neurosci. Behav. Physiol. — 2008. — V. 38, № 1. — P. 49-54.
17. Wronski R., Tompa P., Hutter-Paier B. et al. Inhibitory effect of a brain derived peptide preparation on the Ca++-dependent protease, calpain // J. Neural. Transm. — 2000. — V. 107, № 2. — P. 145-157.
18. Кульчиков А.Е. Применение церебролизина при заболеваниях периферической нервной системы // Неврологический вестник. — 2008. — Т. XV, вып. 4. — С. 110-115.
19. Windisch M., Fruhwirth M., Grygar E., HutterPaier B. Cerebrolysin normalizes MAP2 homeostasis after glutamate induced neuronal cell death // J. Neural Trans. — 2000. — V. 107, № 2. — P. 145-157.
20. Tatebayashi K., Takekawa M., Saito H. A docking site determining specificity of Pbs2 MAPKK for Ssk2/Ssk22 MAPKKKs in the yeast HOG pathway // EMBO J. — 2003. — V. 22. — P. 3624-3634.
21. Церебролизин в современной нейротрофической терапии // Мат-лы ХI Международной конференции «Новые стратегии в неврологии» (Судак, АР Крым, 26–29 апреля 2009 г.). — www.neuro.health-ua.com
22. Rockenstein E., Adame A., Mante M. et al. Amelioration of the cerebrovascular amyloidosis in a transgenic model of Alzheimer’s disease with the neurotrophic compound cerebrolysin // J. Neural Transm. — 2005. — V. 112, № 2. — P. 269-282.
23. Guekht A.B., Moessler H., Novak P.H., Gu- sev E.I. Cerebrolysin in Vascular Dementia: Improvement of Clinical Outcome in a Randomized, Double-Blind, Placebo-Controlled Multicenter Trial // J. Stroke Cerebrovasc. Dis. — 2010 (epub ahead of print).
24. Plosker G.L., Gauthier S. Cerebrolysin: a review of its use in dementia // Drugs Aging. — 2009. — V. 26, № 11. — P. 893-915.
25. Xiao S., Yan H., Yao P. The efficacy of cerebrolysin in patients with vascular dementia: results of a Chinese multicentre, randomised, double-blind, placebo-controlled trial. The Cerebrolysin Study Group // J. Psychiatry. — 1999. — V. 9, № 2. — P. 13-19.
26. Muresanu D.F., Alvarez X.A., Moessler H. et al. A pilot study to evaluate the effects of Cerebrolysin on cognition and qEEG in vascular dementia: cognitive improvement correlates with qEEG acceleration // J. Neurol. Sci. — 2008. — V. 267, № 1–2. — P. 112-119.
27. Muresanu D.F., Alvarez X.A., Moessler H. et al. Persistence of the effects of Cerebrolysin on cognition and qEEG slowing in vascular dementia patients: results of a 3-month extension study // J. Neurol. Sci. — 2010. — V. 299, № 1–2. — P. 179-183.
28. Rainer M., Brunnbauer M., Dunky A. et al. Therapeutic results with Cerebrolysin in the treatment of dementia // Wien. Med. Wochenschr. — 1997. — V. 147, № 18. — P. 426-431.
