Газета «Новости медицины и фармации» Кардиология (338) 2010 (тематический номер)
Вернуться к номеру
Серцева недостатність із збереженою фракцією викиду лівого шлуночка
Авторы: О.Й. Жарінов, д.м.н., професор, Національна медична академія післядипломної освіти, ім. П.Л. Шупика МОЗ України, кафедра кардіології і функціональної діагностики
Версия для печати
Серцева недостатність (СН) — клінічний синдром, що характеризується поєднанням ознак дисфункції лівого шлуночка (ЛШ), затримки в організмі рідини та зниження толерантності до фізичного навантаження. Спочатку поняття дисфункції ЛШ асоціювали лише з погіршенням насосної спроможності міокарда та зниженням фракції викиду (ФВ) ЛШ. Але в 1980–1990-х роках увагу клініцистів та дослідників привернули розлади діастолічного наповнення ЛШ, їх взаємозв’язок із систолічною дисфункцією міокарда, а також регіонарні порушення його скоротливої функції. Було встановлено, що СН не обов’язково спричиняється систолічною дисфункцією ЛШ. Приблизно в 40–50 % хворих діагностують СН із збереженою систолічною функцією серця (ФВ ЛШ ≥ 45 %). Особливо часто цей патогенетичний варіант СН діагностують у пацієнтів з артеріальною гіпертензією (АГ), цукровим діабетом, а також у похилому і старечому віці. З огляду на старіння популяції, а також постійне збільшення поширеності АГ і діабету очікується, що частка пацієнтів із СН зі збереженою ФВ ЛШ зростатиме протягом найближчих десятиліть [11].
Наголосимо, що більшість контрольованих досліджень, результати яких стали основою для стандартизованого «синдромного» лікування СН, були здійснені у пацієнтів з низькою ФВ ЛШ. Відтак, діючі узгоджені рекомендації можуть бути переважно використані для ведення пацієнтів із систолічною дисфункцією ЛШ. Натомість стандарти лікування хворих із CH і збереженою ФВ ЛШ являють собою лише загальні положення, що переважно базуються на думці експертів [10]. Причина цього полягає у невизначеності, «розмитості» критеріїв діагностики діастолічної дисфункції ЛШ і «діастолічної СН», відсутності доказів ефективності досліджених засобів лікування за «жорсткими» кінцевими точками. Мета цієї публікації — узагальнити сучасні критерії діагностики, особливості ведення хворих та лікування СН зi збереженою ФВ ЛШ.
Патогенетичні механізми
Очевидно, провідним патогенетичним чинником виникнення СН зі збереженою ФВ ЛШ є дiастолiчна дисфункцiя ЛШ. Її визначають як неможливiсть наповнення ЛШ без додаткового пiдвищення тиску в лiвому передсердi. Провідні механізми діастолічної дисфункції — порушення процесів pозслаблення (на початку діастоли) або підвищення жорсткості міокарда (здебільшого у другій половині діастоли). Внаслідок цих змін зростає передсердний тиск, з’являються ознаки легеневого чи системного венозного застою. Отже, домінує «недостатність входу крові» (backward failure). Вважають, що прогноз виживання пацієнтів із діастолічною СН не такий тяжкий, як при систолічній дисфункції ЛШ, за винятком хворих з інфільтративним ураженням міокарда. Перебіг захворювання і смертність передусім залежать від ступеня вираженості СН: незалежно вiд показника ФВ ЛШ поява легеневого застою пiсля інфаркту міокарда погipшує перспективи виживання хворих. Але частота госпіталізації з приводу СН зі збереженою ФВ ЛШ не менша, ніж у хворих зі зниженою ФВ ЛШ. З огляду на припущення про важливість діастолічної дисфункції СН зі збереженою ФВ ЛШ нерідко позначають як «діастолічну СН». Але вказані терміни не можна вважати синонімами, оскільки не в усіх випадках СН зі збереженою ФВ ЛШ наявні ознаки порушення діастолічної функції ЛШ. Тому з практичних міркувань передусім важливо розрізняти СН з порушеною (< 45 %) і збереженою (≥ 45 %) ФВ ЛШ.
Патогенез і клінічні ознаки систолічної та діастолічної СН мають чимало спільного. Переважно можна говорити не про ізольовану систолічну чи діастолічну СН, а про переважання порушень систоли чи діастоли. «Недостатність виходу крові» (forward failure) нерідко зумовлює «недостатність входу», тобто порушення скоротливої функцiї міокарда спричинюють підвищення тиску наповнення ЛШ і діастолічну СН. Водночас ізольована діастолічна дисфункція «жорсткого» міокарда ЛШ може зумовити зниження серцевого викиду під час фізичного навантаження, оскільки на фоні тахікардії значно скорочується тривалість періоду діастолічного наповнення серця. Швидке прогресування СН особливо характерне для пацієнтів з обструктивною гіпертрофічною кардіоміопатією, у випадках виникнення пароксизму фібриляції передсердь (ФП). Оскільки наповнення ЛШ переважно відбувається за рахунок систоли передсердь, її втрата на фоні пароксизму ФП може призвести до швидкої декомпенсації кровообігу, незважаючи на відсутність порушень насосної функції серця.
У багатьох хворих із СН діагностують поєднаний варіант СН, коли поєднуються ознаки порушення систолічної і діастолічної функції серця, а «недостатність виходу» виникає і прогресує паралельно з «недостатністю входу».
Розлади діастолічної функції ЛШ найчастіше спричинені ішемією, гіпертрофією та фіброзом міокарда. Невідповідність потреби та постачання енергії у хворих на ІХС зумовлює насамперед уповільнення розслаблення, а фіброз — підвищення жорсткості міокарда; гіпертрофія ЛШ спричинює включення обох основних патогенетичних механізмів діастолічної дисфункції. До так званих «хвороб діастоли» зараховують гiпеpтpофiчну та pестpиктивну каpдiомiопатiї, уpаження мiокаpда пpи цукpовому дiабетi, АГ, аоpтальному стенозi, фiбpозi мiокаpда, в осіб похилого та старечого віку. У багатьох пацієнтів із АГ та ІХС поява ознак діастолічної дисфункції передує зниженню ФВ ЛШ, їх вважають одними з найчутливіших ранніх маркерів захворювання серця.
Діагностичні критерії
Неінвазивна оцiнка дiастолiчної функцiї ЛШ має iстотнi обмеження. Вона не передбачає безпосереднього вимiрювання тиску в камерах серця, проте саме катетеризація шлуночків з одержанням кривої «тиск — об’єм» є еталонним методом дослідження діастоли серця. Передусім доцільно визначити ознаки, характерні для діастолічної дисфункції ЛШ. Виявлення у хвоpих із задишкою та iншими симптомами СН збереженої ФВ ЛШ і pентгенологiчних ознак легеневої венозної гiпеpтензiї дає пiдстави припустити наявність діастолічної дисфункції ЛШ. Нерідко зустрічаються ожирiння, IV тон серця, підвищення дiастолiчного артеріального тиску понад 105 мм рт.ст.; у цих хворих звичайно немає набухання шийних вен. При ехокардiографiчному дослідженні часто виявляють поєднання гiпертрофiї ЛШ з дилатацiєю лiвого передсердя. Доплер-ехокардiографiчне дослідження потоку крові через мітральний клапан — достатньо простий неiнвазивний метод динамічної оцiнки дiастолiчної функцiї ЛШ. Проте при оцiнці iндексiв дiастолiчного наповнення потрібно зважати на вiк хворих, частоту скорочень серця, насосну функцію ЛШ, стан перед- і післянавантаження, ступінь мiтральної регургiтацiї. Раннiми ознаками ураження мiокарда при ІХС і АГ є змiни показникiв розслаблення та зменшення градiєнту тиску мiж лiвими вiддiлами серця, що проявляється подовженням часу сповiльнення i зниженням першого пiку трансмітрального потоку, зниженням співвідношення амплітуд Е/А < 1. Чутлива, але недостатньо специфічна ознака порушення «люзитропної» функції серця — збільшення періоду iзоволюмiчного розслаблення ЛШ. Обмеженням для доплер-ехокардiографiчного дослiдження діастолічної функції ЛШ є ФП. Зазначимо також, що однією з ключових передумов коректної діагностики СН зі збереженою ФВ ЛШ є правильна оцінка показника фракції викиду, особливо в пацієнтів із регіонарними порушеннями скоротливості ЛШ або мітральною регургітацією.
У консенсусі експертів Європейського товариства кардіологів визначення діастолічної СН базується на поєднанні ознак і симптомів СН, збереженої ФВ ЛШ (40–50 %), ехокардіографічних ознаках діастолічної дисфункції, а також підвищенні рівня натрійуретичних пептидів (рис. 1) [7]. Причому для оцінки тиску наповнення ЛШ ключовим параметром є співвідношення амплітуд першого піку трансмітрального потоку і піку раннього наповнення ЛШ, оціненого методом тканинної доплерографії. Перевірка наведеного алгоритму виявила, зокрема, високу інформативність індексу об’єму лівого передсердя [3].
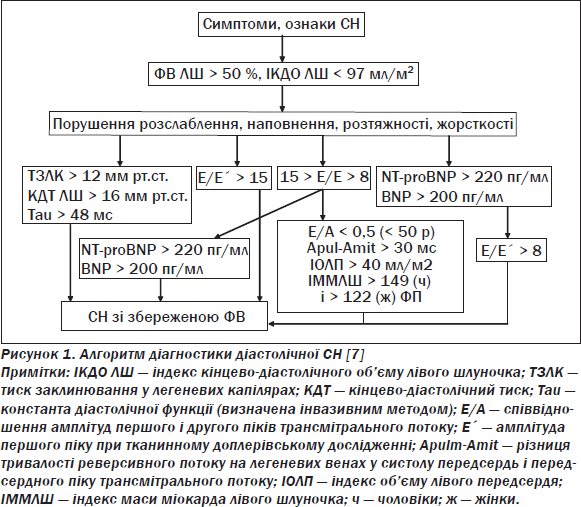
Принципи ведення хворих
Єдиної стратегії лікування хворих із СН на фоні збереженої ФВ ЛШ поки що не розроблено. Передусім це пов’язано з труднощами систематичної верифікації діагнозу «діастолічної» СН, а відтак з обмеженою кількістю контрольованих досліджень, здійснених у вказаної категорії хворих. На відміну від «систолічного» варіанту СН, при якому лікування є переважно синдромним, у хворих із збереженою ФВ ЛШ терапевтичні підходи більше залежать від провідного етіологічного фактору. Очевидно, терапевтична тактика може мати істотні відмінності у хворих із СН на фоні гіпертрофічної кардіоміопатії, АГ та ішемічною хворобою серця. З іншого боку, не існує препаратів з винятково «люзитропними» властивостями, що б вибірково поліпшували розслаблення міокарда, не погіршуючи його скоротливість і стан периферичного кровообігу. Крім того, у деяких випадках розлади діастолічної функції ЛШ взагалі не піддаються медикаментозній корекції, оскільки спричинені незворотним фіброзом або інфільтрацією міокарда.
З огляду на механізми формування СН у хворих зі збереженою ФВ ЛШ для усунення клінічних симптомів потрібно зменшити тиск наповнення ЛШ і прояви «недостатності входу» при збереженні серцевого викиду (табл. 1). Утім, не всі теоретичні припущення можна безпосередньо перенести на клінічну практику. Але основна проблема формування узгоджених терапевтичних підходів полягає у відсутності доказів того, що певний препарат здатний покращити прогноз виживання хворих із СН на фоні збереженої ФВ ЛШ.
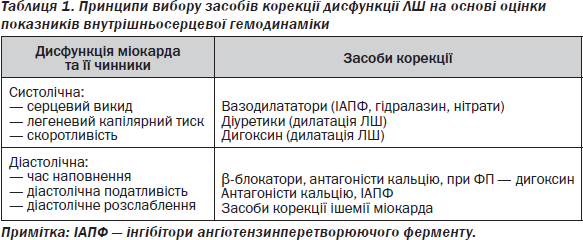
Корисними в пацієнтів із СН і збереженою ФВ ЛШ можуть бути кілька груп медикаментозних засобів, що застосовуються також при «систолічному» варіанті СН. Насамперед це діуретики, які зменшують об’ємне перевантаження і клінічні прояви у пацієнтів із симптомами. Препарати для зменшення частоти серцевих скорочень і негативні інотропні засоби (антагоністи кальцію «міокардіального» типу, бета-адреноблокатори, івабрадин) збільшують тривалість періоду наповнення лівого шлуночка і здатні покращувати розслаблення міокарда. Щоправда, верапаміл і дилтіазем протипоказані пацієнтам з тяжкою застійною СН, а доказова база щодо застосування івабрадину у хворих із СН на фоні збереженої ФВ ЛШ поки що недостатня. Можна також припускати, що будь-який антигіпертензивний засіб забезпечить зменшення гіпертрофії лівого шлуночка і, таким чином, покращить розслаблення міокарда. Причому додаткові переваги можуть мати блокатори ренін-ангіотензинової системи: ІАПФ, блокатори рецепторів ангіотензину ІІ і антагоністи альдостерону. Ці препарати здатні зменшувати перед- і післянавантаження, забезпечувати регресування гіпертрофії лівого шлуночка, запобігати накопиченню інтерстиціального колагену та фіброзуванню міокарда. Для оцінки можливостей поліпшення прогнозу виживання хворих і модифікації перебігу СН із збереженою ФВ ЛШ на фоні застосування блокаторів ренін-ангіотензинової системи останнім часом здійснено ряд контрольованих досліджень.
У найбільшому за обсягом дослідженні CHARM-Preserved застосування препарату з групи блокаторів рецепторів ангіотензину ІІ кандесартан не зменшило сумарної кількості випадків смерті від серцево-судинних причин і госпіталізацій внаслідок СН у 3024 пацієнтів із СН і ФВ понад 40 %, але зменшило частоту госпіталізацій, зумовлених декомпенсацією кровообігу [13]. Варто зазначити, що критерієм включення в це дослідження було поєднання ФВ понад 40 % і госпіталізації будь-якої давності з огляду на захворювання серця. Хоча дослідники реєстрували в пацієнтів ознаки і симптоми СН, такі «розмиті» критерії включення могли призвести до включення значної кількості пацієнтів з іншими станами. У підсумку в 33 % учасників ехокардіографічної частини програми CHARM-Preserved не було виявлено ознак діастолічної дисфункції ЛШ [8].
У дослідженні PEP-CHF вживання препарату з групи ІАПФ периндоприлу не зменшило сумарної кількості випадків смерті або госпіталізацій внаслідок СН у пацієнтів із СН і ФВ понад 40 % протягом усього періоду дослідження. Суттєво вплинути на результат цього дослідження могло те, що багато пацієнтів припинили прийом досліджуваного препарату і перейшли на відкрите застосування ІАПФ. На користь цього припущення свідчило зменшення кількості первинних виходів протягом першого року після початку лікування [2].
У дослідженні VALIDD пацієнти з АГ і ознаками діастолічної дисфункції ЛШ були рандомізовані для прийому валсартану або плацебо [9]. Через 9 місяців після початку лікування рівень артеріального тиску подібно знизився, а діастолічна функція покращилася в обох групах. Втім, у цьому дослідженні спеціально не аналізували результати лікування хворих із діастолічною СН.
Спроба подолати недоліки попередніх досліджень була нещодавно здійснена у Гонконгзькому дослідженні діастолічної СН [12]. У цьому відкритому дослідженні з осліпленою оцінкою кінцевих точок 150 пацієнтів із діастолічною СН і ФВ понад 45 % були рандомізовані для монотерапії діуретиками, комбінацій діуретиків з ірбесартаном 75 мг або раміприлом 10 мг на добу. Показники діастолічної функції, оцінені за трансмітральним потоком і тканинним доплерівським методом, були суттєво гірші за такі в контрольній групі. Через рік зниження АТ у клінічних групах вірогідно не відрізнялось. Не спостерігали відмінностей між групами щодо якості життя, показників тесту з 6-хвилинною ходьбою, а також параметрів діастолічної функції лівого шлуночка.
У 2009 році були оприлюднені результати дослідження ефективності ірбесартану у пацієнтів із СН і збереженою систолічною функцією лівого шлуночка (I-PRESERVE). У ньому 4133 пацієнти були рандомізовані для прийому ірбесартану 300 мг або плацебо. Оцінювали можливість зменшення сумарної кількості випадків смерті та госпіталізацій з серцево-судинних причин [5]. Цікаво, що вихідні характеристики пацієнтів у цьому дослідженні (середній вік 72 роки, 60 % жінок, 88 % — з гіпертензією) значно краще відображали реальні характеристики пацієнтів із діастолічною СН, ніж у дослідженні CHARM-Preserved (середній вік 67 років, 40 % жінок, 64 % — з гіпертензією). Втім, застосування ірбесартану протягом понад 4 років не вплинуло на первинну кінцеву точку — сумарну кількість випадків смерті і госпіталізацій з серцево-судинних причин [4].
У здійснюваному Національним інститутом серця, легень і крові дослідженні ТОРСАТ 4500 пацієнтів із діастолічною СН будуть рандомізовані для прийому спіронолактону 45 мг на добу або плацебо [6]. Крім того, кілька нових препаратів оцінюються у менших за обсягом дослідженнях із сурогатними кінцевими точками. Це, зокрема, еплеренон, спіронолактон, антагоніст ендотеліну ситаксентан, несиритид, валсартан, ранолазин, алопуринол і еритропоетин-альфа [11].
У рекомендаціях Робочої групи з серцевої недостатності Асоціації кардіологів України [1] вказано, що з огляду на різноманітність етіологічних факторів не може існувати єдиного стандарту лікування СН зі збереженою ФВ ЛШ. Ведення хворих обов’язково повинно передбачати адекватний вплив (фармакологічний або хірургічний) на основне захворювання, а також медикаментозну корекцію симптомів та циркуляторних порушень, притаманних СН.
Лікування хворих з діастолічною СН, які складають більшість серед пацієнтів із СН і збереженою ФВ ЛШ, передбачає:
— Зниження рівня артеріального тиску до цільового рівня (засоби першої лінії — ІАПФ або блокатори рецепторів ангіотензину ІІ). У випадку призначення ІАПФ або сартанів пацієнтам із СН і збереженою ФВ ЛШ доцільно враховувати існуючі докази щодо поліпшення перебігу і прогнозу захворювання на фоні тривалого прийому кандесартану, а також периндоприлу.
— Адекватний контроль частоти скорочень шлуночків у хворих з постійною формою ФП (за непереносимості бета-адреноблокаторів можливе застосування верапамілу або дилтіазему) або усунення синусової тахікардії.
— Коли це можливо — відновлення синусового ритму у хворих із ФП.
— Медикаментозне лікування ІХС відповідно до діючих рекомендацій; за наявності показань — реваскуляризація міокарда.
— Контроль волемічного стану за допомогою діуретиків.
Підсумки
Провідним патогенетичним чинником виникнення СН із збереженою ФВ ЛШ є дiастолiчна дисфункцiя ЛШ. Розлади діастолічної функції ЛШ найчастіше спричинені ішемією, гіпертрофією та фіброзом міокарда. Сучасна діагностика діастолічної СН базується на поєднанні ознак і симптомів СН, збереженої ФВ ЛШ (не менше 45–50 %), ехокардіографічних ознак діастолічної дисфункції, оцінених за показниками трансмітрального потоку і тканинної доплерографії, а також підвищеного рівня натрійуретичних пептидів. На відміну від «систолічного» варіанту СН, при якому лікування є переважно синдромним, у хворих із збереженою ФВ ЛШ терапевтичні підходи більшою мірою залежать від провідного етіологічного фактора. Ведення хворих повинно поєднувати адекватний вплив (фармакологічний або хірургічний) на основне захворювання, а також медикаментозну корекцію симптомів та циркуляторних порушень, притаманних СН. Докази здатності модифікувати перебіг СН із збереженою ФВ ЛШ переважно отримані у дослідженнях із застосуванням ІАПФ і блокаторів рецепторів ангіотензину ІІ.
1. Рекомендації Асоціації кардіологів України з діагностики, лікування та профілактики хронічної серцевої недостатності у дорослих (2009). — Київ, 2009. — 22 с.
2. Cleland J.G., Tendera M., Adamus J. et al. PEP-CHF Investigators. The Perindopril in Elderly People with Chronic Heart Failure (PEP-CHF) study // Eur. Heart. J. — 2006. — 27. — 2338-45.
3. Emery W.T., Jadavji I., Choy J.B., Lawrance R.A. Investigating the European Society of Cardiology Diastology Guidelines in a practical scenario // Europ. J. Echocard. — 2008. — 9. — 685-691.
4. Massie B.M., Carson P.E., McMurray J.J. et al. Irbesartan in patients with heart failure and preserved ejection fraction // New. Engl. J. Med. — 2008. — 359. — 2456-2467.
5. McMurray J.J., Carson P.E., Komajda M. et al. Heart failure with preserved ejection fraction: clinical characteristics of 4133 patients enrolled in the I-PRESERVE trial // Eur. J. Heart Fail. — 2008. — 10. — 149-56.
6. National Heart, Lung, and Blood Institute (NHLBI). Trial of aldosterone antagonist therapy in adults with preserved ejection fraction congestive heart failure (TOPCAT). Доступно на веб-сайті: http:\www.clinicaltrials.gov/ct2/show/NCT0094302?term=topcat&rank=1
7. Paulus W.J., Tschope C., Sanderson J.E. et al. How to diagnose diastolic heart failure: a consensus statement on the diagnosis of heart failure with normal left ventricular ejection fraction by the Heart Failure and Echocardiography Associations of the European Society of Cardiology // Eur. Heart. J. — 2007. — 28. — 2539-50.
8. Persson H., Lonn E., Edner M. et al. Investigators of the CHARM Echocardiographic Substudy — CHARMES. Diastolic dysfunction in heart failure with preserved systolic function: need for objective evidence: results from the CHARM Echocardiographic Substudy — CHARMES // J. Am. Coll. Cardiol. — 2007. — 49. — 687-94.
9. Solomon S.D., Janardhanan R., Verma A. et al. Valsartan In Diastolic Dysfunction (VALIDD) Investigators. Effect of angiotensin receptor blockade and antihypertensive drugs on diastolic function in patients with hypertension and diastolic dysfunction: a randomised trial // Lancet. — 2007. — 369. — 2079-87.
10. The Task Force for the diagnosis and treatment of acute and chronic heart failure 2008 of the European Society of Cardiology. Guidelines for the diagnosis and treatment of acute and chronic heart failure 2008 // Europ. Heart. J. — 2008. — 29. — 2388-2442.
11. Voors A.A., de Jong R.M. Treating diastolic heart failure // Heart. — 2008. — 94. — 971-972.
12. Yip G.W.K., Wang M., Wang T. et al. The Hong Kong diastolic heart failure study: a randomised controlled trial of diuretics, irbesartan and ramipril on quality of life, exercise capacity, left ventricular global and regional function in heart failure with a normal ejection fraction // Heart. — 2008. — 94. — 573-80.
13. Yusuf S., Pfeffer M.A., Swedberg K. et al. CHARM Investigators and Committees. Effects of candesartan in patients with chronic heart failure and preserved left-ventricular ejection fraction: the CHARM-Preserved Trial // Lancet. — 2003. — 362. — 777-81.
