Международный неврологический журнал 4 (42) 2011
Вернуться к номеру
Результати хірургічного лікування невропатичного больового синдрому у хворих із наслідками травматичного ушкодження спинного мозку
Авторы: Цимбалюк В.І., Ямінський Ю.Я., Інститут нейрохірургії ім. акад. А.П. Ромоданова АМН України, м. Київ
Рубрики: Неврология
Версия для печати
У статті наведено результати хірургічного лікування невропатичного больового синдрому у 38 хворих із наслідками травми спинного мозку та його корінців. Хворих було розподілено на групи залежно від рівня ушкодження спинного мозку (шийні сегменти — 10 хворих, грудні — 12, поперекові — 16) та характеру поширення болю (сегментарний — 18 хворих, дифузний — 13, корінцевий — 7). Епідуральна електростимуляція виявилась ефективною у 76,9 % хворих, DREZ-томія — у 90,9 %, симпатектомія та передня комісуральна мієлотомія — у 100 % хворих.
Таким чином, диференційований підхід у виборі методу хірургічного лікування невропатичного болю дозволяє значно покращити результати лікування.
Невропатичний біль, хірургічне лікування, травма спинного мозку.
Поряд із руховими порушеннями та дисфункцією сечового міхура невропатичний больовий синдром є одним із важливих чинників, що визначають якість життя хворих з наслідками травматичного ушкодження спинного мозку. За даними різних авторів [1, 2], невропатичний больовий синдром супроводжує травматичну хворобу спинного мозку у 15–17 % пацієнтів. Хірургічному лікуванню підлягають лише ті випадки невропатичного болю, що не піддаються консервативній терапії.
Усі протибольові операції можна розділити на деструктивні та недеструктивні [1, 2, 10]. До деструктивних втручань належать [11–14]: операція деструкції зони входження задніх корінців у спинний мозок (DREZ-томія), задня радикотомія, симпатектомія, передня комісуральна мієлотомія, передньобокова хордотомія та цингулотомія. До недеструктивних [8–10] зараховують епідуральну електростимуляцію спинного мозку, стимуляцію глибинних структур головного мозку та коркову стимуляцію. Від правильного вибору методу хірургічного втручання значною мірою залежить результат лікування.
У нашій роботі ми прагнули поділитися власним досвідом лікування невропатичних больових синдромів спінального генезу.
Методи та матеріали
Наше дослідження ґрунтується на аналізі результатів хірургічного лікування 38 хворих із наслідками травматичного ушкодження спинного мозку та невропатичним больовим синдромом, оперованих у клініці відновлювальної хірургії Інституту нейрохірургії за період з 2002 по 2010 рік.
Серед хворих переважали чоловіки — 35, жінок було 3. Вік хворих коливався від 21 до 49 років (у середньому — 32,8 року).
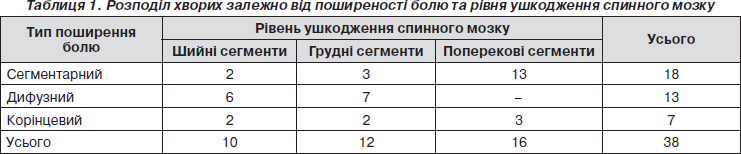
За рівнем ушкодження спинного мозку хворі розподілилися таким чином (табл. 1): у 10 було ушкодження шийних сегментів, у 12 — грудних та у 16 — поперекових сегментів, конусу та епіконусу спинного мозку. Тяжкість травми оцінювали за шкалою ASIA: А — повна відсутність рухів і чутливості дистальніше місця травми і в сегментах S4–S5 — 16 хворих; В — повністю або частково збережена чутливість, але відсутні рухи дистальніше місця травми, включаючи сегменти S4–S5, — 7 хворих; С — частково збережені рухи і чутливість, але більше ніж половина ключових м’язів нижче місця ушкодження мають силу менше за 3 бали — 14 хворих; Д — збережені рухи та чутливість, більше ніж половини ключових м’язів нижче рівня ушкодження мають силу 3 бали і більше — 1 хворий; Е — нормальні рухи і чутливість. Хворих групи Е в нашому дослідженні не було.
Для оцінки болю використовували VAS (visual analog scale) та NRS, згідно з якою хворий сам оцінював інтенсивність болю за 10-бальною шкалою. Залежно від інтенсивності виділяли: помірний біль — 1–3 бали, середній біль — 4–6 балів та сильний біль — 7–10 балів. Хірургічному лікуванню підлягали лише хворі з сильним болем.
За поширеністю розрізняли сегментарний біль, що охоплював лише ті сегменти тіла, які відповідали ушкодженим сегментам спинного мозку; дифузний біль, що охоплював всі сегменти тіла, які знаходилися каудальніше рівня ушкодження, та корінцевий біль, що охоплював зону іннервації одного або декількох корінців (як правило, з одного боку). Розподіл хворих залежно від типу поширення болю та виду патології спинного мозку наведено в табл. 1. У більшості хворих у нашому дослідженні переважав сегментарний характер поширення болю. Такий характер поширення болю був у 18 (47,4 %) хворих, причому у 13 з них було ушкодження поперекових сегментів спинного мозку або корінців кінського хвоста. Дифузний характер поширення болю був у 13 (34,2 %) хворих. Цей тип поширення болю переважав у хворих з ушкодженням шийних та грудних сегментів спинного мозку. Корінцевий тип поширення болю був у 7 (18,4 %) хворих.
Показаннями до застосування хірургічних методів корекції болю в нашому дослідженні були: болі невропатичного характеру, резистентні до адекватного консервативного лікування; біль інтенсивністю більше 6 балів за шкалою NRS; відсутність грубих психічних порушень у хворих; відсутність тяжкої наркотичної залежності; соматичний стан хворого, що дозволяє проведення хірургічних втручань під загальною анестезією.
Нами застосовано такі хірургічні протибольові методики: операції встановлення електродів для епідуральної електростимуляції спинного мозку проведено 26 (68,4 %) хворим, DREZ-томії — 11 (28,9 %) хворим. Операцію передньої комісуральної мієлотомії виконано 2 хворим після неефективного застосування епідуральної електростимуляції. Операцію грудної симпатектомії виконано 3 хворим з «симпатичним» характером болю. У 2 із них попередньо застосовували епідуральну електростимуляцію з поганим результатом.
Операцію встановлення електродів для електростимуляції проводили з виконанням ламінектомії або з міждужкового доступу. Електроди встановлювали на 1–2 сегменти краніальніше місця ушкодження спинного мозку (за даними неврологічного дослідження до операції та інтраопераційної електродіагностики під час операції) в проекції задніх стовпів спинного мозку. Електростимуляцію спинного мозку проводили в поздовжньому напрямку.
Для електростимуляції спинного мозку використовували радіочастотний електростимулятор, що складається з 2 частин: електродів із прийомною антеною, що імплантуються в тіло хворого під час операції, та власне електростимулятора, за допомогою якого проводиться стимуляція в післяопераційному періоді. Ми використовували прилад, створений сумісно співробітниками Інституту нейрохірургії та інженерами наукової лабораторії київського заводу «Квазар-мікро». Електростимуляцію проводили змінним струмом частотою 25 Гц напругою 13 Вт та силою струму 20 мА.
Операцію DREZ-томії виконували із заднього доступу. Проводили ламінектомію кількох хребців на рівні ушкодження спинного мозку. Поздовж розсікали тверду мозкову оболонку. Роз’єднували арахноїдальні злуки та ідентифікували зону входження задніх корінців у спинний мозок. Далі проводили інтраопераційну електродіагностику для ідентифікації корінців спинного мозку, що відповідають за іннервацію зони поширення невропатичного болю. Зону входження задніх корінців у спинний мозок пересікали на глибину 2–3 мм під кутом 45° до серединної лінії. Кровотечу з країв мієлотомної рани зупиняли за допомогою мікрокоагуляції.
Передню комісуральну мієлотомію виконано 2 хворим. Операцію виконували із заднього доступу шляхом проведення ламінектомії 3 хребців на 2–3 сегменти вище місця ушкодження спинного мозку. Розсікали тверду мозкову оболонку. За допомогою інтраопераційної електродіагностики ідентифікували рівень відкритого сегмента спинного мозку. Із застосуванням мікрохірургічної техніки та операційного мікроскопу відпрепаровували і відводили в бік судини задньої щілини спинного мозку, при цьому коагулювали радіарні вени, що йдуть у глибину задньої щілини. Строго по середній лінії проводили мієлотомію, проникаючи в центральний спинномозковий канал. Передньою стінкою цього каналу є передня сіра спайка. Її пересікали на глибину близько 2–3 мм. Рану герметизували за загальноприйнятою методикою.
Симпатектомію виконано 3 хворим з вираженим «симпатичним» компонентом больового синдрому. Для верифікації симпатичного характеру болю проводили новокаїнові блокади відповідних симпатичних гангліїв. Обом хворим виконали резекцію верхніх грудних гангліїв. Операцію виконували з міжлопаткового доступу. Проводили резекцію поперечних відростків Th1–Th3 хребців, головок і проксимальних частин 1–3 ребер. Парієтальну плевру відсепаровували і відводили латерально. При цьому на передньобоковій поверхні хребців у паравертебральній жировій клітковині виявляли верхні грудні ганглії і симпатичний стовбур. Якомога вище і нижче гангліїв пересікали симпатичний стовбур. Пересікали комунікантні гілки і видаляли симпатичні ганглії з частиною стовбура одним блоком.
Результати лікування оцінювали як відмінні, якщо після операції біль зменшувався більше ніж на 75 %, хороші — на 50–75 %, задовільні — на 35–50 % та погані — менше ніж на 35 %.
Результати
Нами проведено аналіз результатів хірургічного лікування невропатичних больових синдромів залежно від рівня ушкодження спинного мозку та типу поширення болю.
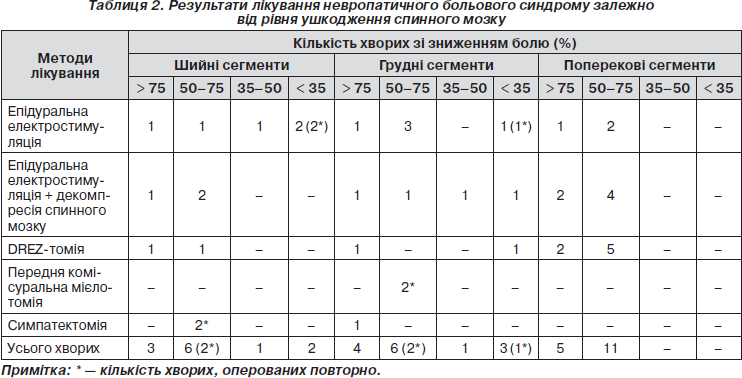
У хворих із наслідками травматичного ушкодження шийних сегментів спинного мозку метод епідуральної електростимуляції нами застосовано у 8 хворих (табл. 2). У 3 із них встановлення електродів супроводжувалося декомпресивними хірургічними втручаннями. У перші 2–3 доби після операції (поки не було почато застосування епідуральної електростимуляції) у всіх цих хворих зберігався больовий синдром на післяопераційному рівні або на 10–20 % меншої інтенсивності. Це свідчить про те, що лише усунення компресії спинного мозку та його корінців є неефективним для лікування невропатичного болю. При застосуванні епідуральної електростимуляції в цій групі хворих відмінного результату вдалось досягти у 2 хворих, хорошого — у 3 хворих, задовільного — в 1 хворого. У 2 хворих не отримали покращення. Ці хворі були прооперовані повторно: проведена грудна симпатектомія з хорошим результатом. У 2 хворих з ушкодженням шийних сегментів спинного мозку проведено шийну DREZ-томію з відмінним та хорошим результатами.
У хворих із ушкодженням грудних сегментів спинного мозку епідуральна електростимуляція застосована у 9 хворих з больовим синдромом. У 4 із них встановлення електростимулюючої системи супроводжувалося декомпресивними хірургічними втручаннями на хребті. Відмінний результат корекції больового синдрому при застосуванні електростимуляції отримано у 2 хворих, хороший — у 4 хворих, задовільний — в 1 хворого. У 2 хворих епідуральна стимуляція виявилася неефективною. Один із них оперований повторно: проведена передня комісуральна мієлотомія з хорошим результатом. Двом хворим з ушкодженням грудних сегментів спинного мозку проведена DREZ-томія. В одного з них больовий синдром регресував повністю, у другого біль залишився на доопераційному рівні. Цьому хворому проведена передня комісуральна мієлотомія з хорошим результатом. Одному хворому з ушкодженням верхньогрудних сегментів спинного мозку та корінцевим поширенням болю проведена грудна симпатектомія з відмінним результатом.
У хворих із наслідками ушкодження поперекових сегментів спинного мозку та корінців кінського хвоста метод епідуральної електростимуляції застосовували у 9 хворих. В усіх цих хворих досягнуто хороших та відмінних результатів корекції больового синдрому. У 7 хворих цієї групи виконана поперекова DREZ-томія. У 2 хворих вона дозволила досягти відмінного і у 5 хворих — хорошого результату.
Таким чином, найкращі результати корекції невропатичного больового синдрому отримано у хворих з ушкодженням поперекових сегментів спинного мозку. У цій групі в усіх хворих вдалося досягти хороших і відмінних результатів. У хворих з ушкодженням шийних і грудних сегментів спинного мозку хірургічні методи корекції больового синдрому були ефективними в 75 % випадків.
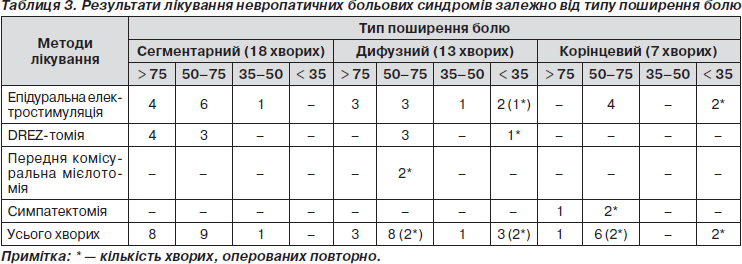
Одним із важливих факторів, що впливав на вибір методу хірургічного лікування та його результат, був характер поширення болю. Результати хірургічного лікування больового синдрому залежно від характеру поширеності болю наведено в табл. 3. Найкращими результати лікування були у хворих із сегментарним поширенням болю. У 17 хворих з 18 вдалося досягти хорошого та відмінного результатів: при застосуванні епідуральної електростимуляції — у 10 хворих з 11 та після DREZ-томії — у 7 хворих.
У хворих із дифузним поширенням болю результати хірургічного лікування були гіршими. В цій групі хворих операцією вибору було встановлення електродів для епідуральної електростимуляції спинного мозку. Метод епідуральної електростимуляції застосовано нами у 9 (69,2 %) хворих із дифузним болем. У 6 хворих досягнуто позитивного результату корекції больового синдрому. В 1 хворого біль зменшився лише на 40 %, а ще у 2 хворих не отримано позитивного результату лікування. Одному з цих хворих проведено передню комісуральну мієлотомію, що дало хороший результат. DREZ-томія виконана 4 хворим з дифузним поширенням болю. У 3 із них отримано позитивний результат. В одного хворого з поганим результатом проведена передня комісуральна мієлотомія, що дозволило зменшити больовий синдром на 60 %.
У 6 хворих із 7 з корінцевим поширенням болю застосовували метод епідуральної електростимуляції. У 4 із них отримано хороший результат, у 2 хворих біль не змінився. Останнім проведена симпатектомія з хорошим результатом. Ще в 1 хворого з корінцевим больовим синдромом виконано грудну симпатектомію з відмінним результатом.
Обговорення
Лікування невропатичних больових синдромів є однією з найскладніших проблем сучасної неврології та нейрохірургії. Тривале неефективне консервативне лікування призводить до виникнення емоційних та психічних порушень у хворих із больовими синдромами, що в подальшому нівелює або погіршує результати хірургічних протибольових операцій [2].
Більшість методик протибольових операцій ґрунтується на деструкції тих чи інших нервових структур. Перші протибольові операції проведені в 1889 році Abbe і Bennett [1]. Ці нейрохірурги, ґрунтуючись на роботах Magendie (який встановив, що чутливі волокна входять у спинний мозок через задні корінці), незалежно один від одного виконали першу задню радикотомію. В 1912 році Martin уперше виконав спіноталамічну хордотомію [1]. У 1940 році Leriche створив концепцію «хірургії болю» і впровадив у клінічну практику широке застосування симпатектомії [6]. Тоді ж Wertheimer запровадив операцію передньої комісуротомії [14]. Таким чином, слідом за новими відкриттями в анатомії і фізіології розвивалися різні методи хірургічного лікування болю. Революційним для сучасної хірургії болю було відкриття в 1965 році Melzach і Wall «ворітної теорії» болю. Більшість сучасних протибольових операцій ґрунтується саме на цій теорії. Melzach та Wall [7] виявили в спинному мозку на рівні задніх рогів зону, що контролює ноцицептивні імпульси. Ноцицептивні імпульси контролюються на сегментарному рівні волокнами великого діаметра Аb (вони відповідають за тактильну і пропріоцептивну чутливість) [4, 5]. Ці волокна посилають свої колатералі до нейронів задніх рогів і йдуть у складі задніх канатиків спинного мозку. Електростимуляція задніх канатиків спинного мозку викликає активацію інгібіторних систем болю в задніх рогах спинного мозку та закриття больових «воріт» [3]. Таким чином, умовою хорошого результату при застосуванні епідуральної електростимуляції є збереження провідності задніх пучків спинного мозку.
У нашій роботі епідуральну електростимуляцію спинного мозку ми застосовували як при дифузному та сегментарному поширенні болю, так і при корінцевому. Однією з головних умов успішного застосування даного методу лікування було збереження глибоких видів чутливості. Найкращими були результати електростимуляції у хворих з сегментарним поширенням болю. В цій групі у 90,9 % хворих отримано хороший і відмінний результати. В групах із дифузним і корінцевим поширенням болю результати лікування були гіршими: хороший і відмінний результати корекції больового синдрому були у 66,7 % хворих. Повторні протибольові операції у 75 % цих хворих виявились ефективними. Дискутабельним залишається питання застосування епідуральної електростимуляції у хворих, в яких за клінічними даними має місце повне порушення провідності, а за результатами інтраопераційних знахідок виявляється анатомічна цілість спинного мозку. У таких хворих, на нашу думку, спочатку виправдане застосування електростимуляцій, недеструктивних методик і лише при їх неефективності слід застосовувати деструктивні хірургічні втручання.
Операцію DREZ-томії виконували хворим з сегментарним поширенням болю через відсутність у хворих пропріоцептивної чутливості. В нашому дослідженні ефективність операцій DREZ-томії для корекції невропатичного болю була високою: відмінного і хорошого результату досягнуто у 90,9 % хворих.
Операції передньої комісуральної мієлотомії та симпатектомії, на нашу думку, слід віднести до «операцій резерву» у лікуванні невропатичних больових синдромів. Через високу травматичність операції передньої комісуротомії ми застосовували даний метод лікування лише у 2 хворих з параплегіями при неефективності інших методів хірургічного лікування. В обох цих хворих мав місце дифузний характер поширення болю і в обох випадках вдалося досягти хорошого результату.
Симпатектомія — ефективний метод хірургічного лікування невропатичних больових синдромів. Показання до даного виду хірургічних втручань обмежуються болями «симпатичного» характеру з корінцевим або сегментарним поширенням [1]. У нашому дослідженні ми звернулися до методу симпатектомії у 3 хворих із корінцевим поширенням болю, у 2 із них — при неефективності епідуральної електростимуляції спинного мозку. В усіх хворих досягнуто хорошого результату.
Таким чином, диференційований підхід у виборі методу хірургічного лікування невропатичного болю дозволяє значно покращити результати лікування. Застосовуючи його, нам вдалося досягти відмінних та хороших результатів у 81,6 % хворих.
Висновки
1. Диференційований підхід у виборі методу хірургічного лікування дозволяє досягти хороших результатів у лікуванні невропатичних больових синдромів.
2. Епідуральна електростимуляція є методом вибору в лікуванні невропатичних больових синдромів у хворих із наслідками травми спинного мозку та його корінців при частково збережених глибоких видах чутливості.
3. Деструкція зони входження задніх корінців у спинний мозок є високоефективним методом лікування невропатичних больових синдромів у хворих із сегментарним поширенням болю.
1. Cetas J.S. Destructive procedures for the treatment of nonmalignant pain: a structured literature review / Cetas J.S., Saedy T., Burchiel K.J. // Neurosurg. — 2008. — Vol. 109. — P. 389-404.
2. Coffey R.J. Neurostimulation for chronic noncancer pain: an evaluationof the clinical evidenceand recomendatioins for future trial designs / Coffey R.J., Lozano A.M. // J. Neurosurg. — 2006. — Vol. 105. — Р. 175-189.
3. Doleys D.M., Klapow J.C., Hammer M. Psychological evaluation in spinal cord stimulation // Pain Review. — 1997. — Vol. 4. — P. 189-204
4. Doleys D.M. Psychological factors in spinal cord stimulation therapy: brief review and discussion / Doleys D.M. // Neurosurg Focus. — 2006. — Vol. 21. — Е1.
5. Jeanmonod D. Intraoperative unit recordings in human dorsal horn with a simplified floating microelectrode / Jeanmonod D., Sindou M., Marnin M. // Elecroencephalogr. Clin. Neurophysiol. — 1989. — Vol. 72. — P. 450-454.
6. Leriche R. De la traitement de la douleur dans les cancers abdominaux et pelviens inopйrables ou rйcidivйs / Leriche R. // Gaz. Hop. Civils. Milit. — 1936. — P. 109, 917.
7. Melzach R. Pain mechanisms. A new theory / Melzach R., Wall P.D. // Science. — 1964. — Vol. 150. — P. 971-979.
8. Spooner J., Yu H., Kao C. et al. Neuromodulation of the cingulum for neuropathic pain after spinal cord injury // J. Neurosurg. — 2007. — Vol. 107. — P. 169-72.
9. Oakley J.C. Spinal сord stimulation: mechanisms of action / Oakley J.C., Prager J.P. // Spine. — 2002. — Vol. 27. — P. 2574-2583.
10. Richard K. Motor cortex stimulation for intractable pain / Richard K., Osenbach M.D. // Neurosurg Focus. — 2006. — Vol. 21. — Р. 7-19.
11. Sindou M. Neurochirurgie de la douleur / Sindou M., Mertens P., Keravel Y. // Encyclopedie Medico-Chirurgical. — 1996. — 17-700-B-10.
12. Sindou M. Surgical procedure for neuropathic pain / Sindou M., Martens P., Garcia-Larrea L. // Neurosurgery Qurterly. — 2001. — Vol. 11. — № 1. — P. 45-64.
13. Taylor R.S. Spinal cord stimulation for chronic back and leg pain and failed back surgery syndrome: a systematic review and analysis of prognostic factors / Taylor R.S., Van Buyten J.P., Buchser E. // Spine. — 2005. — Vol. 30. — P. 152-160.
14. Van Roost D. Myelotomies for chronic pain / Van Roost D., Gybels J. // Acta Neurochir. Suppl. (Wien). — 1989. — 46. — 69-72.