Журнал «Травма» Том 11, №2, 2010
Вернуться к номеру
Состояние периферической гемодинамики при различных механизмах травмы костей голени
Авторы: А.М. Гребенюк, В.М. Оксимец, Н.Н. Шпаченко, Д.А. Ивашутин - НИИ травматологии и ортопедии Донецкого национального медицинского университета им.М.Горького, Донецк, Украина
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
В статье приведены данные реовазографического обследования 33 пострадавших с травмой голени и приведена динамика изменений периферической гемодинамики и ее взаимосвязи с механизмом травмы. Полученные данные свидетельствуют о том, что при травмах голени в поврежденном сегменте развиваются значительные нарушения периферической гемодинамики – нарушения артериального притока и венозного оттока, более выраженные со стороны венозного отдела. Гемодинамические нарушения при прямом механизме травмы в среднем в 2-3 раза более выражены, чем при непрямом, и имеют отчетливую тенденцию к ухудшению.
В статті наведені данні реовазографічного обстеження 33 постраждалих з травмою гомілки та динаміка змін периферійної гемодинаміки й її взаємозв’язку з механізмом травми. Отримані дані свідчать про те, що при травмах гомілки в ураженому сегменті розвиваються значні порушення периферійної гемодинаміки - порушення артеріального притоку та венозного відтоку, більше виражені з боку венозного відділу. Геодинамічні порушення при прямому механізмі травми в середньому в 2-3 рази більше виражені, ніж при непрямому, і мають чітку тенденцію до погіршення.
In article are cited given reovasographic inspections of 33 victims with a trauma of a shin and dynamics of changes of peripheral haemodynamics and its interrelation with the trauma mechanism is resulted. The obtained data testifies that at shin traumas in the damaged segment considerable infringements of peripheral haemodynamics – infringements of arterial inflow and the venous out-flow develop, more expressed from outside venous department. Haemodynamic infringements at the direct mechanism of a trauma on the average in 2-3 times are more expressed, than at indirect and have the distinct tendency to deterioration
травма голени, прямой и непрямой механизм травмы, периферическая гемодинамика
травма гомілки, прямий та непрямий механізм травми, периферійна гемодинаміка
a trauma of a shin, the direct and indirect mechanism of a trauma, peripheral haemodynamics
Нарушение процессов остеорепарации является одной из актуальных проблем современной травматологии и ортопедии, который, несмотря на значительное количество исследований, требует дальнейшего изучения. Значительный интерес среди работ, посвященных изучению дисрегенераторных процессов в костной ткани, представляет работа коллектива авторов Харьковского института патологии позвоночника и суставов, в которой приводятся обобщенные данные анализа клинико-экспериментальных исследований нарушений сращения переломов [3,8]. Рассматривая репаративный остеогенез как многоуровневый и многофазный процесс клеточной реакции на повреждение, авторы отмечают, что большинство причин замедления или несращения переломов связано с ранней стадией регенерации, на которой возможен «биологический сбой» генетически заложенной программы восстановления ткани, но и на последующих стадиях также могут возникнуть нарушения формирования тканевого регенерата.
Среди причин, нарушающих процессы остеорепарации, авторы выделяют причины, которые связаны с самой травмой – видом травмирующего агента и характером повреждения костной ткани [3,6,8]. В исследованиях было показано, что у 55% больных с нарушением репаративного остеогенеза травма была получена в результате воздействия высокоэнергетического травмирующего агента (ДТП и производственная травма, связанная с воздействием движущихся механизмов), у 24% – в результате среднеэнергетической травмы и у 21% - низкоэнергетической (падение на бок, неудачное разгибание конечности) [5].
Одним из важных факторов, влияющих на остеорепаративные процессы, является состояние кровообращения в поврежденном сегменте. Развивающаяся в результате травмы дезинтеграция кровоснабжения приводит к нарушению оксигенации тканей. Выраженность и протяженность области сосудистых нарушений, дестабилизации ультраструктур микроангиоархитектоники и особенно путей оттока крови находится в прямой зависимости от энергии травмирующего агента [1, 2]. Прогрессирование дистрофических процессов в тканях конечности после травмы в значительной мере зависит от посттравматических микроангиопатий, развивающихся на фоне нарушений в венозном отделе микроциркуляторного русла, что приводит к формированию трансэндотелиальных каналов и люков, плазматическому пропитыванию стенки сосудов, ее гиалинозу и склерозу. Вследствие этих изменений возникает нарушение транскапиллярного обмена, нарастает гипоксия и существенно ухудшается трофическое обеспечение тканей конечности, что способствует прогрессированию дистрофического процесса [1] и, как следствие, замедлению или редукции течения первой стадии репаративного процесса. Наряду с уменьшением оксигенации тканей, снижение объемного уровня кровотока в поврежденном участке приводит к нарушению информационных процессов между зоной повреждения и клеточными источниками репарации [4].
Однако, несмотря на столь значимое значение состояния кровообращения в остеорепаративных процессах, работ, посвященных детальному изучению развития гемодинамических нарушений в раннем посттравматическом периоде и их взаимосвязи с механизмом травмы нами найдено не было.
В связи с этим целью настоящего исследования было изучение динамики изменений периферической гемодинамики в травмированном сегменте и их взаимосвязи с механизмом травмы.
Материал и методы
Для достижения поставленной цели у 33 пострадавших с закрытыми переломами костей голени нами было проведено изучение состояния гемодинамики в травмированном и контралатеральном сегменте (голень). Оценку состояния периферического кровообращения осуществляли реовазографическим методом. Исследования проводились при помощи реографа ReoCom. Среди обследованных пострадавших у 14 человек травма была получена в результате прямого механического воздействия травмирующего агента (удар автомобилем при ДТП), у 19 пострадавших травмы возникли в результате непрямого механизма (скручивание или сгибание). Средний возраст пострадавших составил 28,2±6,4 года и колебался от 21 до 35 лет. Среди обследованных больных с наличием сердечно-сосудистой патологии и сахарного диабета не было. Обследование проводили на 1-2 сутки после травмы, а также 4-5, 7-10 и 13-14 сутки после травмы. При анализе реовазограмм оценивали следующие показатели: скорость максимального кровенаполнения, амплитуду систолической волны, время быстрого и медленного кровенаполнения, амплитуду диастолической волны и межамплитудные показатели диастолической волны и инцизуры.
Анализ результатов исследования осуществляли при помощи методов математической статистики [7].
Результаты и обсуждение
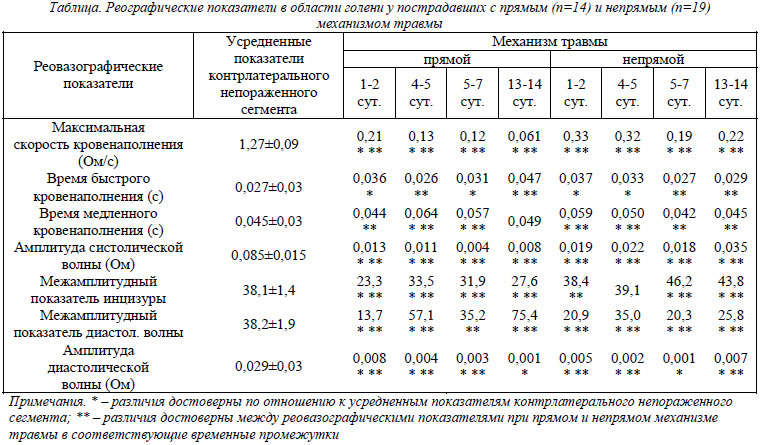
В таблице представлены данные реовазографических исследований.
Из данных, представленных в таблице, видно, что все анализируемые показатели достоверно отличались от таковых на контралатеральном нетравмированном сегменте.
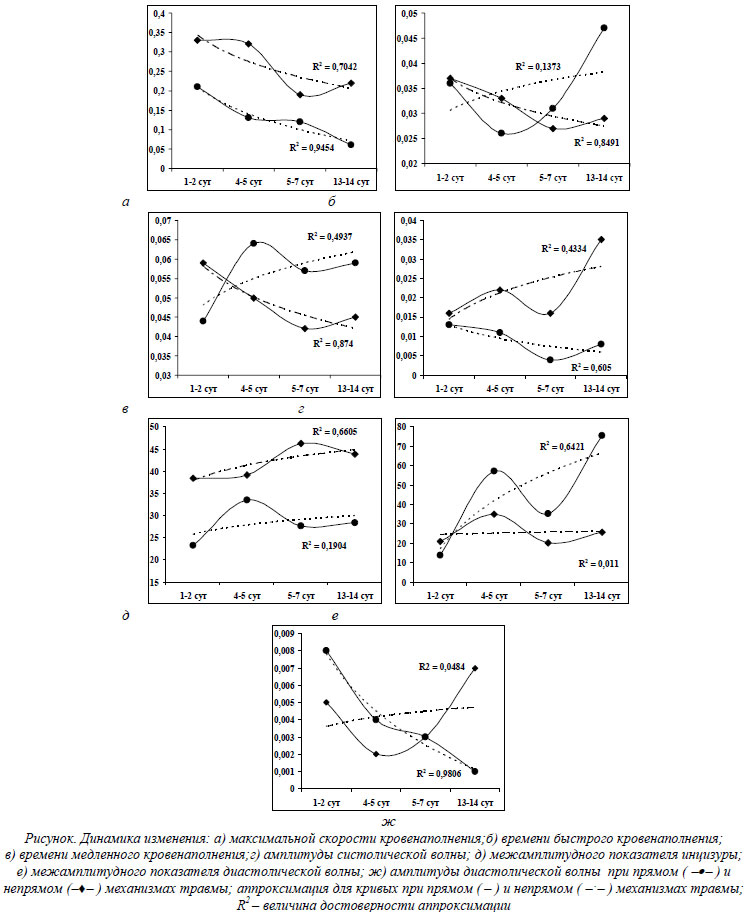
На рисунке представлены графические данные динамики изменения исследуемых реовазографических показателей.
Максимальная скорость кровенаполнения (maxСкКр) в голени при диафизарных переломах большеберцовой и малоберцовой костей снижалась более чем в 6 раз при прямом механизме травмы и в 3,8 раза при непрямом механизме. Динамика изменения maxСкКр в области пораженного сегмента при прямом механизме травмы достоверно отличается (a < 0,005) от таковой при непрямой травме (рис.а). Аппроксимация значений maxСкКр свидетельствует о том, что динамика снижении maxСкКр является достоверной. Причем эта достоверность более выражена для травм с прямым механизмом – R2 стремится к 1 (=0,9454).
При анализе динамики изменения времени быстрого кровенаполнения (tБКр) видно, что в первые сутки после травмы быстрое кровенаполнение голени, как при прямом, так и непрямом механизмах травмы, происходило в 1,3 раза дольше, чем на контрлатеральном сегменте (рис. 1б). В последующие дни это время достоверно уменьшалось при непрямой травме (R2 = 0,8491) и к концу 2-й недели практически не отличается от tБКр на контрлатеральном сегменте. При травмах, полученных в результате прямого воздействия травмирующего агента tБКр, имело тенденцию к увеличению, хотя различия между tБКр при различных механизмах травмы имеют выраженный характер (a < 0,001). Такая же закономерность отмечалась и при анализе динамики изменения времени медленного кровенаполнения (tМКр) (рис.в).
Изменение амплитуды систолической волны (Асв) в течение 2 недель после травмы у пострадавших с непрямым механизмом травмы характеризовалось отчетливой тенденцией к ее увеличению (R2 = 0,4334) после значительного, более чем в 4 раза по сравнению с интактной голенью, уменьшения в течение первых суток после травмы (рис. г). У пострадавших с прямым механизмом перелома Асв достоверно снижалась в течение всего периода наблюдения (R2 = 0,605) и к концу 2-й недели была более чем в 10 раз ниже, чем на контрлатеральном сегменте.
При непрямом механизме травмы межамплитудный показатель инцизуры (МАПин) достоверно увеличивался (R2 = 0,6605) в течение всего периода наблюдения и к концу 2-й недели после травмы был в 1,2 раза больше, чем на нетравмированном сегменте. При прямом механизме травмы МАПин был достоверно ниже, чем на контрлатеральном сегменте в течение всего периода наблюдения (рис.д). Изменения межамплитудного показателя диастолической волны (МАПдв) были диаметрально противоположны изменению МАПин – у пострадавших с непрямым механизмом травмы МАПдв достоверно возрастала (R2 = 0,6421), а при прямом – оставалась практически неизменной (R2 = 0,011) (рис.е).
Амплитуда диастолической волны (Адв) как при прямом, так и непрямом механизмах травмы достоверно снижалась уже с первых суток после травмы (более чем в 4 раза), (рис.ж). Однако в течение последующих суток у пострадавших с непрямым механизмом травмы отмечалась тенденция к увеличению Адв (R2 = 0,6421), а у пострадавших с прямым механизмом – продолжалось достоверное уменьшение Адв (R2 = 0,6421).
Обобщение представленных выше данных свидетельствует о том, что в голени в результате воздействия травмирующего агента происходит развитие значительных нарушений периферического кровообращения. В течение первых суток после травмы значительно снижалась maxСкКр, увеличивалось tБКр и tМКр и снижалась Асв, что свидетельствует о развитии нарушений в артериальном отделе сосудистой системы голени. Выраженность этих нарушений находилась в прямой зависимости от механизма травмы. При прямом воздействии травмирующего агента изменения maxСкКр и Асв были в 1,5-1,6 раза более выражены, чем при непрямом механизме травмы. Наряду с артериальным притоком, значительные изменения развиваются и со стороны венозного отдела – происходит значительное снижение Адв и МАПдв, причем выраженность этих изменений также находится в прямой зависимости от механизма травмы.
Однако более выраженные различия в нарушениях периферической гемодинамики в травмированной голени в зависимости от механизма травмы отмечались в течение последующих суток после травмы. Если при непрямом механизме травмы происходило достоверное уменьшение tБКр и tМКр и к концу второй недели значения этих показателей приближалось к таковым на котрлатеральном сегменте, то при прямом механизме травмы наблюдалась тенденция к увеличению tБКр и tМКр. Такая же тенденция отмечалась и со стороны Асв и МАПин. При непрямом механизме травмы Асв в течение 2 недель отчетливо увеличивалась и к концу 14-х суток достигала практически 50% от значений контрлатерального сегмента. При прямом механизме артериальное кровенаполнение продолжало достоверно уменьшаться и составляло 1/10 от Асв конрлатерального сегмента. МАПин пря непрямом механизме травмы к 13-14 сут. был на 10% больше, чем на нетравмированной голени, а при прямом механизме – почти на 30% меньше.
Согласно нашим исследованиям, наиболее выраженные нарушения в течение первых двух недель после травмы развиваются со стороны венозного отдела, которые проявлялись в виде нарушения венозного оттока и развития застоя в венозном отделе. Так, Адв при прямом механизме травмы была в 29 раз ниже, а при непрямом – почти в 10 раз.
Выводы
Таким образом, полученные в результате исследований данные свидетельствуют о том, что при травмах голени в поврежденном сегменте развиваются значительные нарушения периферической гемодинамики – нарушения артериального притока и венозного оттока. Выраженность этих нарушений находится в прямой зависимости от механизма травмы. Гемодинамические нарушения при прямом механизме травмы в среднем в 2-3 раза более выражены, чем при непрямом, и имеют отчетливую тенденцию к ухудшению в отличие от травм с непрямым механизмом, при которых к концу 2-й недели большинство гемодинамических показателей практически приближаются к показателям нетравмированной голени.
- Володина А.В., Гурко Н.С., Поздняков О.М. Посттравматические микроангиопатии // Анатомо-физиологические и патоморфологические аспекты микрохирургии и огнестрельной травмы / Материалы юбилейной научной конференции, посвященной 125-летию кафедры оперативной хирургии с топографической анатомией ВмедА им. С.М. Кирова, 15-16 ноября 1990 г. – Ленинград, 1990. – С. 95-96.
- Гайворонский А.В., Гайворонский И.В., Дедушкин В.С., Долинин С.В. Состояние микроциркуляции – показатель заживления огнестрельной раны конечности // Анатомо-физиологические и патоморфологические аспекты микрохирургии и огнестрельной травмы / Материалы юбилейной научной конференции, посвященной 125-летию кафедры оперативной хирургии с топографической анатомией ВмедА им. С.М. Кирова, 15-16 ноября 1990 г. – Ленинград, 1990. – С. 96-97.
- Горидова Л.Д., Романенко К.К. Несращения плечевой кости (факторы риска)//Ортопед., травматол. и протезирование. – 2000. – №3. – С. 72-76.
- Илизаров Г.А., Хелимский А.М. Особенности репаративной регенерации при ческостном компрессионно-дистракционном остеосинтезе // Современные проблемы регенерации / Под редакцией Г.Л. Билича и В.Э. Коллы. – Йошкар-Ола, Марийский государственный университет, 1980. – С. 28-55.
- Калашніков А В. Профілактика порушень репаративного остеогенезу// Вісник ортопедії, травматології та протезування. – 2002. – № 2. – С. 54-57.
- Калашніков А. В., Бруско А. Т. Діагностика та лікування розладів репаративного остеогенезу у хворих із переломами кісток // Вісник ортоп., травматол. та протезування. – 2002. - № 3. – С. 35-40.
- Климовицкий В.Г., Колодежный А.В. Вертыло Н.А. Применение математической статистики в медико-биологических исследованиях. – Донецк: издательство «Донеччина», 2004. – 216 с.
- Корж М.О., Горидова Л.Д., Романенко К.К., Дєдух Н.В. Чинники ризику, діагностика та лікування порушень репаративного остеогенезу при діафізарних переломах довгих кісток: Методичні рекомендації. – Київ, 2005.–20 с.