Журнал «Травма» Том 11, №4, 2010
Вернуться к номеру
Перспективні напрями лікування діафізарних переломів кісток гомілки
Авторы: В.М. Шимон, А.А. Шерегій - Ужгородський національний університет, Ужгород, Україна
Рубрики: Травматология и ортопедия
Разделы: Справочник специалиста
Версия для печати
В даній роботі наведено ретроспективний огляд результатів лікування хворих з діафізарними переломами кісток гомілки, проведено порівняльний аналіз результатів лікування гострої травми та ускладнень. Вивчено ефективність традиційних методів оперативних втручань при переломах кісток гомілки на прикладі 160 пацієнтів та обґрунтовано необхідність пошуку новітніх методів лікування.
В данной работе приведен ретроспективный анализ результатов лечения пострадавших с диафизарными переломами костей голени, проведен сравнительный анализ результатов лечения острой травмы и осложнений. Изучено эффективность традиционных методов оперативных методов при переломах костей голени на примере 160 пациентов и выложены взгляды на обоснование необходимости поиска нових методов лечения.
Prospects approaches of tibial fractures treatment has been discribed at the article.
переломи гомілки, остеосинтез, регенерація, мезенхімальні аутологічні клітини
переломи голени, остеосинтез, регенерация, мезенхимальные аутологичные клетки
tibial fractures, osteosynthesis, regeneration, mesenchimal autological cells
Останніми роками в Україні та за кордоном відзначається збільшення числа постраждалих із закритими і відкритими переломами кісток нижніх кінцівок. На сам перед це обумовлено підвищенням темпу життя, та механізацією процесів, які відбуваються в умовах науково технічного прогресу. В механізмі травми гомілки превалюють високо енергетичні агенти, до прикладу такі, як наслідки ДТП, падіння з висоти [3,4]. За даними авторів частка діафізарних переломів серед усіх складає до 48%, а переломи діафізів кісток гомілки складають від 27 до 36% серед всіх діафізарних переломів. 25-35% пацієнтів травматологічних стаціонарів – хворі з переломами кісток гомілки.
Аналіз вітчизняної та зарубіжної літератури вказує на велику медичну та соціально - економічну проблеми лікування діафізарних переломів кісток нижніх кінцівок. Незважаючи на велику кількість розроблених останніми роками і упроваджених в Україні способів стабільно- функціонального остеосинтезу переломів кісток гомілки, нерідко спостерігаються незадовільні результати і ускладнення, які є причиною первинної інвалідності в 2,7-37% випадків. Кількість незадовільних результатів лікування (10-45%), а частота незрощень та утворення псевдоартрозів діафізу гомілки сягає до 15%. При лікуванні складних діафізарних переломів най більше труднощів представляють багато уламкові та роздроблені переломи діафізу гомілки, які складають біля 10% всіх закритих та 35% відкритих переломів кінцівок [5].
Міжнародну статистику, та статистику по Україні підтверджують дані стану показників травматолого – ортопедичної служби Закарпаття, зокрема наші спостереження за період 2006-2009 на базі клініки ЗОКЛ ім. А. Новака.
Основними принципами відновлення цілісності та функції пошкодження кінцівок є раннє застосування раціональних методів лікування. Умовами консолідації таких переломів є зіставлення уламків при мінімальній травматизації та стабільно - функціональна фіксація з можливістю ранньої функції ушкодженої кінцівки. Таким вимогам відповідає метод блокуючого інтрамедулярного остеосинтезу [2,8]. Наряду з перевагами даного методу не слід нехтувати наступними недоліками - інтрамедулярний остеосинтез викликає розповсюджені і тривалі структурні зміни кісток, характер яких, з одної сторони, обумовлені порушеннями медулярного кровотоку, але з другої – подразнюючим впливом на кістковий орган [9]. Як альтернативний метод слід вважати метод через кісткового дистракційно компресійного остеосинтезу апаратами зовнішньої фіксації різних конструкцій.
Однією з найважливіших причин сповільненої і порушеної консолідації є порушення мінерального і білкового метаболізму Ці порушення нерідко пов’язані з віком пацієнта, інтеркуррентними захворюваннями або з екологічними чинниками та недостатній регенераторний потенціал кісткової тканини даної локалізації. [6,7]. Тому досить актуальним залишається пошук чинників впливу на репаративний остеогенез з метою його стимуляції та оптимізації. Відомо багато засобів фізичного, хімічного, медикаментозного, гормонального, ферментативного та інших методів впливу на остеорепарацію, але в останні роки все більш очевидним є той факт, що наведені вище засоби, на які покладались великі надії, далеко не завжди виправдовують ці надії, особливо з метою оптимізації репаративних потенцій.
Конструювання нових систем компресійно – дистракційних апаратів, виробів для функціонально стабільного остеосинтезу безумовно наділені обмеженнями, обумовленими біологічними властивостями тих тканин, забезпечити оптимальну регенерацію яких вони покликані. Клінічні спостереження підтверджують що перспектива покращення результатів лікування патології кісток тільки за рахунок вдосконалення з’єднання та утримання відломків переважно вичерпані. Кількість створюваних технологій на сучасному етапі уже ледь помітно переходить в якість лікування. Саме по цій причині «біологічний» напрямок, як додатковий метод лікування пацієнтів травматолого-ортопедичного профілю базуючись на використанні клітинних технологій та біоімпланталогії притягує жваву зацікавленість. Перспективним є застосування клітинної та тканинної фетотерапії саме з метою оптимізації та стимуляції відновлювальних процесів [1]. Являючись похідною мезенхіми кісткова тканина відноситься до відновлюючоїся тканини, диферонна організація якої представлена від стовбурових клітин до високо диференційованих клітин.
Вважається доведеним, що фетальні клітини мають значно більший пластичний потенціал, ніж зрілі структури, в зв'язку з чим останні здатні до диференціації в залежності від мікрооточення, а темп їх проліферації суттєво вищий, ніж в зрілих клітинах (Грищенко В.І. із співавт., 2004).
Клітинними джерелами репаративної регенерації кісткової тканини є мало- диференційовані клітини - попередники, у яких функція проліферації не блокована. До них відносяться стромальні (мезенхімальні) стовбурові клітини (ССК) локалізовані в стромі кісткового мозку та поза скелетних кровотворних органах. Остеогенні клітини внутрішнього шару періосту, клітинні еле- менти каналів остеонів та ендоста та періваскулярні клітини.
Згідно даних В.М.Казаков, В.Г.Климовицький, В.М.Пастернак, В.М.Оксимець, А.Г. (2006 р.) аутологічні мезенхімальні клітини наділені значними можливостями відновлювати утрачений репаративний потенціал клітинних джерел остео- та хондрорепарації.
Мета роботи - покращення результатів лікування пацієнтів з діафізарними переломами кісток гомілки та ускладненнями у вигляді незрощень, неоартрозів, та сповільненої консолідації.
Матеріал та методи
За період від 2006 по 2009 роки в умовах клініки ортопедії ЗОКЛ ім. А. Новака з приводу гострої травми гомілки госпіталізовано 138 пацієнтів. Пацієнтів які звертались з приводу ускладнень, незадовільних результатів лікування переломів гомілки об’єднали в окрему групу, це 22 пацієнти. Загальна частка постраждалих з діафізарними переломами гомілки від усіх госпіталізованих з приводу діафізарних переломів склала 27,3 %.
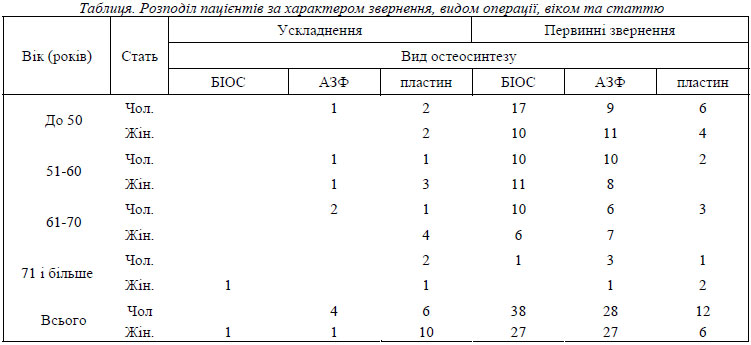
Нами хворі були розподілені наступним чином: пацієнти які звернулись з приводу травми – 138 осіб та пацієнти які звернулись повторно з приводу ускладнень – 22. В кожній із цих груп сформовано підгрупи за наступними критеріями. За статтю: чоловіки -78, жінки - 60; в групі з ускладненнями: чоловіків - 10, жінок - 12. За віком 4 вікові групи: до 50 р. - 35 чоловіків та 27 жінок, 51-60 рр. - 24 чоловіків та 23 жінок, 61-70рр. - 22 чоловіків та 17 жінок; в віковій групі старше 71 р. - 7 чоловіків та 5 жінок (табл.). Контрольні огляди проводили в термінах 1, 3, 6 міс., та в 12 місяців по можливості. З метою застосування найбільш адекватного методу оперативного лікування переломів за показами застосовували різні методики оперативних втручань, а саме: позавогнищевий остеосинтез апаратами зовнішньої фіксації (АЗФ), інтрамедалярний остеосинтез (БІОС), погружний накістковий остеосинтез та консервативно. В плані передопераційної підготовки використовували системи скелетного витяжіння у 39 випадках первинних звернень.
Нами проведено серію лабораторних досліджень на білих лабораторних щурах в ході яких вивчалась регенерація кісткової тканини в зоні змодельованого дефекту стегнової кістки. Використовувались зрілі білі лабораторні щурі вагою 60-90 г. Під загальним знечуленням із доступу в проекції нижньої третини стегнової кістки в проксимальному епіметафізі стегна проводилась остеоперфорація – бором створювали округлої форми моно кортикальний дефект кісткової тканини. В зону дефекту культивували суміш мезенхімальних клітин. З метою наглядності створена контрольна група тварин, яким трансплантація не проводилась. Поетапно тварин виводили з експерименту. В ході експерименту тварини підлягали клінічному спостереженню та рентгенологічному контролю. Для визначення клітинного складу кісткового регенерату виконували гістологічні зрізи з наступним морфометричним та цитологічним дослідженням визначали динаміку репаративного процесу. Досліди проводились на базі лабораторії Інституту патології хребта і суглобів ім. проф. М.І.Ситенка АМН України. Тварини виведені з експерименту. Тривають лабораторні дослідження та обробка отриманих даних.
Результати та обговорення
Результати лікування оцінювали відповідно до критеріїв R. Johner., O. Wruhs [8] за допомогою рентгенологічного обстеження, за даними об’єктивного спостереження та відновленням функції кінцівки та здатністю її витримувати тривале навантаження. З метою порівняльного аналізу оцінкам «відмінно», «добре», «задовільно», та «незадовільно» присвоєні кількісні значення – 5, 4, 3, 2, відповідно.
В терміни 1 місяць після операції відхилень від очікуваних результатів не було відмічено, в 3 місяці післяопераційного періоду результати були оцінені як відмінні в 93% , добрі в 5% та задовільні в 2 %. В 3 місяці повторно було оглянуто 122 пацієнтів. В 6 місяців оглянуто 109 пацієнтів. Результати розцінені як відмінні в 86%, добрі в 7% та задовільні в 5%, незадовільні – 2%. В 12 місяців оглянуто 74 пацієнтів.
Результати мали наступний вигляд: відмінні в 81%, добрі в 10% та задовільні в 6%, незадовільні – 3%.
Як видно із наведеної таблиці найбільше число ускладнень при остеосинтезі діафізарних переломів гомілки несе метод накісткового остеосинтезу 16 (72,7% серед усіх незадовільних результатів). Аналізуючи наведені дані хочемо відмітити, що більша частина пацієнтів це жінки які народили 2 або більше дітей дітей (7 хворих).
Після застосування через кісткового остеосинтезу незадовільні результати спостерігались у 5 (22,7 %) випадках. В одному випадку (4,6%) незадовільний результат після блокую чого інтрамедулярного остеосинтезу у вигляді незрощення перелому в термін 11 місяців після оперативного втручання по причині інтерпозиції м’яких тканин було констатовано у 76 річної пацієнтки. Пацієнти, які поступали з незадовільними результатами попереднього лікування були повторно оперовані в умовах клініки ортопедії травматології ЗОКЛ ім. А. Новака. Нами було виконано блокуючий інтрамедулярний остеосинтез без розсвердлювання інтрамедулярного каналу в 9 випадках, римеризація застосовувалась в 5 випадках. Апарат зовнішньої фіксації застосовувався в 8 випадках. Операції доповнювались кістковою аутопластикою спогіозним аутотрасплантатом із крила здухвинної кістки у 8 випадках. При незрощенні після інтрамедулярного остеосинтезу в ході повторної операції виконано усунення інтерпозиції м’яких тканин, фіксація відломку кортикальним гвинтом, кісткова аутопластика спонгіозним аутотрасплантатом.
Висновки
В ході передопераційного планування слід віддавати перевагу на користь малоінвазивних, мало травматичних методик.
При лікуванні асептичних ускладнень, незрощень та складних багато уламкових переломів запроваджувати досягнення клітинної інженерії.
- Деев Р.В., Исаев А.А., Кочиш А.Ю., Тихилов Р.М. Пути развития клеточных технологий в костной хирургии // Травматология и Ортопедия России.-№1 – (47).-2008.-С.64-74.
- Дубас В.И., Сулима В.С., Щибель И.В. с соавт. Десятирічний досвід використання на Прикарпатті пружно стійкого остеосинтезу при лікуванні хворих з переломами довгих кінцівок // Ортопедия, травматология и протезирование.-№3.-2007.-С.127 – 130.
- Калашніков А.В. Профілактика порушень репаративного остеогенезу //Вісник ортопедії, травматології та протезування. – 2002. – № 2. – С. 54-57.
- Климовицкий В.Г., Пастернак В.Н., Оксимец В.М. с соавт. Влияние этиологического фактора травмы на течение репаративного остеогенеза. Часть 1. Сращение диафизарных переломов голени при непрямом механизме травмы // Травма.Т.8,№1.-2007.-С.7 -12.
- Редько К.Г., Соломин Л.Н. Приоритеты в выборе метода остеосинтеза у пациентов с закрытыми диафизарными переломами большеберцовой кости // Травматология и Ортопедия России.№1(34).-2005.-С. 68-71.
- Шимон В.М., Гелета М.М., Василинець М.М., Сігеті В.Ю. Показники калію та кальцію у хворих з переломами діалізів кісток в гірських районах // Травма.-2008.-Т.9, №4.-С.448-452.
- Allen J., Lindsey R.W., Hipp J.A et al. The effect of retained in- tramedullary nails on tibial bone mineral density // Clinical Biomechan- ics.-N23.-2008.-P.839–843.
- Johner R., Wruhs O. Classification of libial shaft fractures and cor- relation with results after rigid internal fixation // Clin. Orthop. - 1983. - №178. - P.7-25.
- Forster M.C., Bruce A.S.W. Should the tibia be reamed when nail- ing? // Injury, Int. J. Care Injured.-2005.-N36.-P.439-444.