Журнал «Травма» Том 11, №4, 2010
Вернуться к номеру
Лечение несросшихся диафизарных переломов конечностей путем стимуляции фибриногенеза и создания напряжений регенерирующих тканей
Авторы: А.К. Попсуйшапка, В.А. Литвишко - Харьковская медицинская академия последипломного образования, Харьков, Чугуевская районная больница, Чугуев, Украина
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
В статье изложен опыт лечения несросшихся переломов конечностей у 145 больных в сроки после травмы от 1 года до 6 лет. У всех пациентов лечение предусматривало полную функциональную нагрузку конечности при фиксации отломков внешним стержневым аппаратом или функциональной повязкой (для переломов голени). У 26 больных использована костная аутопластика губчатым трансплантатом с препаратами стимулирующими фибриногенез.
В статті наведений досвід лікування переломів кінцівок, які не зростаються, у 145 хворих у терміни після травми від 1 до 6 років. Усіх пацієнтів лікування передбачало повне функціональне навантаження кінцівки при фіксації відламків зовнішнім стержньовим апаратом або функціональною пов’язкою (при переломах гомілки). У 26 хворих використана кісткова аутопластика губчастим трансплантатом з препаратами, що стимулюють фібріногенез.
In this article were reported our experience of non-union extremities fractures treatment in 145 patients, in the period from 1 to 6 years after trauma. In all cases we applied complete functional weight-bearing in fracture’s external fixation or functional brace cast. In 26 patients were used autografting with combinations of medicines that stimulate fibrinogenesis.
несросшиеся переломы, стержневые аппараты, напряжения, фибриногенез
переломи, що не зрослися, стрижневі апарати, напруги, фібриногенез
non-healed fracture, rod’s apparatus, tension, fibrinogenesis
Начнем с того, что широкое внедрение остеосинтеза при диафизарных переломах, включая и использование новейших версий фиксаторов, не уменьшает число несращений. Такое явление в травматологии ставит много спорных вопросов, и по ним высказываются различные предположения, которые можно разрешить только путем исследования механизмов регенерации костной ткани. К сожалению, на сам процесс регенерации при остеосинтезе мало обращают внимания, а чаще возникшее осложнение объясняют погрешностью в его выполнении. Всякая повторная операция по поводу несращения должна вызывать у хирурга стремление к раскрытию природы прошедшего, чтобы его последующие действия были более правильными. Лечение таких последствий дает возможность понять многие важные особенности процесса сращения и более осознанно смотреть на предшествующие действия. К сожалению, лечение последствий далеко не всегда приходится выполнять тому, с чьей «подачи» они возникли. В результате тот, кто начинал лечение, не всегда имеет возможность критически оценить свои действия и результат, к которому они привели.
В данной работе представлен личный клинический опыт авторов за период с 1989 по 2009 годы (20 лет). Больные лечились в клиниках ГУ «Институт патологии позвоночника и суставов им. проф. М.И. Ситенко АМН Украины», областной травматологической больнице г. Харькова и Чугуевской районной больнице Харьковской области. Всего нами пролечено 145 больных в возрасте от 7 до 83 лет. По локализации поврежденного сегмента они распределились следующим образом: несросшиеся переломы костей голени – 91; несросшиеся переломы бедра – 35; несросшиеся переломы плеча – 11; несросшиеся переломы предплечья – 8.
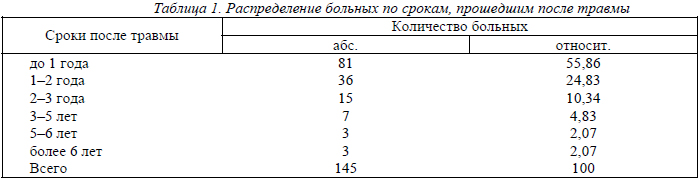
По срокам, прошедшим после травмы до обращения к нам больные распределялись следующим образом (табл. 1)
Все больные имели классическую картину несросшегося перелома с наличием угловой подвижности отломков различной амплитуды: от едва уловимой (1-2°) до отчетливо регистрируемой в объем 7–20°.
Амплитуда подвижности отломков так же, как и величина периостальных костных разрастаний вокруг концов отломков, как правило, была пропорциональна срокам после травмы и функциональной активности пациента. Атрофический тип несращения имел место у 19 больных, олиготрофический – у 61, гипертрофический – у 65. У 8 пациентов несращение сочеталось с наличием межотломкового дефекта кости длиной от 7 до 16 мм. Это было характерным для несращений большеберцовой кости или одной из костей предплечья, когда дефект сохранялся благодаря целостности рядом расположенной кости.
У большинства больных (117) имела место фиксированная угловая деформация сегмента величиной в среднем 10–25°, у двоих она достигала 60–80°.
Важно отметить, что из наблюдаемых нами больных 14 из них были уже подвергнуты повторно оперативным вмешательствам по поводу развившегося несращения в различных лечебных учреждениях Украины. Причем четыре из них перенесли по два повторных вмешательства, два по три повторных вмешательства, один – 4, один – 9. У троих несращение сочеталось с остеомиелитом.
Принципы лечения и применяемые методики. Исходя из многих данных литературы, следует выделить два основных фактора, оказывающих стимулирующее воздействие на несростающиеся переломы это:
- механические напряжения регенерирующих тканей;
- повторная травма в виде различных костно-пластических операций, которые запускают новый цикл процесса регенерации, и при этом он дополнительно стимулируется [2].
При лечении данных осложнений мы опираемся на следующие представления о механизмах действия этих факторов.
Первое. При уже существующем несращении всегда существует фактор атипичных по величине и вектору напряжения тканей в зоне перелома [1, 3]. Либо эти напряжения настолько ничтожны, что не в состоянии обеспечить эффект стимуляции пролиферации опорных тканей, либо вектор этих напряжений направлен в поперечном направлении, что приводит к соответствующей (патологической) ориентации клеток, формирующих коллаген. Как правило, это обусловлено либо отсутствием функциональных нагрузок на конечность, либо блокированием этих нагрузок целой малоберцовой костью или одной из костей предплечья.
Наш клинический опыт показывает, что только включение отломков в правильную и полноценную осевую нагрузку сопровождается перестройкой фиброзной ткани в межотломковой зоне и завершается сращением. Поэтому первым и обязательным условием лечения несросшегося перелома мы считаем полную функциональную нагрузку поврежденной конечности с максимальным участием отломков и тех тканей, которые их соединяют, в передаче механических усилий. Для нижней конечности – это ходьба с полной опорой, для верхней – лечебные упражнения. При этом функция фиксирующего устройства должна состоять лишь в противодействии боковым перемещениям дистального фрагмента относительно проксимального, при сохранении контактной передачи напряжений через зону регенерирующих тканей. Такие условия в максимальной степени имеют место при использовании функциональных повязок и аппаратов внешней фиксации. В отличие от внутренних фиксаторов, которые «шунтируют» напряжения в зоне контакта отломков.
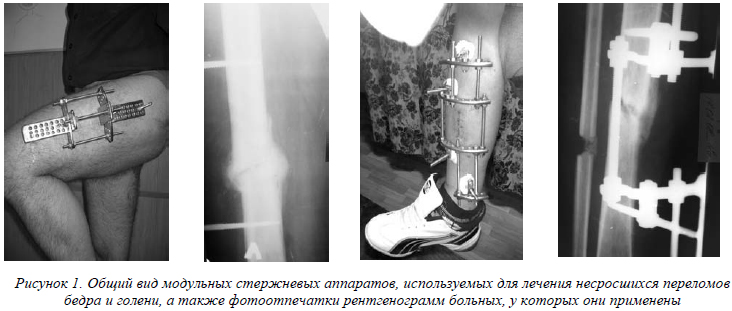
При лечении несросшихся переломов голени, плеча и предплечья мы использовали модульные стержневые аппараты (рис. 1), позволяющие проводить коррекцию деформаций и обеспечивать режим динамической фиксации отломков при условии полной функциональной нагрузки конечности. При несросшихся переломах голени всегда выполняли резекцию участка малоберцовой кости на уровне несращения большеберцовой для возможности последней испытывать полную осевую нагрузку. У части больных при сохранении правильной оси голени фиксацию отломков осуществляли функциональной гипсовой повязкой.
Второе. Полагаем, что положительный эффект любой костно-пластической операции при несращении в первую очередь связан с повторным разрушением тканей, кровоизлиянием, которые запускает новый виток процесса регенерации. Именно так выглядели впервые предложенные операции: перфорация по Беку, декортикация по Жюде. Позже стали использовать аутрансплантаты и их рассматривали, как дополнительный пластический материал, обладающий, к тому же, стимулирующими регенерацию свойствами.
На основании собственного опыта мы полагаем, что использование аутопластического материала несет в себе две основные функции. Первая – это заполнение дефекта механическим матриксом, и вторая – это стимуляция фибриногенеза при контакте с излившейся кровью. Обилие разрушенных сосудов губчатой кости сопровождается высвобождением тканевого фактора, который стимулирует агрегацию тромбоцитов и последующий коагуляционный каскад, который заканчивается образованием фибринового сгустка [2]. Проще говоря, при смешивании крови с измельчены губчатым аутотрансплантатом успешно образуется фибриновый сгусток с костными включениями, который представляет собой морфогенетический матрикс, на котором быстро происходит рост новых сосудов и формирование костной ткани. Как мы убедились, в этом плане наиболее эффективными оказываются измельченные губчатые трансплантаты, смешиваемые с фибринсодержащими препаратами: гемостатическая губка, тахакоб, сержисел, а также добавление аутоплазмы, обогащенной тромбоцитами.
Свободную костную пластику со стимуляцией фибриногенеза выполняли при атрофических типах несращения, а также при наличии костного дефекта. Приводим таблицу с указанием основных вариантов операций, выполненных нами (табл. 2).
Выводы
Выполненное нами оперативное вмешательство оказалось последним у 140 больных. У одного нами были выполнены две операции, и еще у одного три. Повторные операции были связаны с быстрым сращением малоберцовой кости после резекции ее участка и отсутствием сращения отломков большеберцовой кости. Важно отметить, что в процессе лечения пациенты сохраняли физическую активность, осуществляли трудовую деятельность. Сроки фиксации аппаратом или функциональной повязкой составили у большинства больных 3–5 месяцев. У 6 пациентов они были более продолжительными 6–13 месяцев. У троих костного сращения достигнуто не было. Из них двое пациентов с низкими переломами плечевой кости и один с низким переломом большеберцовой кости. Эти пациенты пользуются вспомогательными ортезами и приспособились к условиям жизни.
- Мутасем Самани. Функциональное лечение несрастающихся переломов большеберцовой кости (клиникоэкспериментальное исследование) / Мутасем Самани Дис. … канд. мед. наук. – Х., 1998. – 114 с.
- Попсуйшапка А. К. Сращение отломков после перелома кости / А.К. Попсуйшапка, В.А. Литвишко, О.А. Подгайская // Международный медицинский журнал. – 2009. – Т. 15, № 2 (58) – С. 73-80.
- Попсуйшапка А.К. Использование стержневых аппаратов для функционального лечения несросшихся переломов бедренной кости / А.К. Попсуйшапка // Ортопед. травматол. – 1999. № 1. – С. 59-62.