Журнал «Травма» Том 10, №2, 2009
Вернуться к номеру
Електроміографічне дослідження в оцінці структурно-функціонального стану скелетних м’язів у хворих з прогресуючою м’язовою дистрофією
Авторы: О.Г. Гайко, Ю.М. Гук, А.М. Зима - Інститут травматології та ортопедії АМН України, Київ, Україна
Рубрики: Травматология и ортопедия
Разделы: Справочник специалиста
Версия для печати
В статті надані сучасні дані по електроміографічному дослідженню пацієнтів з ортопедичними проявами при прогресуючій м’язовій дистрофії, висвітлені показники голчастої електроміографії з позицій структурно-функціонального стану скелетних м’язів, виявлені їх зміни в залежності від динаміки міодистрофічного процесу. Наданий аналіз результатів електро-міографічного дослідження скелетних м’язів у 25 хво-рих з різною ортопедичною патологією при прогресую-чій м’язовій дистрофії.
В статье представлены современные данные электромиографического исследования пациентов с ортопедическими проявленими при прогрессирующей мышечной дистрофии, освещены показатели игольчатой электромиогафии с позиций структурно-функционального состояния скелетних мышц, выявлены их изменения в зависимости от динамики миодистрофичческого процесса. Представлен анализ результатов электромиографического исследования ске-летних мышц у 25 больных с разной ортопедической патологией при прогрессирующей мышечной дистрофии.
Modern data of electromyographic investigation of patients with orthopedic manifestation at progressive muscular dystrophy were presented, indices of needle- shaped electromyography at the positions of structural-functional state of skeletal muscles, their changes were revealed depending on dynamics of myodystrophic process. The analysis of electromyographic investigation results is presented. This analysis included investigation of skeletal muscles of 25 patients with various ortho-pedic pathology at progressive muscular dystrophy.
прогресуюча м''язова дистрофія, електроміографічне дослідження, ортопедична патологія
прогрессирующая мышечная дистрофия, электромиографическое исследование, ортопедическая патология
progressive muscular dystrophy, electromyographic investigation, orthopedic pathology
На сьогоднішній день електроміографічне (ЕМГ) дослідження є провідним неінвазійним методом оцінки структурно-функціонального стану м'язів та діагностики нервово-м'язових захворювань.
В сучасних літературних джерелах існує загальна інформація про зміни показників біоелектричної активності при ЕМГ-дослідженні у хворих з первинними міопатіями взагалі та при прогресуючій м’язовій дистофії (ПМД) зокрема. Також відомо, що даний метод дослідження застосовують для вирішення питання диференційної діагностики між первинними (м'язовими) та вторинними (невральними) міопатіями [1, 2, 3].
Окрім уточнення первинного характеру ушкодження м’язів, головним завданням нашого дослідження було оцінити структурно-функціональний стан скелетних м’язів та активність міодистрофічного процесу шляхом вивчення спонтанної активності (СА), параметрів потенціалів рухових одиниць (ПРО), ЕМГ максимального скорочення та порівняння цих показників з клінічним даними. Не останню увагу приділили дослідженню коливання показників від стадії та варіанту перебігу захворювання.
Важливим і доцільним було визначити ЕМГ показники, які підтверджують клінічні дані стосовно показань чи протипоказань до оперативного втручання, в тому числі з використанням скелетних м’язів.
З теоретичних позицій зрозуміло, що при показниках ЕМГ-дослідження, які свідчать про знижену функцію м’язів, їх використання в оперативному втручанні неможливе. Так, оперативні втручання на сухожилках чи м’язах, в основі яких лежить їх подовження або транспозиція з метою усунення контрактури суглоба і відновлення активних рухів в ньому, виконувати недоцільно, що пов’язано з втратою м’язової сили останніми при їх використанні на 2 бали.
Розуміння та трактовка результатів любого ЕМГ дослідження лежить в площині вивчення параметрів потенціалів рухової одиниці (РО). РО складається із альфа-мотонейрону, його аксону з множинними термінальними розгалуженнями, нервово-м'язового сінапса та сукупності м'язових волокон, що іннервуються даним мотонейроном. Основним електрофізіологічним проявом активності РО є потенціал, що формується усіма м'язовими волокнами, які входять до її складу. Цей потенціал прийнято називати потенціалом рухової одиниці (ПРО) [1-4]. До параметрів ПРО відносять тривалість, амплітуду та форму потенціалу. Саме їх аналіз є основою дослідження стану РО.
За даними літературних джерел відомо, що при ПМД вищезазначені показники відрізняються загальними змінами: зменшенням тривалості та амплітуди ПРО; збільшенням кількості поліфазних потенціалів [1, 3, 4-6].
Матеріал та методи
Електроміографічне дослідження проводили на електроміографі "Neuroscreen" фірми Tonnies (Німеччина) у 25 хворих (65 м’язів) з різними формами ПМД віком від 3 до 34 років. В динаміці обстежено було 12 пацієнтів. Дане дослідження застосовували при чотирьох найпоширеніших формах ПМД у пацієнтів на різних стадіях захворювання з характерною ортопедичною патологією. В групі обстежених переважали хворі з ПМД Дюшена – 19 хворих. Серед інших обстежених: з ПМД Ерба-Ротта було двоє пацієнтів, Емері-Дрейфуса – троє хворих, Ландузі-Дежеріна – один пацієнт. У майже всіх пацієнтів було діагностовано характерну ортопедичну патологію, а саме деформацію стоп та контрактури великих суглобів. У двох пацієнтів з ПМД Дюшена, що знаходились в доклінічній стадії захворювання, ортопедична патологія була відсутня. Хворим проводилась голкова електроміографія (ГЕМГ) m. rectus femoris, m.tibialis ant., m.deltoideus.
При проведенні ЕМГ дослідження значення показників тривалості, що були отримані у обстежених хворих з ПМД, порівнювалися з відповідними значенням за нормативними таблицями для різних м'язів здорових людей різних вікових груп (Гехт Б.М., 1997) [1, 4].
При дослідженні використовували стандартну ЕМГ з використанням концентричних голкових електродів. Слід нагадати, що класична ГЕМГ включає в себе дослідження: спонтанної активності м`язових волокон в стані спокою, вивчення параметрів потенціалів рухових одиниць при мінімальному довільному скороченні м`язів.
Умови реєстрації: електрод заземлення у вигляді стрічки закріплювали на передпліччі чи гомілці; шкіру оброблювали спиртом; біполярний голковий електрод вводили в рухову точку м`яза, який тестували. Велике значення надавали положенню хворого під час дослідження, враховуючи необхідність можливості повного розслаблення досліджуваної групи м’язів. При наявності больового синдрому або контрактури суглобів для укладки хворого використовували валики та спеціальні мішечки з піском.
ГЕМГ має 3 основних етапи:
1-й етап - дослідження м'яза у спокої. Якщо електрод знаходиться в повністю релаксованому нормальному м'язі, то ніякої активності не фіксується (біоелектрична мовчанка). Іноді (менше ніж у 10 % випадків) можна записати потенціали фасцикуляцій. Якщо вони не поєднуються з іншими ненормальностями, то це є так звані доброякісні фасцикуляції.
Активність міодистрофічного процесу оцінювали шляхом дослідження спонтанної денерваційної активності (СА), під якою розуміють активність, що спостерігається в м’язі за відсутності його довільного скорочення. Відомо, що в здорових м'язах СА не виявляється. Серед СА у хворих на ПМД констатовано потенціали фібриляцій (ПФ) та позитивні гострі хвилі (ПГХ), а також в поодиноких випадках – міотонічні чи псевдоміотонічні розряди.
Оцінку інтенсивності СА проводили по наступних критеріях за Б.М. Гехтом та ін.[1, 4]:
«+» - ПФ, ПГХ слабкої вираженості (1-3 потенціали);
«++» - середньої вираженості (4-6 потенціалів);
«+++» - виражені (7-15 потенціалів);
«++++» - бурні (більше 15 потенціалів).
Чутливість ЕМГ-апарата на цьому етапі становила 50 мкВ на поділці, швидкість розгортки - 10 мс на поділці.
2-й етап – дослідження при мінімальному напруженні м'яза. Пацієнта просять ледь-ледь (майже подумки) напружити досліджуваний м'яз (саме напружити, а не виконати рух, що, природньо, у більшості випадків неможливо у цього контингенту хворих). При цьому починають фіксувати ПРО з найнижчим порогом рекрутування. Для кожної рухової одиниці параметри амплітуди вимірюються від найнижчої точки позитивного піку до найвищої точки негативного піку, тривалість - від початку відхилення кривої потенціала від ізолінії до повернення до неї, форма чи фазність - як кількість позитивно-негативних компонентів потенціала, що перетинають ізолінію.
Амплітуда - найбільш варіабельний параметр ПРО, в нормі знаходиться в межах 300-1000 мкВ. При аналізі форми ПРО оцінюється кількість фаз потенціалу, яка в нормі не перевищує 4. Число поліфазних потенціалів у здорових людей залежить від м’яза і в більшості не перевищує 5-10 %. Найбільш важливим та інформативним, а, головне, стійким параметром є тривалість ПРО. Отримані параметри тривалості порівнювали з середніми величинами здорової людини в залежності від м’яза, що досліджується, та віку пацієнта [1, 4].
Чутливість ЕМГ-апарата на цьому етапі становить 100 мкВ на поділці; швидкість розгортки – 10 мс на поділці.
3-й етап – дослідження при максимальному напруженні м'яза. При максимальному напруженні нормального м'яза ПРО слідують один за одним настільки часто, що починають взаємно накладатись один на одного. Таким чином, відокремити окремі ПРО стає неможливо.
Чутливість ЕМГ-апарата на цьому етапі становить 100-200 мкВ на поділці; швидкість розгортки - 10 мс на поділці.
Результати та обговорення
Найбільш важливим та вагомим ЕМГ параметром в дослідженні структурно-функціонального стану скелетних м’язів при ПМД є тривалість ПРО, яка відображає площу або величину території РО, що залежить від кількості м'язових волокон та їх діаметра. Ці данні підтверджуються і патоморфологічними дослідженнями [1, 2, 4].
Відомо, що ПМД характеризується ушкодженням окремих м'язових волокон з їх анатомічним і функціональним випадінням із складу РО: зменшенням діаметру міофібрил, ураженням різної глибини – від легких змін до грубих некрозів волокон із значним порушенням скорочувальної функції м’яза. Вищевказані процеси призводять до зменшення тривалості ПРО внаслідок зменшення м’язових волокон у РО [1, 4, 5]. Так, у всіх обстежених пацієнтів відмічено зміну тривалості ПРО в сторону її зменшення (рис. 1.).
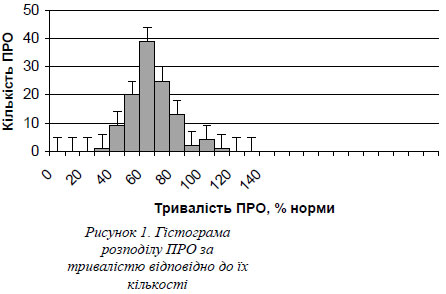
При аналізі гістограми розподілу ПРО за тривалістю виявлено, що показник тривалості знаходився в межах 33-117 % норми; 60,1 % ПРО мали зменшену тривалість (≤ 70% середньої величини тривалості ПРО м’язів здорових людей відповідного віку). За даними літератури, нормальними вважаються потенціали, в яких тривалість знаходиться в межах ±30 % від середньої величини при умовах їх нормальної амплітуди та кількості фаз, а середня тривалість ПРО - при відхиленні в межах ± 13-20% від середнього значення норми [1, 4].
Наступний показник, який вивчали, була амплітуда ПРО, яка як відомо залежить від діаметра м'язового волокна, щільності розміщення м'язових волокон у зоні відведення концентричного голчатого електрода та ступеня його близькості до джерела генерації [3]. У більшості випадків (52%) амплітуда ПРО знаходилась в межах 200-400 мкВ. Наступний показник, що вивчався, була форма ПРО. У 57% хворих на ПМД відмічено збільшення кількості поліфазних ПРО (більше 5 фаз) до 30 - 50% та більше. Інтенсивність СА коливалася при різних формах ПМД: від мінімальної (+) при початковій стадії ПМД Емері-Дрейфуса та Ландузі-Дежеріна до вираженої в стадії розгорнутої клінічної симптоматики ПМД Дюшена. Найбільша її вираженість (+++) була відмічена при швидкопрогресуючому варіанті перебігу ПМД Дюшена та Ерба-Ротта в стадії розгорнутої клінічної симптоматики (рис. 2).
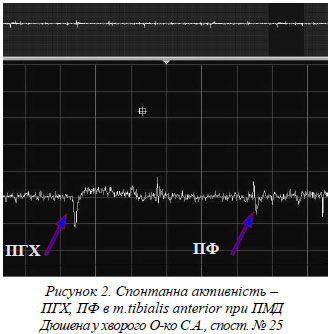
В усіх хворих спостерігали «міопатичний тип» рекрутування РО – при мінімальному русі з поступовим збільшенням сили скорочення реєструється більша, ніж в нормі ступінь рекрутування РО. Це призводить до формування низькоамплітудної «насиченої» ЕМГ з більшим числом потенціалів на однаковому відрізку часу [1, 4].
Виникнення цих змін пояснюються слабкістю РО, яка втратила частину своїх м'язових волокон, тому для виконання мінімального скорочення м’яза необхідно використати більшу кількість ушкоджених дистрофічним процесом РО (рис.3.).
Нами було виявлено деяку залежність змін ЕМГ показників від варіанту перебігу захворювання відповідно до його форми та стадії ПМД.
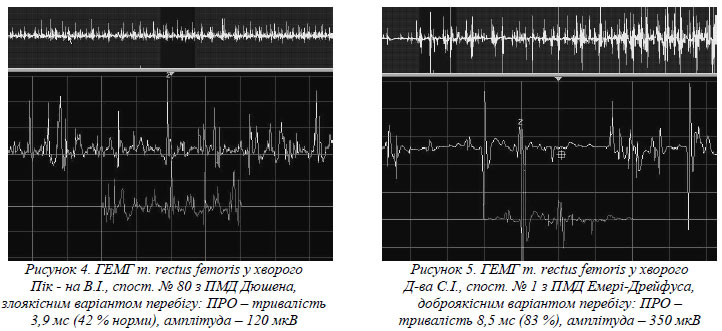
При злоякісній формі ПМД Дюшена та Ерба-Ротта спостерігалися різко виражені зміни тривалості ПРО - зменшення середнього показника до 65,3% норми, в більшості випадків тривалість окремих ПРО знаходилась в межах 45-71% норми, а амплітуда 140-420 мкВ, виявлявся значний відсоток (до 40 %) поліфазних ПРО (рис 4.). При аналізі гістограми розподілу ПРО за тривалістю 68,9 % ПРО мали тривалість ≤ 70% норми. СА особливо була виражена в стадії розгорнутої клінічної симптоматики (до +++).
Ми вважаємо, що зниження тривалості ПРО, кількість поліфазних ПРО та СА є найбільш постійними показниками активності міодистрофічного процесу. Прослідковується залежність між цими показниками та активністю (злоякісністю) дистрофічного процесу у м’язах.
При доброякісних формах ПМД Емері-Дрейфуса, Ландузі-Дежеріна та Ерба-Ротта зміни ЕМГ показників були менш виражені: зменшення середньої тривалості до 79,3 %, в більшості випадків тривалість окремих ПРО знаходилась в межах 61 - 99% норми, а амплітуда 210-650 мкВ; кількість поліфазних ПРО була меншою, ніж при злоякісних формах (рис. 1.5.). Спонтанна активність була не значно виражена (+) або відсутня. При аналізі гістограми розподілу ПРО за тривалістю тільки 30,7 % ПРО мали тривалість ≤ 70% норми.
Але потрібно зауважити, що лише динаміка змін показників ЕМГ дослідження може підтвердити клінічний варіант перебігу захворювання, а саме тип зі швидким чи повільним прогресуванням.
Вивчення змін параметрів ПРО залежно від стадії захворювання показало, що в початковій стадії з’являлася тенденція до зниження тривалості та амплітуди ПРО, збільшення кількості поліфазних потенціалів, що пояснюється ушкодженням незначної кількості м’язових волокон; в стадії розгорнутої клінічної симптоматики відмічено значне зниження тривалості та амплітуди ПРО, збільшення кількості поліфазних ПРО та виражену СА; в термінальній стадії констатовано найбільш виражені зміни ПРО, СА менш виражена, що пов’язано із затуханням дистрофічного процесу – ушкоджені м'язи некротизувалися та замістилися сполучною та жировою тканинами.
Викликає цікавість і дослідження взаємозв’язку – зниження м’язової сили та зміни показників ПРО. У наших пацієнтів виявлено, що найменша тривалість ПРО виявлена при силі м’язів 1-2 бали, а найбільша при 3-4 балах.
Таким чином, електроміографічне дослідження дає можливість встановити характер м’язового ушкодження (первинне чи вторинне), а зміни параметрів ПРО м'язів при голковій ЕМГ залежать від клінічного варіанту перебігу ПМД та дозволяють оцінити активність міодистрофічного процесу і структурно-функціональний стан м’язів. Прослідковується тенденція залежності показників ЕМГ відносно динаміки патологічного процесу у м’язах.
Висновки
1. Електроміографічне дослідження дає можливість провести диференційну діагностику між первинною та вторинною міопатією та встановити характер м’язового ушкодження.
2. Встановлено тенденцію до залежності між змінами показників ЕМГ (параметри потенціалів рухових одиниць – тривалість, амплітуда та форма), вираженістю спонтанної активності (позитивні гострі хвилі, потенціали фібріляцій) та динамікою дистрофічного процесу у м’язах.
- Електромиография в диагностике нервно-мышечных заболеваний / Б.М. Гехт, Л.Ф. Касаткина, М.И. Самолов, А.Г. Санадзе. – Таганрог: Изд-во ТРТУ. – 1997. – С. 21–44, 121–165.
- Гаусманова-Петрусевич И. Мышечные заболевания. – Варшава: Польское гос. мед. изд-во, 1971. – С. 165–171.
- Гехт Б.М., Касаткіна Л.Ф. Типология потенциалов двигательных единиц и плотность мышечных волокон при нервно-мышечных заболеваниях // Невропатология и психиатрия им. C.С. Корсакова. – 1984. – Т. 84, № 11. – С. 1635–1642.
- Коуен Х., Брумлик Дж. Руководство по електромиографии и електродиагностике. – М.: Медицина, 1975. – С. 61– 62, 128– 130.
- Гехт Б.М., Касаткина Л.Ф., Кевиш А.В. Електромиография с использованием игольчатых электродов в анализе структуры и функционального состояния двигательных единиц при нервно-мышечных заболеваниях // Невропатология и психиатрия им. C.С. Корсакова. – 1980. – Т. 80, № 6. – С. 822–829.
- Shapiro F., Specht L. Сurrent concepts review. The diagnosis and orthopaedic treatment of inherited muscular diseases of childhood // J. Bone Jt Surg. – 1993. – Vol. 75-A, №3. – Р. 439–454.