Журнал «Медицина неотложных состояний» 5 (36) 2011
Вернуться к номеру
Трансфузиологические вопросы современной реаниматологии. Часть II. Анемия и гемотрансфузия при критических состояниях
Авторы: Усенко Л.В., Царев А.В., Петров В.В., Панченко Г.В., Дубина В.Н., Кузьмова Е.А., Кобеляцкий Ю.Ю. Кафедра анестезиологии и интенсивной терапии Днепропетровской государственной медицинской академии, КУ «Днепропетровская областная клиническая больница им. И.И. Мечникова»
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Версия для печати
В статье освещаются вопросы оптимального уровня гемоглобина при различных критических состояниях, показания к гемотрансфузии и ее осложнения, а также ее влияние на исход критического состояния.
Анемия, гемотрансфузия, критические состояния, интенсивная терапия.
Гемоглобин —это не статическое здание, а динамический механизм, не кислородное вместилище, а молекулярное легкое, изменяющее свои размеры при присоединении кислорода и его отдаче.
M.F. Perutz (1978)
Согласно данным эпидемиологических исследований, проведенных в Западной Европе, Канаде, Великобритании и США, примерно 40 % больных в критическом состоянии проводится гемотрансфузия в среднем пяти доз эритроцитной массы, с целью коррекции постгеморрагической анемии для улучшения доставки кислорода (DO2). Причем у менее чем 20 % пациентов отделений реанимации и интенсивной терапии (ОРИТ) гемотрансфузия проводилась с целью лечения геморрагического шока, основной же массе пациентов гемотрансфузия проводилась по поводу анемии [1]. Однако в последние годы происходит переоценка взглядов на показания к проведению гемотрансфузии, что обусловлено целым рядом гемотрансфузионно-ассоциированных осложнений (инфекционных, иммуносупрессии и пр.). В ряде клинических исследований было выявлено ухудшение исходов после проведения гемотрансфузии у пациентов в критических состояниях [2]. При этом, несмотря на все вышеизложенное, гемотрансфузия в современной реаниматологии остается одним из ее краеугольных камней, являясь жизнеспасающим мероприятием, подчас играющим одну из решающих ролей в исходе критического состояния. В связи с этим во второй части нашей работы мы бы хотели изложить современные подходы к проведению трансфузии компонентов и препаратов крови на основании международного опыта, а также консенсусных «Рекомендаций по гемотрансфузии у взрослых пациентов с травмами и при критических состояниях» Американского колледжа медицины критических состояний (ACCM), Общества медицины критических состояний (SCCM) и Восточной ассоциации хирургии и травмы, принятых в 2009 г. [1].
Общие фундаментальные представления о функции крови
Появление крови у животных в эволюционном аспекте было связано с возникновением и отделением от пищеварительной трубки и полостей тела сосудистой системы, а формирование элементов крови — с образованием мезодермы и соединительной ткани. Эволюция животных, начиная с беспозвоночных, происходила вначале в направлении возникновения амебоцитов (которые, по-видимому, являются предшественниками в эволюции лейкоцитов — губки, кишечнополостные), последующего затем формирования незамкнутой кровеносной системы, сообщающейся с лакунами и содержащей гемолимфу (членистоногие, большинство моллюсков и пр.), и в конечном итоге формирования замкнутой кровеносной системы (кольчатые черви, немертины, некоторые моллюски), в которой находится гемолимфа, содержащая дыхательные пигменты (поскольку все белковые переносчики кислорода имеют определенный цвет). Известно четыре дыхательных пигмента, обеспечивающих транспорт кислорода: гемоцианин — медьсодержащий, синего цвета (ракообразные, паукообразные, моллюски), и хлорокруорин — железосодержащий, зеленого цвета (кольчатые черви), гемоглобин — красного цвета (многие черви, моллюски, членистоногие, иглокожие), гемэритрин — розового или фиолетового оттенка (он в отличие от гемоглобина не содержит в своей молекуле порфирин), встречается только в эритроцитах некоторых кольчатых червей (полихеты).
Таким образом, в природе существует целый ряд белковых переносчиков кислорода. Необходимо отметить, что гемоглобин у беспозвоночных животных в большинстве случаев растворен в плазме и только у некоторых (моллюски, немертины, иглокожие, полихеты) содержится в эритроцитах. Молекулярный вес дыхательных пигментов, растворенных в крови, значительно больше, чем тех, которые содержатся в эритроцитах. Так, молекулярный вес гемоглобина, растворенного в гемолимфе, около 2 250 000 дальтон, гемоцианина — до 10 млн дальтон, а гемоглобина эритроцитов беспозвоночных — только 16–17 тыс. дальтон (у человека 60 тыс. дальтон). Все эритроциты беспозвоночных являются ядерными клетками округлой или овальной формы.
У позвоночных животных растворенных в плазме дыхательных пигментов нет, поскольку все позвоночные содержат гемоглобин, заключенный в эритроциты. Наиболее крупные эритроциты имеют пресмыкающиеся и земноводные, в связи с чем они имеют наименьшее в природе содержание эритроцитов (амфибии — 0,13–0,02 х 1012, Hb — 50–90 г/л; рептилии — 0,5–1,5 х 1012, Hb — 35–120 г/л). Начиная с хрящевых рыб у позвоночных появляются тромбоциты, которые также являются ядросодержащими клетками. Лейкоциты представлены зернистыми и незернистыми формами. На последних этапах эволюции у высших позвоночных животных — млекопитающих — эритроциты безъядерные (как и тромбоциты), круглой формы в виде двояковогнутого диска, только у ламы и верблюда все эритроциты овальные.
Крайне важным в реаниматологии является понимание значимости поддержания оптимального уровня гемоглобина для обеспечения адекватного газообмена в организме. Так, в 1 л артериальной крови содержится в среднем 200 мл кислорода (СаО2 — 190–210 мл/л), причем только 3 мл (1,5 %) растворено в плазме крови, остальной кислород связан с гемоглобином. Поэтому если бы человек использовал только растворенный в плазме кислород, то для обеспечения поддержания аэробного метаболизма потребовался бы минутный объем сердца, равный 89 л/мин (при норме 4–6 л/мин).
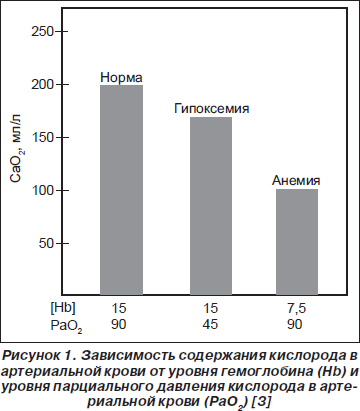
Необходимо подчеркнуть, что снижение парциального давления кислорода в артериальной крови (РаО2) на 50 % (c 90 до 45 мм рт.ст.) приводит к снижению СаО2 только на 18 % (с 200 до 163 мл/л). Напротив, снижение уровня гемоглобина на 50 % (с 150 до 75 г/л) сопровождается 50% снижением СаО2 (с 200 до 101 мл/л). Эту важную особенность влияния указанных факторов на оксигенацию организма П. Марино определил как проблему «анемия или гипоксемия» [3]. Действительно, анемия оказывает значительно большее влияние на оксигенацию крови, чем гипоксемия, играя одну из ведущих ролей в исходе того или иного критического состояния (в частности, черепно-мозговой травмы, острого инфаркта миокарда и пр.), являясь патофизиологическим обоснованием ряда нижеизложенных рекомендаций (рис. 1).
Общие правила назначения, эффекты и свойства компонентов крови
1. Эритроциты. В настоящий момент выделяют следующие эффекты проведения гемотрансфузии:
— повышение доставки кислорода тканям, однако при этом не доказано повышение потребления кислорода (VO2) тканями;
— повышение клеточной массы и глобулярного объема после острой кровопотери или анемии;
— коррекция кардиальных эффектов тяжелой анемии с критическим уровнем DO2 [4–6].
Отдельно выделяют целый ряд факторов риска, ассоциированных с гемотрансфузией: гиперволемия, отек легких, посттрансфузионная циркуляторная перегрузка, лихорадки, острые постгемотрансфузионные реакции, синдром полиорганной недостаточности, трансмиссивные инфекции и пр.
Гемотрансфузия вызывает иммуномодулирующий эффект у реципиента, повышая риск развития нозокомиальных инфекций, острого повреждения легких (TRALI) и, возможно, аутоиммунных заболеваний в отдаленном периоде [1].
При хранении донорской крови ее вязкость резко увеличивается, причем нарастание вязкости крови выявляется в большей мере после 5–10 суток консервации. При старении эритроцитов нарушение реологии связано с изменением как их потенциала, так и структуры мембран — снижение ее деформируемости. При трансфузии крови с нарушенной реологией происходят уменьшение текучести и секвестрация эритроцитов перед первой капиллярной сетью — в легочных сосудах [7].
В целом трансфузия «старой» донорской крови ведет к нарушению тканевого и органного кровообращения вследствие снижения уровня 2,3-ДФГ и смещения кривой диссоциации оксигемоглобина влево, т.е. ведет к развитию гипоксии [8]. Консервированная кровь донора отнюдь не идентична циркулирующей крови пациента и характеризуется сниженной коагуляционной способностью, гиперкалиемией и сниженным рН [9]. Таким образом, извлеченная из сосудистого русла кровь теряет свои нативные свойства, в значительной мере превращаясь в суспензию из микросгустков тромбоцитов и неполноценно функционирующих эритроцитов. Донорская кровь представляет собой чужеродную ткань, неизбежно отторгаемую организмом реципиента. По мнению А.И. Воробьева, переливание крови представляет собой антифизиологическое явление и старая формулировка «переливание капля за каплю» находится в абсолютном противоречии с физиологией человека [10].
Показанием к проведению трансфузии эритроцитов является острая анемия вследствие массивной кровопотери, т.е. потеря 25–30 % объема циркулирующей крови, сопровождающаяся снижением уровня Hb < 70–80 г/л, Ht < 25 % и возникновением циркуляторных нарушений (при отсутствии сердечной недостаточности, угрожающей коронарной недостаточности, церебральной патологии).
Согласно Е.Б. Жибурту, назначение эритроцитов для пациентов с нормоволемией и без продолжающегося кровотечения должно строиться с учетом клинических признаков:
— признаков анемии (постуральная гипотензия или тахикардия, одышка и головокружение при нагрузке, апатичность или спутанность сознания);
— сопутствующей патологии (ишемическая болезнь сердца (ИБС), цереброваскулярные заболевания, дисфункция левого желудочка, шок или снижение транспорта кислорода, хроническая патология легких, острая дыхательная недостаточность, беременность.
Исходя из вышеизложенного, целевой уровень гематокрита должен составлять:
а) отсутствуют клинические признаки анемии и нет сопутствующей патологии — 0,21 л/л;
б) клинический признак анемии или сопутствующая патология — 0,26 л/л;
в) продолжающаяся химиотерапия, или лечение острого лейкоза, или трансплантация костного мозга — 0,26 л/л;
г) дооперационная анемия и ожидаемая потеря крови > 500 мл или беременность — 0,26 л/л;
д) клинический признак анемии и сопутствующая патология — 0,29 л/л;
е) острый коронарный синдром (острый инфаркт миокарда или нестабильная стенокардия) — 0,30–0,33 л/л [11].
В настоящее время в Украине доступны следующие эритроцит-содержащие среды: эритроцитная масса; эритроцитная масса, обедненная лейкоцитами (ЭМОЛ); эритроцитная масса, обедненная лейкоцитами и тромбоцитами (ЭМОЛТ); отмытые эритроциты; эритроцитная взвесь; криоконсервированные эритроциты.
К сожалению, в Украине наиболее широко используемой в клинической практике остается эритроцитная масса, которая характеризуется содержанием > 2,5 x 109 лейкоцитов, до 90 % тромбоцитов и более 70 мл плазмы (> 3,5 г белка), что обусловливает высокий риск развития побочных эффектов гемотрансфузии, поскольку, как было изложено в первой части данной статьи, постгемотрансфузионные осложнения в большом числе случаев связаны с донорскими лейкоцитарными реакциями. В связи с этим для нивелирования лейкоцитарных реакций прибегают к использованию ЭМОЛ (лейкоциты < 1,0 х 106 и менее 15 % тромбоцитов), ЭМОЛТ (лейкоциты < 1,2 х 109; тромбоциты < 20 х 109), отмытых эритроцитов (лейкоциты < 5,0 х 108; белок < 0,5 г; IgA < 0,2 мг), а также криоконсервированных эритроцитов (лейкоциты < 1,0 х 109).
При этом необходимо отметить, что консерванты, которые используются при заготовке эритроцитных сред (глюгицир, CPDA-1 содержат цитрат натрия, фосфат, дигидрофосфат натрия и аденин), для длительного хранения эритроцитов малоэффективны. Поскольку основная часть веществ, необходимых для обеспечения функциональной активности клеток (аденин, глюкоза), удаляется вместе с плазмой в процессе центрифугирования на этапе заготовки эритроцитной массы. В связи с этим были разработаны и широко стали применяться в мире принципиально иные системы контейнеров, содержащих безадениновый антикоагулянт СPD в донационном контейнере, и консервант (ресуспендирующий — взвешивающий раствор) для эритроцитной массы — в трансфер-контейнере (SAGM — аденин, декстроза, маннитол). Полученная по данной технологии эритроцитная взвесь является наиболее оптимальным вариантом заготовки эритроцитов и основной эритроцитной средой, используемой в клинической практике мира.
Эритроцитная взвесь в отличие от эритроцитной массы обеднена лейкоцитами (< 1,0 х 106 в дозе), имеет длительный срок хранения (42 дня), за счет добавления ресуспендирующего раствора обеспечивает достаточный энергетический запас для консервированных эритроцитов, а входящие в состав раствора аденин, глюкоза и маннитол снижают метаболическое истощение эритроцитов, обеспечивают меньший уровень гемолиза и длительную сохранность 2,3-ДФГ. Использование данной технологии позволяет получить из цельной крови большее количество донорской плазмы, при этом доза эритроцитной взвеси, имея гематокрит Ј 0,70 л/л, обеспечивает значительное снижение вязкости и облегчает трансфузию (не надо разводить) [12].
Также необходимо помнить, что при переливании более 1000 мл эритроцитной массы, консервированной цитратом натрия, требуется его нейтрализация путем введения хлорида или глюконата кальция (5 мл 10% раствора) внутривенно на каждые 500 мл переливаемой эритроцитной среды. Однако введение большой дозы хлорида (глюконата) кальция (30–40 мл 10% раствора) может привести к развитию побочных эффектов в виде повышения возбудимости миокарда, брадикардии и пр. [1].
2. Свежезамороженная плазма (СЗП). Показанием к назначению СЗП служит только нарушение свертывания, особенно в тех клинических случаях, когда имеется дефицит нескольких факторов свертывания крови (СЗП не применяется для коррекции гипопротеинемии!).
Показанием к назначению СЗП является продолжающееся кровотечение либо проводимая операция при показателях МНО > 1,5; АЧТВ > 45 с.
Дозирование СЗП (за исключением случаев массивных кровотечений > 1 объема циркулирующей крови или 10 доз эритроцитной массы; тромбоцитопенической пурпуры, а также проведения плазмафереза) должно быть основано исходя из массы тела пациента:
— масса тела 50 кг — 2 дозы;
— масса тела 50–80 кг — 3 дозы;
— масса тела > 80 кг — 4 дозы [11].
С целью срочной инактивации действия варфарина (при активном кровотечении или при экстренном хирургическом вмешательстве), кроме СЗП, необходимо применение витамина К. В то же время витамин К не показан, если требуется кратковременная нормализация МНО и по клиническим показаниям необходимо возобновление действия варфарина через 24–48 часов после операции.
Выделяют следующие целевые значения показателей МНО и АЧТВ:
а) кровотечение, значительное хирургическое вмешательство или инвазивная процедура — МНО < 1,5; АЧТВ < 45 с;
б) срочная инверсия эффекта варфарина — МНО < 1,5 [11].
Критические состояния. Согласно последним исследованиям, пациенты в критических состояниях сохраняют толерантность к анемии при снижении уровня гемоглобина до 70 г/л. Но при этом отмечается, что данный усредненный уровень при ряде критических состояний (коронарная патология, цереброваскулярные и легочные заболевания) не является толерантным [1].
По определению ВОЗ, под анемией у взрослых лиц подразумевают снижение уровня гемоглобина ниже 130 г/л у мужчин и ниже 120 г/л у небеременных женщин. В целом не остро развившаяся анемия является характерной чертой для пациентов в отделениях реанимации и интенсивной терапии. Снижение уровня гемоглобина ниже 90 г/л в ОРИТ ассоциировано с повышением летальности [13]. Однако при этом ряд исследований продемонстрировал прямую взаимосвязь между числом гемотрансфузий и уровнем летальности пациентов в критических состояниях [1].
У пациентов с геморрагическим шоком (политравма, желудочно-кишечные, сосудистые кровотечения и пр.), который не корригируется введением 2 л кристаллоидов, рекомендуется ранняя эмпирическая гемотрансфузия, которая должна основываться не только на учете уровня гемоглобина, но и на физиологических параметрах каждого конкретного пациента, скорости и предполагаемом объеме продолжающегося кровотечения (уровень 1).
Гемотрансфузия может быть показана у пациентов с доказанным острым кровотечением и нестабильной гемодинамикой либо неадекватной доставкой кислорода (уровень 1).
Причинами развития анемии (не связанной с острой кровопотерей) при критических состояниях являются: нарушение продукции эритропоэтина и метаболизма железа [14, 15], проведение регулярных эксфузий крови для лабораторных исследований, развитие активных кровотечений (эрозивно-язвенные изменения желудочно-кишечного тракта, применение антикоагулянтов и пр.), снижение эритропоэза [16]. В последнем случае причинами угнетения эритропоэза выступают:
— истощение эритропоэтической реакции при низком гемоглобине;
— развитие воспалительной реакции, вызванной TNF, IL-1, IL-6;
— повышение уровня гепсидина (пептид-гормона, регулирующего метаболизм железа);
— дефицит железа, витаминов;
— иные патологические состояния (например, повреждение почек разной этиологии) [17].
При развитии анемии, т.е. дефиците носителя кислорода, происходит сдвиг кривой диссоциации оксигемоглобина вправо, являясь компенсаторным механизмом, облегчающим снабжение тканей кислородом. При этом хроническая анемия сама по себе является стимулом для повышения в эритроцитах уровня 2,3-ДФГ и соответствующего снижения сродства гемоглобина к кислороду. Это общая реакция для всех типов анемии, в частности при почечной недостаточности, циррозе печени, железодефицитной анемии. Поэтому тканевая оксигенация на определенном этапе развития анемии может быть поддержана без существенного увеличения сердечного выброса.
В случае острой кровопотери в процессе эволюции у животных и человека отработаны физиологические компенсаторные реакции, включающие в себя развитие аутодилюции, снижение АД, усиление отдачи кислорода за счет снижения его сродства к гемоглобину, увеличение текучести крови. Снижение АД при острой кровопотере приводит к «заболачиванию» эритроцитами микроциркуляторного русла, в том числе легких и периферии, в результате чего развивается стаз. При этом рефлекторно повышается свертываемость — наступает фаза гиперкоагуляции. Указанные сдвиги могут привести к срыву компенсации и развитию ДВС-синдрома, тяжелым нарушениям органной микроциркуляции и синдрому полиорганной недостаточности (СПОН) [8].
Согласно последним международным рекомендациям [1], использование в клинической практике рестриктивной стратегии трансфузионной терапии (т.е. проведение гемотрансфузии при пороговом уровне Hb < 70 г/л) является более эффективным, чем либеральной стратегии (пороговый уровень Hb, при котором необходимо проводить гемотрансфузию, — < 100 г/л), у большинства пациентов в критических состояниях, которые имеют стабильную гемодинамику. За исключением группы пациентов с острым инфарктом миокарда или нестабильной стенокардией (уровень 1). Так, уровень летальности при использовании рестриктивной стратегии был ниже (22,3 %) в сравнении с либеральной стратегией (28,1 %), особенно в группах пациентов в критическом состоянии, имевших менее 20 баллов по шкале АРАСНЕ II и возраст < 55 лет.
Использование в клинической практике только показателя уровня Hb в качестве порогового значения для принятия решения о проведении гемотрансфузии недопустимо. Выработка показаний для проведения гемотрансфузии должна индивидуально основываться на показателях волемического статуса больного, наличии признаков шока, длительности и степени выраженности анемии, а также состоянии параметров сердечно-сосудистой и дыхательных систем (уровень 2) [1]. То есть обоснованием для проведения гемотрансфузии должны быть данные о том, что у конкретного пациента анемия не является толерантной.
Острое изоволемическое снижение уровня гемоглобина до 50 г/л ассоциировано с достоверным развитием когнитивных изменений у здоровых лиц, чего не наблюдается при снижении гемоглобина до 70 г/л.
Доставка кислорода находится на адекватном уровне у большинства лиц при снижении гемоглобина до 70 г/л. Причем было показано, что снижение DO2 до 7,3 ± 1,4 мл х кг–1 х мин–1 у здоровых лиц в сознании не приводит к неадекватной системной оксигенации, а критическая DO2 развивается только при достижении значений ниже указанного уровня. В случае острой анемии снижение содержания кислорода в артериальной крови обычно является толерантным за счет компенсаторного повышения сердечного выброса. Так, согласно исследованию TRICC, было показано, что критическим уровнем, при котором необходимо начинать гемотрансфузию, является уровень гемоглобина, равный 70 г/л у большинства пациентов, находящихся в критическом состоянии [18].
Cогласно рекомендациям [1], в отсутствие острого кровотечения гемотрансфузия должна быть проведена введением одной дозы эритроцитной массы. Это позволит избежать трансфузионно-ассоциированной циркуляторной перегрузки и снизить риск развития отека легких. Однако у ряда пациентов с критической анемией, которая приводит к развитию компенсаторных реакций в виде увеличения сердечного выброса, перераспределения органного кровотока и повышения экстракции кислорода, что неизбежно будет вести к нарушению тканевой оксигенации и развитию гипоксии, необходимым будет введение более 1 дозы эритроцитной среды.
Отсутствуют преимущества «либеральной» гемотрансфузионной стратегии у критических пациентов, находящихся на искусственной вентиляции легких (уровень 2).
Таким образом, гемотрансфузия должна проводиться при снижении уровня гемоглобина ниже 70 г/л у критических больных со стабильной кардиальной патологией (уровень 2).
В целом гемотрансфузия не должна рассматриваться как абсолютный метод улучшения тканевого потребления кислорода при критических состояниях. Цель гемотрансфузии — повышение уровня гемоглобина для улучшения доставки кислорода тканям. Однако проведение гемотрансфузии повышает адгезию эритроцитной массы к эндотелию кровеносных сосудов реципиента, таким образом достоверно снижая кровоток в микроциркуляторном русле [19].
Гемотрансфузия может быть полезной у пациентов с острым коронарным синдромом, у которых имеет место снижение уровня гемоглобина ниже 80 г/л (уровень 3) [1].
Современные данные не поддерживают рутинное проведение гемотрансфузии у больных с ИБС, а порог для ее проведения остается дискутабельным. Так, в ретроспективном исследовании 78 974 пациентов в возрасте более 64 лет, у пациентов с низким уровнем гематокрита на момент поступления уровень 30-дневной летальности был выше. Проведение гемотрансфузии было ассоциировано со снижением уровня 30-дневной летальности. Но при этом среди пациентов с уровнем Ht > 0,33 л/л проведение гемотрансфузии не приводило к снижению летальности, и наоборот, у пациентов с Ht > 0,36 л/л ее проведение было ассоциировано с высоким риском летального исхода.
Политравма. Исследования показали, что рестриктивная стратегия гемотрансфузии является более безопасной у пациентов с политравмой. Алгоритм проведения гемотрансфузии при политравме в случае остановленного и непродолжающегося острого кровотечения на фоне уже проведенной начальной с момента получения травмы волемической ресусцитации должен строиться исходя из следующих этапов (рис. 2):
1. Идентификация у пациента с политравмой уровня Hb < 70 г/л или Ht < 0,21 л/л.
2. При уровне Hb < 70 г/л необходимо провести гемотрансфузию (причем у пациентов с тяжелой сердечно-сосудистой патологией порог для начала гемотрансфузии должен быть выше).
3. При уровне Hb > 70 г/л необходимо исключить гиповолемию:
3.1. В случае наличия гиповолемии необходимо провести волемическую ресусцитацию кристаллоидами и/или коллоидами для достижения нормоволемии.
3.2. В отсутствие гиповолемии необходимо исключить возможное нарушение доставки кислорода тканям (в виде снижения SvO2, персистирующего дефицита оснований или лактат-ацидоза).
4. При выявлении нарушения доставки кислорода необходимо установить катетер Свана — Ганца для измерения сердечного выброса и оптимизации DO2.
5. В отсутствие нарушения DO2 — мониторирование уровня гемоглобина в динамике.
Нейрореаниматология. Большинство обсервационных исследований нейрореанимационных пациентов с субарахноидальным кровоизлиянием (САК), черепно-мозговой травмой (ЧМТ) и инсультами демонстрируют прямую взаимосвязь между гемотрансфузиями и плохим исходом заболевания [20].
1. Эффекты анемии на функции головного мозга. Уровень гемоглобина является одним из основных компонентов доставки кислорода в головной мозг, поэтому анемия негативно влияет на скорость церебрального метаболизма. Преимущественное увеличение церебрального кровотока, которое обратно пропорционально снижению содержания кислорода в крови и ее вязкости, что и имеет место при анемии, обеспечивает доставку DO2 к тканям головного мозга. Механизм, обеспечивающий развитие церебральной вазодилатации, является важным фактором улучшения церебральной DO2 в случае анемии. При этом гемоглобин в эритроцитах может выступать в роли кислородного сенсора при гипоксии, обеспечивающий модуляцию кровотока с реализацией вазодилатации посредством оксида азота и АТР, таким образом повышая кровоток и, следовательно, поступление DO2 к тканям головного мозга.
У здоровых добровольцев оптимальный уровень DO2 соответствует уровню Ht около 0,42 л/л [21].
2. Эффекты гемотрансфузии на функции головного мозга. Согласно ряду исследований, гемотрансфузия повышает уровень оксигенации головного мозга в большинстве случаев у пациентов с САК и ЧМТ [22]. При этом прирост парциального давления кислорода в ткани головного мозга (PbtO2) после гемотрансфузии не зависел от уровня церебрального перфузионного давления, однако прямо пропорционально коррелировал с приростом концентрации гемоглобина и обратно пропорционально – с базальной церебральной оксигенацией [23]. Cледовательно, у пациентов с анемией и низким уровнем PbtO2 (< 15 мм рт.ст.) гемотрансфузия оказывает более благоприятный эффект, еще раз подчеркивая тот факт, что базальная церебральная оксигенация является важным фактором, обеспечивающим эффект гемотрансфузии.
3. Субарахноидальное кровоизлияние. Гемотрансфузия выступает независимым фактором риска развития вазоспазма и плохого исхода. Предполагается, что гемотрансфузия может приводить к еще большему вазоспазму при САК посредством локального ингибирования NO, ответственного за вазодилатацию. При этом, согласно данным исследования, уровень гемоглобина > 110 г/л на момент поступления у пациентов с САК обеспечивал протективный эффект вазоспазм-индуцированной ишемии мозга. Другое проведенное сравнительное исследование рестриктивной гемотрансфузионной стратегии (уровень гемоглобина 70–90 г/л) и поддержания гемоглобина в пределах 100 г/л показало, что более высокий уровень ассоциирован со снижением риска плохого исхода у пациентов с САК. Таким образом, как анемия, так и проведение гемотрансфузии ассоциированы с увеличением летальности при САК [20, 24].
4. Ишемический инсульт. Поскольку гематокрит является главной детерминантой, определяющей вязкость крови, и существует обратно пропорциональная связь между гематокритом и церебральным кровотоком, то повышение гематокрита в области пенумбры может вызвать развитие стаза и локального тромбоза, что в целом ухудшает исход ишемического инсульта [25].
Считается, что уровень гемоглобина 100 г/л является наиболее оптимальным при ишемическом инсульте и должен определять показания к проведению гемотрансфузии [20].
5. Черепно-мозговая травма. ЧМТ характеризуется дисбалансом между церебральной доставкой и потреблениемкислорода, приводящим к гипоксии мозга. При ЧМТ для пациентов с САК и инсультом также было показано, что и гемотрансфузия, и тяжелая анемия достоверно ассоциированы с плохим исходом [20]. Согласно данным исследования TRICC, отмечено увеличение 30-дневной летальности и риска развития СПОН у пациентов с рестриктивной (Hb 70–90 г/л) стратегией гемотрансфузии по сравнению с либеральной (Hb 100–120 г/л) [18]. Однако, согласно рекомендациям [1], не выявлено доказательств преимущества либеральной стратегии гемотрансфузии у пациентов со средней или тяжелой ЧМТ (уровень 2).
Важным фактором нейромониторинга, позволящим определить показания к гемотрансфузии, являются методы прямого измерения PbtO2 или непрямого измерения инфракрасной церебральной оксиметрии (rSO2), которые необходимо применять у всех нейрореанимационных пациентов.
В целом трансфузиологический подход в нейрореаниматологии должен строиться на основании следующих критериев:
1) Hb > 100 г/л — не проводить гемотрансфузию;
2) Hb < 70 — проводить гемотрансфузию;
3) Hb 70–100 при PbtO2 < 20 мм рт.ст. или rSO2 < 60 % — проводить гемотрансфузию [20].
Тяжелый сепсис и септический шок. На сегодняшний день оптимальный уровень гемоглобина при данной патологии не определен и показания к проведению гемотрансфузии должны вырабатываться индивидуально (уровень 2). Согласно данным ряда исследований, проведение гемотрансфузии у септических больных приводило к повышению доставки кислорода и, как правило, не увеличивало потребление кислорода тканями. Показано, что гемотрансфузия, несмотря на повышение уровня гемоглобина, в то же время не улучшала тканевую оксигенацию у пациентов с SIRS/сепсисом, имевших уровень гемоглобина ниже 90 г/л.
Согласно рекомендациям [1], если в первые 6 часов проведения жидкостной ресусцитации при тяжелом сепсисе или септическом шоке показатели центральной венозной сатурации (ScVO2) или смешанной венозной сатурации (sVO2) составляют 70 или 65 % соответственно и не достигается целевое центральное венозное давление, необходимо произвести гемотрансфузию для достижения уровня Ht і 0,30 л/л и/или подключить инфузию добутамина для достижения целевого значения (2С).
При наличии признаков тканевой гипоперфузии, в отсутствие других причин (ишемия миокарда, тяжелая гипоксемия, острая кровопотеря, лактат-ацидоз) рекомендуется проведение гемотрансфузии при снижении уровня гемоглобина < 70 г/л для достижения целевого значения гемоглобина 70–90 г/л у взрослых (1В).
СОЛП/ОРДС. Необходимо избегать проведения гемотрансфузии у пациентов с высоким риском развития синдрома острого легочного повреждения/острого респираторного дистресс-синдрома (СОЛП/ОРДС) (уровень 2). В исследовании TRICC было показано, что риск развития ОРДС был выше у пациентов с либеральной трансфузионной стратегией (11,4 %) в сравнении с рестриктивной (7,7 %) [18]. В другом исследовании из 688 пациентов с ОРИТ и сепсисом, политравмой, аспирацией или массивными гемотрансфузиями у 221 пациента (32 %) развился ОРДС с уровнем летальности на 60-й день, достигающим 46 %. Причем среди предикторов развития ОРДС в данной группе пациентов было и проведение гемотрансфузии.
Проведение гемотрансфузии ассоциировалось с повышением летальности при ОРДС и достоверно носило дозозависимый характер. Таким образом, в результате проведенного исследования гемотрансфузия ассоциировалась как с увеличением риска развития, так и повышением уровня летальности в случае манифестации ОРДС [26].
Отдельно стоит вопрос о связи между гемотрансфузией и развитием СОЛП/ОРДС у пациентов с политравмой. Так, в проспективном когортном исследовании 102 пациентов с ОРИТ и политравмой было показано, что при переливании в первые 24 часа с момента травмы от 0 до 5 единиц эритроцитной среды развитие СОЛП/ОРДС имело место в 21 % случаев, 6–10 единиц — в 31 %, а при переливании более 10 единиц — в 57 % случаев.
Таким образом, гемотрансфузия является независимым фактором риска развития СОЛП/ОРДС. Гемотрансфузия также является независимым фактором риска развития нозокомиальных инфекций, СПОН и SIRS, особенно у больных с политравмой [1].
В заключение необходимо отметить, что, как видно из вышеизложенного, на данный момент нет абсолютно четких рекомендаций проведения гемотрансфузии при тех или иных критических состояниях, а целый ряд вопросов носит дискутабельный характер. Однако в постоянно развивающемся и меняющемся мире представлений о современной реаниматологии все-таки необходимо осмысленно руководствоваться теми ориентирами, которые были представлены в настоящих рекомендациях.
1. Napolitano L.M., Kurek S., Luchette F.A et al. Clinical practice guidelines: Red blood cell transfusion in adult trauma and critical care // Critical Care Medicine. — 2009. — V. 37. — P. 3124-3157.
2. Vincent J.L., Sark Y., Sprung C. et al. Are blood transfusion associated with greater mortality rates? Results of Sepsis Occurrence in Acutely Ill Patients study // Anaesthesiology. — 2008. — V. 108. — P. 31-39.
3. Марино П. Интенсивная терапия. — М.: ГЭОТАР-Медиа, 2010. — 768 с.
4. Napolitano L.M., Corwin H.L. Efficacy of RBC transfusion in the critically ill // Critical Care Clin. — 2004. — V. 20. — P. 255-268.
5. Vincent J.L., Sark Y., DeBacker D. et al. Efficacy of allogenic RBC transfusions. // Pract. Res. Clin. Anaesthesiol. — 2007. — V. 21. — P. 209-219.
6. Fernandes C.J., Akamine N., DeMarco F.V. et al. RBC transfusion does not increase oxygen consumption in critically ill septic patients // Critical Care. — 2001. — V. 5. — P. 362-367.
7. Симбирцев С.А., Беляков Н.А. Микроэмболия легких. — М.: Медицина, 1986. — 216 с.
8. Рябов Г.А. Гипоксия критических состояний. — М.: Медицина, 1988. — 288 с.
9. Кемминг Г. Анемия в интенсивной терапии: лечить или выжидать? // Актуальные проблемы анестезиологии и реаниматологии. Освежающий курс лекций 1991–2006. Особая папка. — Архангельск, 2007. — С. 170-175.
10. Воробьев А.И. Острая массивная кровопотеря // Иваницкий Г.Р., Жибурт Е.Б., Маевский Е.И. (Ред.) Перфторуглеродные соединения в биологии и медицине. — Пущино, 2003. — С. 9-13.
11. Жибурт Е.Б., Шестаков Е.А., Клюева Е.А., Коденев А.Т., Губанова М.Н., Караваев А.В. Правила назначения компонентов крови // Украинский журнал экстремальной медицины. — 2010. — № 2. — С. 17-19.
12. Коваленко А.Б., Корж Ю.Б. Качественный подход в получении компонентов крови // Украинский журнал экстремальной медицины. — 2010. — № 2. — С. 24-27.
13. Napolitano L.M., Corwin H.L., Fink M.P. Anemia in critical care: Etiology, treatment and prevention // Critical Care. — 2004. — V. 8 (Supp. 2). — P. S1-S64.
14. Weiss G., Goodnough L.T. Anemia of chronic disease // N. Engl. J. Med. — 2005. — V. 352. — P. 1011-1023.
15. Sihler K.C., Napolitano L.M. Anemia of inflammation in critically ill patients // J. Intensive Care Med. — 2008. — V. 23. — P. 295-302.
16. Walsh T.S., Saleh E.E. Anaemia during critical illness // Br. J. Anaesth. — 2006. — V. 97. — P. 278-291.
17. Nemeth E. Iron regulation and erythropoiesis // Curr. Opinion Hemathology. — 2008. — V. 15. — P. 169-175.
18. Hebert P.C., Wells G., Blajchman M.A. et al. A multicenter, randomized, controlled clinical trial of transfusion requirements in critical care. Transfusion Requirements in Critical Care Investigation // N. Engl. J. Med. — 1999. — V. 340. — P. 409-417.
19. Luk C.S., Gray-Statchuk L.A, Cepinkas G. et al. WBC reduction reduces storage - associated RBC adhesion to human vascular endothelial cells under conditions of continuous flow in vitro // Transfusion. — 2004. — V. 43. — P. 151-156.
20. Leal-Noval S.R., Munoz-Gomez M., Murillo-Cabezas F. Optimal hemoglobin concentration in patients with subarachnoid hemorrhage, acute ischemic stroke and traumatic brain injury // Current Opinion in Critical Care. — 2008. — V. 14. — P. 156-162.
21. Pendem S., Rana S., Mano E.M., Gajic O. A review of red cell transfusion in the neurological intensive care unit // Neurocritical Care. — 2006. — V. 4. — P. 63-67.
22. Smith M.J., Stiefel M.F., Magge S. et al. Packed erythrocytes transfusion increases local cerebral oxygenation // Critical Care Medicine. — 2005. — V. 33. — P. 1104-1108.
23. Leal-Noval S.R., Rincon-Ferrari M.D., Marin-Niebla A. et al. Transfusion of erythrocyte concentrates produces a variable increment on cerebral oxygenation in patients with severe traumatic brain injury // Intensive Care Medicine. — 2006. — V. 32. — P. 1733-1740.
24. Naidech A.M., Drescher J., Ault M.L. et al. Higher hemoglobin is associated with less cerebral infarction, poor outcome, and death after subarachnoid hemorrhage // Critical Care Medicine. — 2007. — V. 35. — P. 2383-2389.
25. Allport L.E., Parson M.W., Butcher K.S. et al. Elevated hematocrit is associated with reduced reperfusion and tissue survival in acute stroke // Neurology. — 2005. — V. 65. — P. 1382-1387.
26. Gong M.N., Thompson B.T., Williams P. et al. Clinical predictors of and mortality in acute respiratory distress syndrome: Potential role of red cell transfusion // Critical Care Medicine. — 2005. — V. 33. — P. 1191-1198.
