Журнал «Медицина неотложных состояний» 5 (36) 2011
Вернуться к номеру
Применение Глиатилина у больных с тяжелой черепно-мозговой травмой и мозговым инсультом
Авторы: Черний В.И., Колесников А.Н., Дергунов Д.В., Осадчий М.Б., Хайлиулина А.С. Донецкий национальный медицинский университет им. М. Горького КМУ «Клиническая Рудничная больница», г. Макеевка
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Версия для печати
Целью исследования являлось доказательство эффективности применения препарата Глиатилин у больных с острой неврологической и нейрохирургической патологией. В группу исследования было включено 65 пациентов с ишемическим и геморрагическим инсультом, тяжелой ЧМТ, субарахноидальным кровоизлиянием. Благодаря внедрению новых подходов к интенсивной терапии инсультов и тяжелой ЧМТ (Глиатилин) удалось принципиально снизить летальность в данной группе.
Глиатилин, ОНМК, геморрагический инсульт, ишемический инсульт, черепно-мозговая травма, субарахноидальное кровоизлияние.
Введение
В последние годы в отделениях интенсивной терапии (ИТ) наметилась положительная тенденция к снижению летальности у больных нейрохирургической и неврологической групп. Тем не менее летальность остается достаточно высокой [1–9].
Острые нарушения мозгового кровообращения наряду с черепно-мозговой травмой в настоящее время являются одной из ведущих причин летальности и инвалидизации больных неврологического профиля. На экономически развитые страны приходится 1/3 всех случаев нарушения мозгового кровообращения [8, 9].
Смертность (в сроки до 30 суток с момента развития заболевания) при ишемическом инсульте составляет 8–20 %, субарахноидальном кровоизлиянии (САК) — 42–46 %, внутримозговом кровоизлиянии — 48–82 % [20–25].
Гипоксия, следующая за прекращением кровотока, приводит к разрушению мембран и истощению энергетических ресурсов, к многочисленным функциональным и морфологическим повреждениям клеток. Поэтому приоритетной задачей для исследователей является поиск методов, увеличивающих толерантность мозгового вещества к гипоксическому повреждению. Подтверждение способности фосфолипидов и деацитилированных фосфолипидов поддерживать целостность мембран нервных клеток путем восстановления синтеза фосфолипидов и нейротрансмиттера ацетилхолина в поврежденном мозге стало основанием в предположении, что эти соединения могут использоваться в качестве нейрозащитных агентов. Именно поэтому центральные холиномиметики (Глиатилин, холина альфосцерат), являясь источниками холина и фосфатидилхолина, поддерживая физиологический уровень ацетилхолина, обладают мембраностабилизирующими свойствами, служат средствами, восстанавливающими межнейрональную трансмиссию.
Глиатилин (L-a-глицерилфосфорилхолин) как полусинтетическое производное фосфатидилхолина является относительно новым холинергическим препаратом. Доклинические исследования показали, что это вещество увеличивает высвобождение ацетилхолина в гиппокампе у крыс [39] и тем самым способствует обучению и улучшению памяти у подопытных животных [40], способствует преобразованию импульсов в головном мозге [41], а также снижает возрастные структурные изменения в лобных долях и гиппокампе у крыс [42]. Этот препарат также облегчает процесс синтеза фосфолипидов и глицеролипидов клеточных мембран, повышая степень их текучести [43]. С функциональной точки зрения Глиатилин оказывает положительное воздействие на когнитивные расстройства при экспериментальном моделировании процессов старения в головном мозге [44, 45], а также компенсирует расстройства памяти, вызванные приемом скополамина [39, 40]. На основании приведенных выше данных было установлено парасимпатомиметическое действие холина альфосцерата, что оправдывает его клиническое применение для лечения пациентов с острой церебральной недостаточностью (ОЦН) и страдающих когнитивными расстройствами. Исходя из механизма его действия, холина альфосцерат был отнесен к парасимпатомиметикам центрального действия как в международных стандартах на лекарственные препараты [46], так и в Международном классификаторе болезней.
Глиатилин противодействует биохимическому и функциональному дефициту холинергической системы, подвергшейся влиянию ишемии, что обосновывает его применение при острых нарушениях мозгового кровообращения [16]. Нейропротекторное действие источников экзогенного холина при ишемических повреждениях было доказано для предшественников холина как в доклинических [18, 28, 34], так и в клинических исследованиях [47, 48].
В большинстве работ [20–25] подчеркивается эффективность и дозозависимость терапевтического воздействия. В течение последних двух десятков лет клиническая эффективность и переносимость холина альфосцерата (Глиатилина) была изучена в целом ряде клинических исследований. Наиболее крупное многоцентровое исследование эффективности Глиатилина у пациентов с ишемическим инсультом было проведено в Италии в 176 неврологических центрах с участием 2058 пациентов под руководством проф. С. Барбагалло [15]. Лечение начиналось не позднее 10 дней после начала инсульта или транзиторной ишемической атаки и продолжалось не менее 6 месяцев. Достоверное уменьшение когнитивных и двигательных нарушений наблюдалось уже после первого месяца инъекционной терапии Глиатилином (1000 мг в/м). Все результаты подтверждают эффективность холина альфосцерата при восстановлении неврологических и психических расстройств, являющихся следствием цереброваскулярных нарушений, что было наиболее очевидно (достоверно) к третьему месяцу наблюдений [15, 16, 20, 23, 28–31, 33–36]. Таким образом, по данным литературного поиска, эффективность Глиатилина, обосновывающая его применение в протоколах интенсивной терапии, обусловлена следующими факторами:
— механизм действия препарата обусловлен важностью ацетилхолина как одного из основных медиаторов ЦНС;
— жировой компонент препарата обеспечивает сохранность мембранных структур клетки;
— физиологичность препарата обеспечивает хорошую переносимость и безопасность применения в широком возрастном диапазоне;
— выводится преимущественно через легкие, что снижает нагрузку на почки;
— не содержит компонентов животного происхождения (не может являться источником прионовых инфекций);
— не взаимодействует с другими лекарственными субстанциями;
— Глиатилин является оригинальным продуктом.
Цель работы: исследовать эффективность применения препарата Глиатилин (производитель «Италфармако», Италия) в протоколе лечения больных с острыми нарушениями мозгового кровообращения, тяжелой формой черепно-мозговой травмы, субарахноидальным кровоизлиянием, находившихся на лечении в отделении анестезиологии и ИТ и отделении неврологии КМУ «Клиническая Рудничная больница».
Материалы и методы
Исследование проводится в отделении анестезиологии и ИТ и отделении неврологии КМУ «Клиническая Рудничная больница». Отделение анестезиологии и ИТ является базой кафедры анестезиологии, ИТ, МНС и лабораторной диагностики ФИПО ДонНМУ и в своем составе содержит 6 коек для неотложной помощи пациентам с инсультами. Представлены данные за 2009–2011 гг., когда в протокол лечения пациентов мы начали включать препарат Глиатилин.
В группу 1 исследования включено 65 пациентов, из них 16 — с геморрагическим инсультом, 30 — с ишемическим инсультом, 15 — с тяжелой черепно-мозговой травмой (ТЧМТ), 4 — с субарахноидальным кровоизлиянием. Пациенты вместе с лечением по стандартному протоколу интра- и экстрацеребрального воздействия получали дополнительно препарат Глиатилин («Италфармако»):
— при геморрагическом инсульте и САК наряду со стандартной схемой Глиатилин («Италфармако») по схеме 2000 мг парентерально первые 7 дней, затем перорально 800 мг в течение 50–90 дней;
— при ишемическом инсульте наряду со стандартной схемой Глиатилин («Италфармако») по схеме 2000 мг парентерально первые 10 дней, затем перорально 800 мг в течение 50–90 дней;
— при сочетанной травме наряду со стандартной схемой Глиатилин («Италфармако») по схеме 1000–2000 мг парентерально первые 7 дней, затем перорально 800 мг в течение 30–90 дней.
В группу 2 исследования включено 97 пациентов, из них 27 — с геморрагическим инсультом, 38 — с ишемическим инсультом, 20 — с тяжелой черепно-мозговой травмой, 12 — с субарахноидальным кровоизлиянием. Пациенты получали стандартную терапию согласно протоколу лечения тяжелой ОЦН:
— при геморрагическом инсульте пациенты получали маннит, актовегин, нимотоп, цераксон, L-лизина эсцинат, сеансы гипербарической оксигенации (ГБО);
— при ишемическом инсульте пациенты получали латрен, фраксипарин, тиоцетам, сорбилакт, ГЭК, церебролизин, цераксон, актовегин, L-лизина эсцинат;
— при сочетанной травме (тяжелая ЧМТ, субарахноидальное кровоизлияние) пациенты получали лечение согласно протоколам лечения ЧМТ, сеансы ГБО.
Кроме интрацеребрального воздействия, больным обеих групп проводились экстрацеребральные мероприятия, включающие в себя:
— мониторирование витальных функций;
— обеспечение адекватной оксигенации;
— коррекцию показателей гемодинамики;
— адекватную инфузионно-трансфузионную программу;
— коррекцию уровня гликемии;
— нутриционную поддержку;
— коррекцию водно-электролитного баланса;
— нормализацию температуры тела;
— профилактику трофических расстройств;
— профилактическую защиту глаз;
— противосудорожную терапию;
— профилактику развития стрессовых язв в желудочно-кишечном тракте;
— профилактику гнойно-септических осложнений (антибактериальная терапия).
Летальность в группах исследования составила:
Группа 1: ТЧМТ — 3 пациента из 15; геморрагический инсульт — 4 пациента из 16; ишемический инсульт — 4 пациента из 30; САК — 0 из 4 пациентов.
Группа 2: ТЧМТ — 5 пациентов из 20; геморрагический инсульт — 8 пациентов из 27; ишемический инсульт — 7 пациентов из 38; САК — 1 из 12 пациентов.
Дизайн исследования:
— опрос и осмотр больных проводились в первые (162 пациента), третьи (159 пациентов), седьмые (125 пациентов), десятые сутки (105 пациентов), 30-е (86 пациентов), 60-е сутки (52 пациента), 90-е сутки (36 пациентов);
— проводилась оценка согласно шкалам: ШКГ, NIHSS, Barthel, Rankin.
Результаты исследования
Ниже представлены предварительные результаты лечения группы больных, принимавших Глиатилин («Италфармако», Италия).
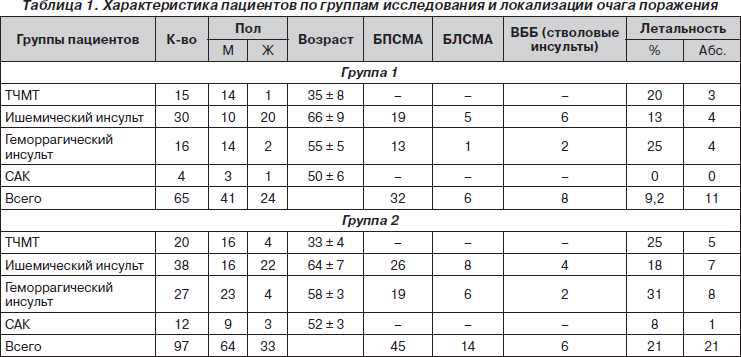
Данные, представленные в табл. 1, позволяют сделать предварительные выводы о распространенности инсульта в мужской (преимущественно геморрагический) и женской (преимущественно ишемический) популяции и о локализации (преимущественно БПСМА) патологического процесса в обеих исследуемых группах. Показатели летальности в группе 1, где в схему стандартной терапии был включен Глиатилин, ниже таковых в группе 2, где применялись только стандартные схемы терапии. Так, по нашим данным, летальность в группе 1 ниже на 5 % у больных с ТЧМТ и на 6 % у больных с геморрагическим инсультом, чем в группе 2. Летальность при ишемическом инсульте в группе 1 также на 5 % ниже, чем в группе 2.
Однако полученные данные можно считать предварительными, так как исследование не закончено. В данной статье представлены пилотные сведения, которые на данном этапе могут показывать лишь тенденцию.
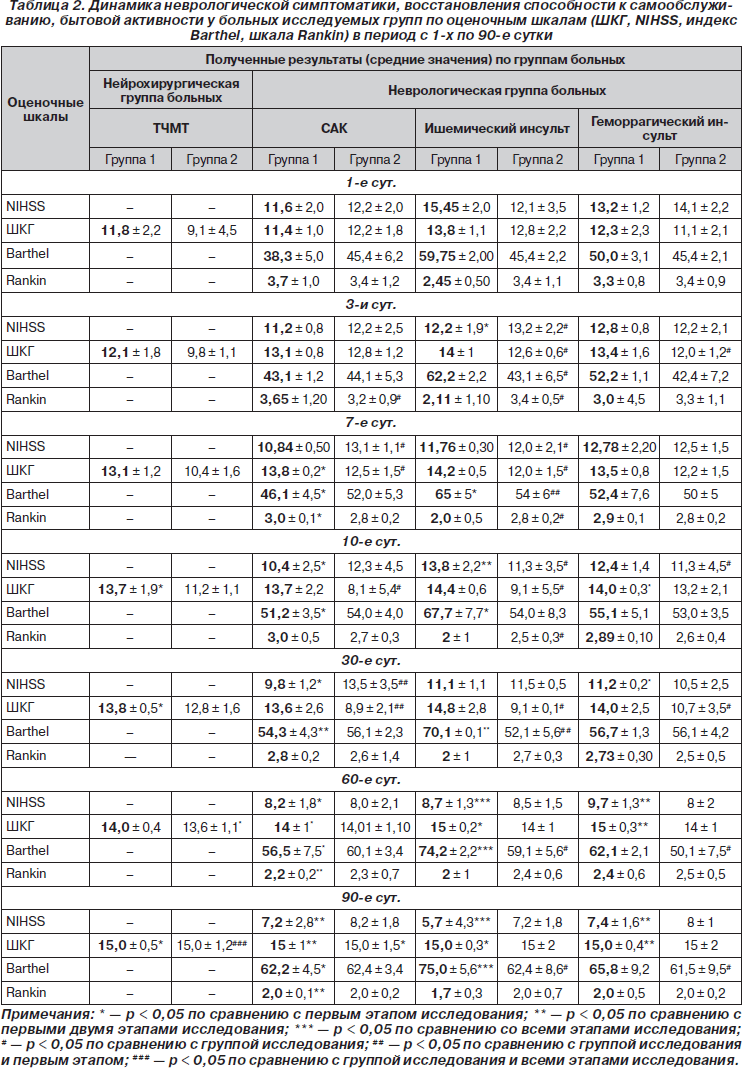
В ходе анализа результатов клинического обследования с использованием ШКГ, NIHSS, индекса Barthel, шкалы Rankin изучались показатели в первые, третьи, седьмые, десятые, тридцатые, шестидесятые и девяностые сутки после дебюта заболевания, а также их динамика (табл. 2).
Для корректности сравнение проводилось с группой пациентов, получавших стандартное лечение, с исходной тяжестью заболевания более 9 баллов по NIHSS.
Оценивая показатели в группе больных с черепно-мозговой травмой, явную положительную динамику в неврологическом статусе можно увидеть уже на 7-е сутки исследования: в группе 1, где использовался Глиатилин, уровень сознания по ШКГ на 7-е сутки наблюдения соответствовал умеренному оглушению, в то время как в группе 2, со стандартным лечением, сознание было на уровне глубокого оглушения — сопора. При этом достоверного отличия динамики неврологического дефицита в исследуемых группах в поздних периодах наблюдения (после 60-х суток) не зарегистрировано. Вероятно, это связано с тем, что регресс очаговых неврологических нарушений в большей степени обусловлен проведением стандартных комплексов физической реабилитации и в меньшей степени зависит от действия исследуемого препарата.
На данном этапе исследования наиболее показательными были данные, полученные в группе с ишемическим инсультом, согласно которым различия в восстановлении между группами были видны уже на 3-и сутки исследования: в группе 1 уже на 3-и сутки у 11 из обследуемых больных регрессировали признаки гемипареза и нарушения чувствительности в конечностях; в свою очередь, в группе 2 подобная динамика прослеживалась в более поздние сроки — к 16–21-м суткам. Что касается способности к самообслуживанию, то в группе 1, где назначался Глиатилин, количество больных с умеренной зависимостью в повседневной деятельности было на 8 % больше, чем в группе 2, со стандартной терапией. Таким образом, на фоне приема Глиатилина позитивная динамика основных неврологических и нейропсихологических параметров была отмечена уже через 3 недели. Применение стандартного курса патогенетической и симптоматической терапии (группа 2) также приводило к положительной динамике показателей, не всегда достигающих устойчивого достоверного отличия от показателей до лечения.
В группах САК и геморрагического инсульта значимый регресс неврологического дефицита на данном этапе исследования наблюдался не ранее 10-х суток. Так, уровень сознания в группе 1 к этому периоду времени по ШКГ был на уровне умеренного оглушения, а в группе 2 — ближе к глубокому оглушению. В отношении способности к самообслуживанию, оценка которой производилась по шкале Бартел на 60–90-е сутки, то в группе 1 отмечалась более значимая положительная динамика в сравнении с группой 2. Так, больные группы 1 к 60-м суткам частично нуждались в некоторой помощи окружающих при выполнении персональной гигиены, приеме пищи, перемещении, в то время как в группе 2 больные полностью зависели от окружающих, а положительная динамика в двигательной активности отмечалась лишь к 90-м суткам наблюдения.
Таким образом, по данным проводимого исследования применение Глиатилина для лечения пациентов неврологической группы (преимущественно ишемический инсульт) способствовало снижению неврологического дефицита и увеличению способности пациентов к самообслуживанию. Так, количество больных с легкими неврологическими нарушениями (NIHSS < 8 б.) к 60-м суткам наблюдения составило 34 % от общего числа больных в группе 2 и 48 % — в группе 1. Количество больных, степень восстановления которых соответствовала умеренной зависимости в выполнении повседневных действий (суммарный балл по шкале Barthel > 75), в группе 1 на 8 % больше, чем в группе 2. Аналогичная картина прослеживается по критериям мобильности больных, их способности к самообслуживанию, бытовой активности (шкала Rankin).
Оценивая предварительные результаты данного исследования, необходимо отметить уникальную способность Глиатилина к ускорению выхода из комы. В наших исследованиях имеются 5 клинических наблюдений, когда пациенты были доставлены из приемного отделения в состоянии комы 1–2 с диагнозом «ишемический инсульт «в ходу». На фоне плановой терапии и внутривенного капельного введения от 1000 до 2000 мг Глиатилина в течение 2–3 часов происходило восстановление сознания до уровня оглушения.
В 4 случаях подобный эффект был отмечен у пациентов с токсической энцефалопатией, поступивших в отделение с диагнозом «отравление неустановленным веществом, кома неясной этиологии».
По нашему мнению, процент положительного ответа на терапию Глиатилином мог бы быть выше при условии транспортировки пациентов в период «терапевтического окна», тогда как большинство пациентов были либо доставлены спустя 10–12 часов с момента первых клинических проявлений, либо переведены в отделение уже в состоянии комы.
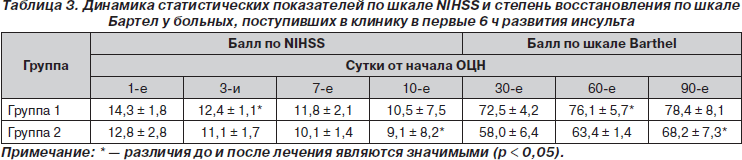
При анализе клинической картины инсульта у пациентов, получавших Глиатилин и включенных в исследование в первые 6 ч, определялся более высокий клинический балл по шкале NIHSS (более тяжелое клиническое состояние) в 1-е и на 3-и сутки инсульта по сравнению с пациентами, получавшими стандартную терапию (табл. 3).
Оценка динамики клинического балла по шкале NIHSS у пациентов, поступивших в клинику в первые 6 ч инсульта, выявила явное значительное опережение восстановления неврологических функций к 30-м суткам заболевания в группе пациентов, получавших Глиатилин, по сравнению с пациентами, получавшими стандартное лечение.
Кроме острого периода церебральной ишемии, у нас имеется положительный клинический опыт (более 10 пациентов) сочетанного применения Глиатилина и ГБО в восстановительном периоде у пациентов с ТЧМТ и пациентов после удачного оперативного удаления внутримозговых гематом.
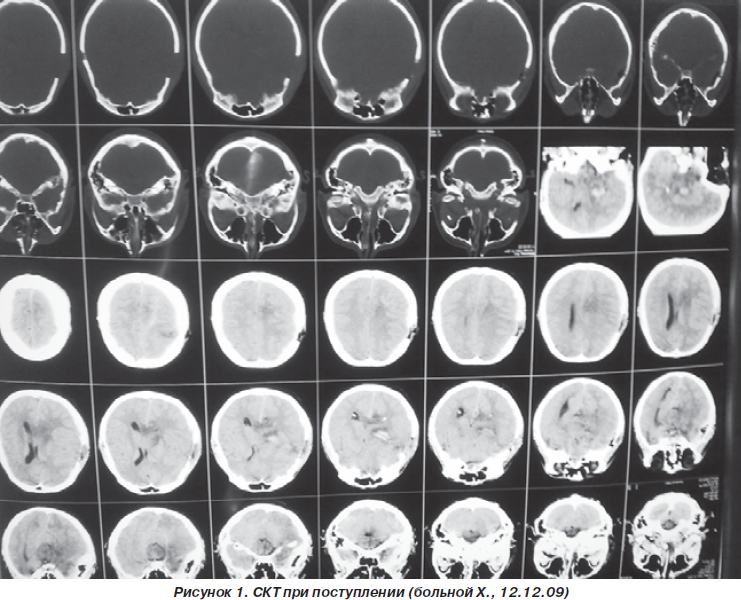
Клинический пример. Больной Х., 25 лет, доставлен в КМУ «Клиническая Рудничная больница» бригадой скорой помощи. Со слов сопровождающих, травма получена 12.12.09 г. около 23.00 на дискотеке в результате падения с высоты (уровня 2-го этажа). При поступлении состояние крайне тяжелое. Сознание отсутствует. Кома 2. Менингеальных знаков нет. Глазные щели закрыты, зрачки — фотореакция отсутствует. Анизокория справа. Сухожильные и периостальные рефлексы равны, снижены, D = S. АД 100/70 мм рт.ст., пульс 50 уд/мин. В лобно-теменной области справа припухлость мягких тканей, выступающая над поверхностью кожи, плотной консистенции, размером 6,0 х 3,0 см. Ушибленная рана затылочной области длиной до 3,0 см. В области правой ключицы — припухлость мягких тканей. На СКТ: отмечается незначительное уменьшение плотности в участках с геморрагическим компонентом (незначительное рассасывание). Сохраняется отек стволовых структур, в височно-затылочных областях справа — признаки масс-эффекта. Контузионный очаг в корковых отделах лобной области справа. Субдуральная гематома?Нельзя исключить наличие диффузионно-аксонального повреждения головного мозга, перелома по типу трещины в теменной области справа (рис. 1).
Диагноз: ЧМТ: ушиб головного мозга. Перелом теменной области по типу трещины со сдавлением внутричерепной гематомой. Ушибленная рана затылочной области, ушиб мягких тканей лобно-теменной области справа. Перелом правой ключицы.
Операция: КРТ черепа справа с удалением субдуральной и эпидуральной гематом, лечебно-диагностическое трепанационное отверстие слева по поводу сочетанной ЧМТ — ушиба головного мозга тяжелой степени, острых субдуральных и эпидуральных гематом справа, перелома свода с переходом на основание черепа в теменно-височной области справа, отека головного мозга, ушибленной раны затылочной области.
Анестезия: ТВА с ИВЛ (модификация стресс-лимитирующей анестезии): пропофол 2 мг/кг/ч + кетамин 1 мг/кг/ч + фентанил 0,05 мг/кг/ч + натрия оксибутират 100 мг/кг/ч.
Инфузионная терапия: 1100 мл (NaCl 0,9% 200 мл, гекодез 500 мл, альбумин 10% 100,0, маннит 100,0, L-лизина эсцинат 10,0 + реосорбилакт 200,0 перед вскрытием ТМО). АД стабильное: 110/70 — 100/60 мм рт.ст. в течение операции, ЧСС с тенденцией к брадикардии до 40 в минуту, стабилизировалась после вскрытия ТМО на уровне 78–82 уд/мин. Диурез 2500 мл.
Переведен в ОАИТ из операционной НХО. Состояние больного тяжелое. Сознание отсутствует — кома 2–3. Менингеальный синдром выражен умеренно. Сухожильные рефлексы с конечностей S > D, снижены. Зрачки D = S, взгляд фиксирован вправо и вверх. Фотореакция отсутствует. Симптом Бабинского вызывается с 2 сторон. Мышечная гипотония, гипорефлексия. Асептическая повязка, дренаж функционирует.
Кожные покровы бледно-розовые, сухие, теплые. Спонтанное дыхание отсутствует, проводится ИВЛ аппаратом Raphael в режиме нормовентиляции. Аускультативно в легких везикулярное дыхание с жестким оттенком. Системное кровообращение субкомпенсировано. Пульс мягкий, 96 уд/мин. АД 105/70 мм рт.ст.
Учитывая оценку по шкале ком Глазго 3–4 балла, в ОРИТ начата интенсивная терапия, включающая:
— краниоцеребральную гипотермию в течение всего первого периода заболевания (15 суток);
— антибиотикотерапию: нетромицин 1,0 х 2 р/сут, тиментин 3,2 х 3 р/сут (смена на меронем);
— первичную нейропротекцию: нимотоп постоянно капельно с помощью инфузионного насоса в начальной дозировке 0,5–1 мг/ч, актовегин 20% 200 мл, L-лизина эсцинат 5,0 мл 3 р/сут;
— посиндромную терапию: гордокс 100 тыс. КИЕД 3 р/сут; противоотечную терапию: маннит 200 мл, альбумин 10% 200 мл; квамател 20 мг; дицинон 4 мл 3 р/сут; дексалгин 2 мл 3 р/сут; лазолван 2 мл 4 р/сут; энтеральное питание — берламин.
По мере улучшения состояния пациента проводилось расширение нейропротекторной терапии. С 10-х суток терапии: Глиатилин 2000 мг/сут + ГБО.
Лечение проводилось в «мягких» режимах, один сеанс в сутки:
1-й с. — 1,2 ата, компрессия 5–7 мин, изопрессия 30 мин, декомпрессия 15 мин.
2-й с. — 1,2 ата, компрессия 5–7 мин, изопрессия 40 мин, декомпрессия 15 мин.
3-й с. — 1,3 ата, компрессия 5–7 мин, изопрессия 40 мин, декомпрессия 15 мин.
4–8-й с. — 1,4 ата, компрессия 7–10 мин, изопрессия 40 мин, декомпрессия 15 мин.
9-й с. — 1,3 ата, компрессия 5–7 мин, изопрессия 40 мин, декомпрессия 15 мин.
10-й с. — 1,2 ата, компрессия 5–7 мин, изопрессия 40 мин, декомпрессия 15 мин.
Обращаем внимание на пролонгированную декомпрессию, которая сохранялась таковой на протяжении всего периода лечения. После сеанса ГБО больному проводилась ингаляция кислорода на протяжении не менее 1–1,5 часа, периодически на фоне непродолжительной ИВЛ (15–20 мин). Преследовалась цель улучшить дренаж и санацию трахеобронхиального дерева. Уже после первого сеанса уменьшился птоз. К 3–5-му сеансу мокрота приобрела жидкую консистенцию слизистого характера, легко откашливалась, не возникало проблем с санацией. Активные движения в нижних конечностях появились к 4–5-му сеансу.
Обращало на себя внимание, что на фоне сеансов ГБО и применения Глиатилина был достигнут значительный и быстрый прогресс в улучшении общего состояния пациента. Более всего произвело впечатление то, что после второго сеанса ГБО пациент открыл глаза и четко ответил на вопросы.
Выписан из ОАИТ 26.01.10 (45-е сутки) в 14.00. Продолжает болеть, госпитализирован в нейрохирургическое отделение КМУ «Клиническая Рудничная больница». Из нейрохирургического отделения выписан на 64-е сутки, переведен в центр реабилитации. При выписке: в сознании, адекватен, самостоятельно садится и стоит, ходит с поддержкой. Активно разговаривает, вспомнил все подробности своей жизни, самостоятельно переключает программы пультом дистанционного управления телевизора, вспомнил пароль на «Одноклассниках».
Таким образом, применение Глиатилина для лечения пациентов неврологической группы способствует восстановлению сознания, уменьшению неврологического дефицита и увеличению способности пациентов к самообслуживанию.
В частности, раннее и своевременное начало нейропротективной терапии обеспечивает ускорение выхода из комы; восстановление уровня сознания; ускорение отмены протезирования жизненно важных функций; увеличение двигательной активности пациентов.
Применение Глиатилина у больных нейрохирургической группы способствует более раннему по сравнению с контрольной группой выходу из комы и более полному восстановлению уровня сознания, а также усилению скорости линейного кровотока на пораженной стороне, при условии сохранения ауторегуляции мозгового кровообращения. Глиатилин способствует увеличению выживаемости и снижению инвалидизации больных.
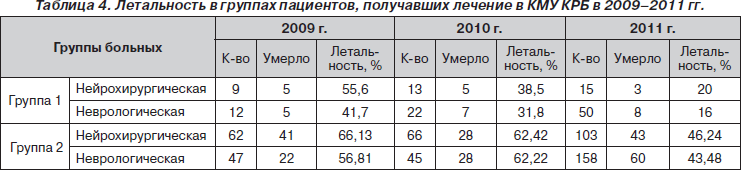
В целом применение современной стратегии нейропротекции и своевременное сочетание нейропротекторных мероприятий и препаратов позволили снизить летальность в отделении ИТ (табл. 4).
Оценивая в целом показатели летальности пациентов, можно отметить положительную динамику по снижению летальности, что связано в основном с более четким соблюдением протоколов, прежде всего экстрацеребрального воздействия. Положительный эффект в группах пациентов с применением Глиатилина отмечен у пациентов, поступивших в период «терапевтического окна». У пациентов с длительным периодом отсутствия терапии, как правило, Глиатилин назначали не ранее 10–14-х суток, по мере регрессирования неврологического дефицита.
Выводы
1. Включение препарата Глиатилин («Италфармако») в стандартную схему позволило снизить летальность в неврологической и нейрохирургической группах на 26,78 и 26,24 % соответственно.
2. При оценке динамики неврологических проявлений по шкале NIHSS выявлен регресс признаков когнитивных и очаговых нарушений: суммарный балл во всех трех группах больных снизился с уровня значительного (14 баллов) и умеренно выраженного дефицита до легкого (< 8 баллов).
3. Согласно шкале Рэнкина, больные группы 1 к 90-м суткам наблюдения имели легкие признаки инвалидности, были в состоянии ухаживать за собой без посторонней помощи. У больных в группе 2 наблюдалась менее прогрессивная динамика, отмечались умеренно выраженные признаки инвалидности, больные нуждались в некоторой посторонней помощи при одевании, гигиеническом уходе за собой.
4. В ходе терапии Глиатилином наиболее значимая положительная динамика неврологического дефицита прослеживается в остром периоде церебральной ишемии.
5. Перспективно для реабилитационных мероприятий сочетание нейропротекции (Глиатилин) и гипербарической оксигенации.
1. Верещагин Н.В., Пирадов М.А. Принципы ведения и лечения больных в острейшем периоде инсульта // Интенсивная терапия острых нарушений мозгового кровообращения. — Орел, 1997. — С. 3-11.
2. Виленский Б.С. Инсульт: профилактика, диагностика и лечение. — СПб.: Фолиант, 2002. — 397 с.
3. Виленский Б.С. Современная тактика борьбы с инсультом. — СПб.: Фолинат, 2005. — 288 с.
4. Вознюк И.А., Голохвастов С.Ю., Фокин В.А. и др. Нарушения церебрального кровотока и перфузионные расстройства в остром периоде ишемического инсульта // Инсульт (приложение к Журналу неврологии и психиатрии им. С.С. Корсакова). — 2007. — Спец. выпуск. — С. 242-243.
5. Гусев Е.И., Скворцова В.И. Ишемия головного мозга. — М.: Медицина, 2001. — 327 с.
6. Инсульт: диагностика, лечение, профилактика / Под ред. З.А. Суслиной, М.А. Пирадова. — М.: МЕДпресс-информ, 2008. — 283 с.
7. Одинак М.М., Вознюк И.А. Новое в терапии при острой и хронической патологии мозга. — СПб.: ВМедА, 2000. — 31 с.
8. Одинак М.М., Вознюк И.А., Янишевский С.Н. Ишемия мозга (нейропротективная терапия, дифференцированный подход). — СПб.: ВМедА, 2002. — 75 с.
9. Одинак М.М., Вознюк И.А. Ишемия мозга — преемственность в решении проблемы // Мед. акад. журн. — 2006. — Т. 6, № 3. — С. 88-94.
10. Одинак М.М., Вознюк И.А., Голохвастов С.Ю. и др. Мониторинг перфузионных нарушений в острейшую стадию ишемического инсульта // Вестн. Рос. воен.-мед. акад. — 2005. — № 2. — С. 25-30.
11. Одинак М.М., Вознюк И.А., Голохвастов С.Ю. и др. Особенности ранней нейровизуализационной диагностики при острых нарушениях мозгового кровообращения // Регионарное кровообращение и микроциркуляция. — 2007. — № 1(21). — С. 113-114.
12. Одинак М.М., Вознюк И.А., Янишевский С.Н. Инсульт. Вопросы этиологии, патогенеза. Алгоритмы диагностики и терапии. — СПб.: ВМедА, 2005. — 192 с.
13. Труфанов Г.Е., Одинак М.М., Фокин В.А. Магнитно-резонансная томография в диагностике ишемического инсульта. — СПб.: ЭЛБИ-СПб, 2008. — 271 с.
14. Труфанов Г.Е., Фокин В.А., Пьянов И.В. и др. Рентгеновская компьютерная и магнитно-резонансная томография в диагностике ишемического инсульта. — СПб.: ЭЛБИ-СПб, 2005. — 192 с.
15. Barbagallo S.G., Barbagallo M., Giordano M. et al. a-Glycerophosphocholine in the mental recovery of cerebral ischemic attacks. An Italian multicenter clinical trial // Pharmacology of Aging Process (Annals of the New York Academy of Sciences). — 1994. — Vol. 717. — P. 253-269.
16. Bergamaschi M., Piccolo O. Deacylated phospholipids: Chemistry and therapeutic potential // Phospholipids: characterization, metabolism, and novel biological applications / G. Cvec, F. Paltauf. — USA: AOCS Press, 1995. — Р. 228-247.
17. Blusztajn J.K., Wurtman R.J. Choline and cholinergic neurons // Science. — 1983. — 221. — 19-22.
18. Casamenti F., Mantovani P., Amaducci L., Pepeu G. Effect of phosphatidylserine on Ach output from the cerebral cortex of the rat // J. Neurochem. — 1979. — 32. — 529-533.
19. Clark W.M., Wissman S., Albers G.W. et al. Recombinant Tissue-Type Plasminogen Activator (Alteplase) for Ischemic Stroke 3 to 5 Hours After Symptom Onset. The ATLANTIS Study // J. Am. Med. Association. — 1999. — Vol. 282, № 21. — P. 2019-2026.
20. D’Orlando J.K., Sandage B.W. Citicoline (CDP-choline): mechanism of action and effects in ischemic brain injury // Neurol. Res. — 1995. — 17. — 281-284.
21. Delwaide P.J., Gyeselynck A.M., Hurlet A., Ylieff M. Double-blind randomized controlled study of phosphatidylserine in senile patients // Acta Neurol. Scand. — 1986. — 73. — 136-140.
22. Dorman P.J., Sandercock P.A. Considerations in the design of clinical trials of neuroprotective therapy in acute stroke // Stroke. — 1996, Sep. — 27(9). — 1507-15.
23. Dross K., Kevitz H. Concentration and origin of choline in the rat brain // N.S. Arch. Pharmacol. — 1972. — 274. — 91-10.
24. Fisher M., Takano K. The penumbra, therapeutic time window and acute ischemic stroke // Baillieres Clin. Neurol. — 1995. — Vоl. 4, № 2. — P. 279-295.
25. Flentge F., Van Der Berg C.J. Choline administration and Ach in brain // J. Neurochem. — 1979. — 32. — 1331-1333.
26. Freeman J.J., Jenden D.J. The source of choline for Ach synthesis in brain // Life Science. — 1976. — 19. — 949-962.
27. Heiss W.-D. Detection of the penumbra as a rationale for therapy of ischemic stroke // Журн. неврол. и психиат. (приложение «Инсульт»). — 2003. — 9. — 13-15.
28. Jope R.S. Effects of phosphatidylcholine administration to rats on choline in blood and choline and Ach in brain // JPET. — 1982. — 220. — 322-328.
29. Jope R.S., Jenden D.J. Choline and phospholipid metabolism and synthesis of Ach in rat brain // J. Neuroscience Res. — 1979. — 4. — 69-82.
30. Loffelholtz K. Receptor regulation of choline phospholipid hydrolysis // Biochemical Pharmacol. — 1989. — 38. — 1543-1544.
31. Sandage Jr. et al. Reduction of infarct volume using citicoline // United States Patient. — Feb. 16, 1999. — 5, 872, 108.
32. Schehr R.S. New treatments for acute stroke // Nature Biotechnology. — 1996. — 14. — 1549-1554.
33. Schmidt D.E, Wecker L. CNS effects of choline administration: evidence for temporal dependence // Neuropharmacology. — 1981. — 20. — 535-539.
34. Secades J.J., Frontera G. CDP-choline: Pharmacological and clinical review // Methods Find Exp. Clin. Pharmacol. — 1995. — 17 (Suppl B). — 2-54.
35. Studies on the pharmacological and biochemical effects of alfa-glycerylphosphorylcholine in experimental animals. Report from Shionogy Research Laboratories.
36. Tommasina C., Manzino M., Novello P., Pastorino P. Studio clinico dell’efficacia terapeutica e della tollerabilitа della colina alfoscerato in 15 soggetti con compromissione delle funzioni cognitive successiva ad ischemia cerebrale focale acuta // Rivista di Neuropsichiatria e Scienze Affini. — 1991. — 37. — 21-28.
37. Wurtmann R.J., Heftl F., Melamed E. Precursor control of neurotransmitter synthesis // Pharmacological. Rev. — 1981. — 32. — 31-335.
38. Warach S., Pettigrew L.C., Dashe J.F. et al. Effect of citicoline on ischemic lesions as measured by diffusion-weighted magnetic resonance imaging. Citicoline 010 Investigators // Ann. Neurol. — 2000, Nov. — 48(5). — 713-22.
39. Sigala S., Imperato A., Rizzonelli P., Casolini P., Missale C., Spano P.F. L-alpha-glycerylphosphorylcholine antagonizes scopolamine-induced amnesia and enhances hippocampal cholinergic transmission in the rat // Eur. J. Pharmacol. — 1992. — 21. — 351-358.
40. Govoni S., Lopez C., Battaini F., Longoni A., Trabucchi M. Effetti di GFC sul comportamento di evitamento passivo del ratto e sui livelli di acetilcolina // Basi. Raz. Ter. — 1990. — 20. — 55-60.
41. Schettini G., Florio T., Ventra C., Grimaldi M., Meucci O., Landolfi E., Effetto del trattamento in vivo con GFC (colina alfoscerato) sull’attivita` dei sistemi di trasduzione a livello cerebrale // Basi. Raz. Ter. — 1990. — 20. — 23-30.
42. Amenta F., Franch F., Ricci A., Vega J.A. Cholinergic neurotransmission in the hippocampus of aged rats: influence of L-alpha-glycerylphosphorylcholine treatment // Ann. N.Y. Acad. Sci. — 1993. — 695. — 311-313.
43. Aleppo G., Nicoletti F., Sortino M.A., Casabona G., Scapagnini U., Canonico P.L. Chronic L-glycerylphosphorylcholine increases inositol phosphate formation in brain slices and neuronal cultures // Pharmacol. Toxicol. — 1994. — 74. — 95-100.
44. Canonico P.L., Nicoletti F., Scapagnini U. Effetti neurochimici e comportamentali di GFC (colina alfoscerato) // Basi. Raz. Ter. — 1990. — 20. — 53-54.
45. Drago F., Nardo L., Freni V., Spadaro F., Valerio C. Effetti comportamentali di GFC in modelli di invecchiamento cerebrale patologico // Basi. Raz. Ter. — 1990. — 20. — 65-68.
46. Reynolds J.E.F. Parasimpathomimetics // Martindale — The Extra Pharmacopoeia, thirty-first ed. Royal Pharmaceutical Society. — London, 1996. — Р. 1413-1428.
47. Tazaki Y. Treatment of acute cerebral infarction with a choline precursor in a multicenter double blind placebo-controlled study // Stroke. — 1988. — 19. — 211-215.
48. Clark W.M. A randomized dose-response trial of citicholine in acute ischemic stroke patients // Neurology. — 1997. — 49. — 671-678.