Журнал «Медицина неотложных состояний» 5 (36) 2011
Вернуться к номеру
Выявление независимых предикторов рецидива мерцательной аритмии у больных с пароксизмальной и персистирующей формой фибрилляции предсердий
Авторы: Целуйко В.И., Вашакидзе З.С. Харьковская медицинская академия последипломного образования Лучков А.Б. Городская клиническая больница № 8, г. Харьков
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Версия для печати
Проанализированы данные холтеровского мониторирования и эхокардиографии у пациентов с пароксизмальной и персистирующей формой фибрилляции предсердий. Для оценки риска рецидива фибрилляции предсердий установлена прогностическая ценность таких показателей, как среднее и максимальное число сердечных сокращений, суточное количество суправентрикулярных нарушений ритма и групповых наджелудочковых экстрасистол, а также увеличение переднезаднего диаметра левого предсердия, наличие диастолической дисфункции левого желудочка по типу недостаточной релаксации и гипертрофии левого желудочка. Проведенный сравнительный анализ показал, что увеличение числа сердечных сокращений, предсердная эктопическая активность, наличие диастолической дисфункции левого желудочка и увеличение левых отделов сердца являются независимыми факторами риска рецидива фибрилляции предсердий.
Фибрилляция предсердий, диастолическая дисфункция, холтеровское мониторирование ЭКГ, суправентрикулярные нарушения ритма.
Введение
Фибрилляция предсердий (ФП) является самой частой разновидностью аритмий и составляет 1/3 всех случаев обращений в клинику по поводу нарушений сердечного ритма [1]. Основными причинами госпитализаций пациентов с ФП являются рецидивы аритмии, нарушение гемодинамики и тромбоэмболические осложнения, связанные с повторными пароксизмами ФП. Вследствие этого особую актуальность имеет прогнозирование риска возникновения рецидивов ФП [6].
Выявление дополнительных предикторов развития аритмии может позволить рационально и своевременно корректировать терапию у пациентов группы высокого риска.
Согласно сведениям литературы [2, 3], факторами риска возникновения ФП по данным эхокардиографии (ЭхоКГ) являются увеличение размеров левого предсердия (ЛП), снижение фракции выброса (ФВ) левого желудочка (ЛЖ) и его диастолическая дисфункция [8, 9]. Холтеровское мониторирование позволяет значительно чаще, чем стандартная ЭКГ, выявлять нарушения ритма в течение суток, что имеет значение для диагностики непродолжительных, кратковременных, недиагностируемых эпизодов ФП, протекающих малосимптомно [10].
Цель исследования. Оценить значение параметров ЭхоКГ и данных холтеровского мониторирования ЭКГ у больных с пароксизмальной и персистирующей формой фибрилляции предсердий для прогнозирования риска возникновения рецидивов фибрилляции предсердий.
Материалы и методы исследования
Нами было проведено динамическое наблюдение 80 амбулаторных и стационарных больных (54 мужчины и 26 женщин, средний возраст 59,95 ± 1,23 года, с умеренной гипертензией, имеющие в анамнезе пароксизмальную или персистирующую форму ФП и синусовый ритм во время исследования) на базе ГКБ № 8 в 2010 году (в течение 6 месяцев). Критериями исключения были клапанные пороки сердца, размер левого предсердия более 55 мм, острый коронарный синдром, нарушение функции щитовидной железы, онкологические заболевания, сердечная недостаточность III–IV класса (по NYHA). Все пациенты перед включением в исследование и на протяжении всего периода наблюдения получали базисную терапию (гипотензивные препараты, антиаритмики, антикоагулянты при наличии показаний, статины).
Первоначально все пациенты прошли 24-часовой мониторинг ЭКГ и ЭхоКГ по стандартной методике [2].
Для оценки диастолической функции ЛЖ с помощью ЭхоКГ определяли максимальную скорость раннего наполнения (Е) ЛЖ и в систолу предсердий (А), их отношение (Е/А), время замедления скорости раннего диастолического наполнения ЛЖ (DT) и время изоволюметрического расслабления миокарда ЛЖ (IVRT). Тип диастолической дисфункции ЛЖ определяли в соответствии с канадской классификацией [8]. Проводили эхокардиоскопическое обследование на аппарате Sonoscape 5000.
По данным холтеровского мониторирования были проанализированы максимальная, минимальная и средняя частота сердечных сокращений (ЧСС), аритмии и нарушения проводимости. Обследование осуществлялось с помощью 2- и 3-канальных аппаратов INCART (Венгрия). Обработка полученных данных проводилась с унифицированным протоколом с помощью Cardiospy.
Пациенты были под наблюдением в течение 6 мес., у них оценивали наличие пароксизмов ФП, их частоту и продолжительность. Обработку результатов выполняли с использованием пакета статистического анализа Statistica 6.0. При нормальном распределении количественные признаки были представлены в виде среднего ± стандартное отклонение (М ± s), для сравнения средних двух выборок иcпользовали критерий Стьюдента. Различия считали статистически значимым при величине Р < 0,05.
Результаты исследования и их обсуждение
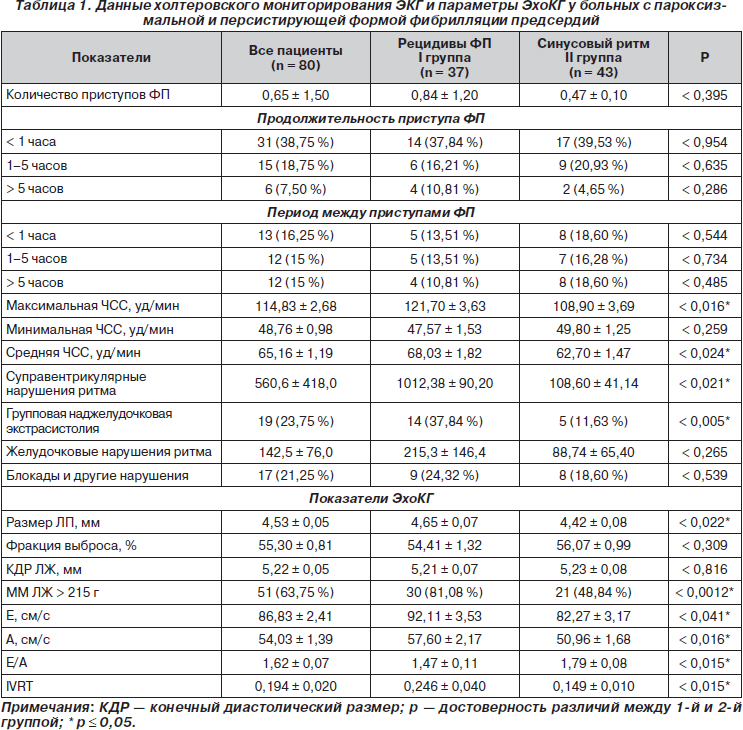
Во время 6-месячного периода наблюдения проводилась регистрация рецидивов фибрилляции предсердий и ее продолжительности. У 37 (46,25 %) больных (1-я группа) отмечался повторный срыв ритма, остальные 43 (53,75 %) пациента (2-я группа) имели синусовый ритм во время всего периода наблюдения. У 7 (8,75 %) больных повторный срыв ритма произошел более чем 2 раза. У больных 1-й группы (рецидивы ФП) количество эпизодов ФП за время наблюдения составило в среднем 2,0 ± 1,2, при этом первый эпизод аритмии развился в среднем через 2,6 ± 1,8 мес. от начала исследования. Результаты представлены в табл. 1.
При оценке параметров трансмитрального кровотока обнаружено значимое (р < 0,041) снижение пика Е, возрастание пика А и уменьшение в результате этого отношения Е/А у пациентов 1-й группы по сравнению со 2-й (табл. 1). Этот тип дисфункции ЛЖ (тип недостаточной релаксации) выявлен у 24 (64,86 %) больных 1-й группы и у 15 (34,88 %) — 2-й. Для стратификации риска рецидивов ФП при анализе параметров ЭхоКГ выявлено, что КДР и ФВ ЛЖ у пациентов 1-й и 2-й групп не различались. У больных 1-й группы диаметр ЛП был достоверно (р < 0,05) больше. При этом величина диаметра ЛП положительно коррелировала с количеством пароксизмов аритмии (p < 0,022).
По данным исходного суточного мониторирования ЭКГ (табл. 1), у пациентов 1-й группы (рецидивы ФП) по сравнению со 2-й (синусовый ритм) достоверно (p < 0,024; p < 0,016) выше были средняя (соответственно 68,03 ± 1,82 и 62,70 ± 1,47 в 1 мин) и максимальная (соответственно 121,70 ± 3,63 и 108,90 ± 3,69 в 1 мин) ЧСС. Cуправентрикулярные экстрасистолы были зарегистрированы у 25 (67,57 %) пациентов 1-й группы (рецидивы ФП) и у 19 (44,19 %) больных 2-й (синусовый ритм). Их количество за сутки было достоверно выше в 1-й группе, чем во 2-й, — соответственно 1012,38 ± 90,20 и 108,60 ± 41,14 (p < 0,021). Парные суправентрикулярные экстрасистолы отмечали у 14 (37,84 %) больных 1-й группы и лишь у 4 (9,3 %) пациентов 2-й (p < 0,005).
Таким образом, достоверными факторами риска повторных пароксизмов фибрилляции предсердий оказались: увеличение переднезаднего диаметра левого предсердия > 4,53 см (станд. откл. 0,05; p < 0,022), наличие диастолической дисфункции левого желудочка по типу недостаточной релаксации и гипертрофии левого желудочка (p < 0,0012), средняя ЧСС > 68 ударов в минуту (станд. откл. 1,82; p < 0,024); максимальная ЧСС > 122 ударов в минуту (станд. откл. 3,63; p < 0,016), 24-часовое количество суправентрикулярных нарушений ритма > 1012 (станд. откл. 90,2; p < 0,021) и групповые наджелудочковые экстрасистолы > 14 (37,84 %) (p < 0,005).
В заключение следует отметить, что увеличение ЧСС и предсердная эктопическая активность являются независимыми факторами риска рецидива фибрилляции предсердий.
Выводы
1. Достоверными предикторами развития рецидивов аритмии являются увеличение переднезаднего диаметра левого предсердия > 4,53 см (p < 0,022), наличие диастолической дисфункции левого желудочка по типу недостаточной релаксации и гипертрофия левого желудочка (p < 0,0012).
2. Высокая частота сокращений сердца и эктопическая активность предсердий являются независимыми факторами риска возникновения рецидивов фибрилляции предсердий (p < 0,016).
3. По данным холтеровского мониторирования ЭКГ, риск возникновения рецидивов фибрилляции предсердий увеличивается при возрастании средней частоты сокращений сердца свыше 68 в 1 мин и максимальной частоты сокращений сердца свыше 122 в 1 мин (p < 0,024; p < 0,016).
4. Дополнительным неблагоприятным прогностическим фактором срыва синусового ритма в ФП, по данным холтеровского мониторирования ЭКГ, является возрастание суточного количества наджелудочковых экстрасистол и эпизодов групповой наджелудочковой эктрасистолии (p < 0,021; p < 0,005).
Определение показателей диастолической функции ЛЖ и холтеровского мониторирования ЭКГ обладает прогностической ценностью и оптимизирует процесс выбора врачебной тактики у пациентов с пароксизмальной и персистирующей формой ФП, что подтверждает перспективность данных методов обследования.
1. Дзяк Г.В. Фибрилляция предсердий // Здоров’я України. Тематичний номер. — 2009, вересень. — С. 15-16.
2. Зотов Д.Д. Современные методы функциональной диагностики в кардиологии / Зотов Д.Д., Гротова А.В. — СПб.: Фолиант, 2002. — С. 119.
3. Свистов А.С. Возможности электрокардиографии высокого разрешения в прогнозировании пароксизмальной фибрилляции предсердий у больных ишемической болезнью сердца / Свистов А.С., Гришаев С.Л., Солнцев В.Н. и др. // Вестник аритмологии. — 2005. — № 37. — С. 25-31.
4. Arriagada G. Predictors of arrhythmia recurrence in patients with lone atrial fibrillation / Arriagada G., Berruezo A., Mont L. et al. // Europace. — 2008. — Vol. 10. — P. 9-14.
5. Devereux R.B. Echocardiographic assessment of left ventricular hypertrophy: comparison to necropsy findings / Devereux R.B., Alonso D.R., Lutas E.M. et al. // Am. J. Cardiol. — 1986. — Vol. 57. — P. 450-458.
6. John Camm A. ACC/AHA/ESC guidelines for the management of atrial fibrillation/ A. John Camm, Kirchhof Р., Gregory Y.H. Lip. et al. // Eur. Heart J. — 2010. — Vol. 31. — P. 2369-2429.
7. Materazzoa C. Atrial fibrillation after non-cardiac surgery: P-wave characteristics and Holter monitoring in risk assessment / Materazzoa C., Piottia P., Mantovania C. et al. // Eur. J. Cardiothorac. Surg. — 2007. — Vol. 31. — P. 812-816.
8. Rakovsky H. Canadian consensus recommendation for the measurement and reporting of diastolic dysfunction in echocardiography / Rakovsky H., Appleton C., Chan K. et al. // J. Am. Soc. Echocardiogr. — 1996. — Vol. 9. — P.736- 760.
9. Sherif F. Nagueh. EAE/ASE (European Association of Echocardiography, a branch of the European Society of Cardiology) RECOMMENDATIONS 2009 Recommendations for the Evaluation of Left Ventricular Diastolic Function by Echocardiography / Sherif F. Nagueh, Christopher P. Appleton, Thierry C. Gillebert // European Journal of Echocardiography. — 2009. — 10. — 165-193.
10. Vincenti A. Onset mechanism of paroxysmal atrial fibrillation detected by ambulatory Holter monitoring / Vincenti A., Brambilla R., Fumagalli M.G. et al. // Europace. — 2006. — Vol. 8. — P. 204-210.