Журнал «Медицина неотложных состояний» 7-8 (38-39) 2011
Вернуться к номеру
Интенсивная терапия тяжелого сепсиса и септического шока с учетом рекомендаций экспертов Движения за выживаемость при сепсисе
Авторы: Курсов С.В., Михневич К.Г. Харьковский национальный медицинский университет
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Версия для печати
1. Клинико-физиологические особенности тяжелого сепсиса и септического шока
Септический шок — состояние, включающее в себя два клинических синдрома — сепсис и шок, каждый из которых уже сам по себе является сложным клиническим понятием (как, например, понятие «острый живот» в хирургии). Оба синдрома являются осложнениями различных тяжелых заболеваний, и оба могут осложнять друг друга, многократно утяжеляя состояние пациента.
В 1992 году сепсис был определен как синдром, характеризующийся наличием как инфекции, так и системного воспалительного ответа. В качестве диагностических критериев сепсиса предложены следующие:
1. Клинические признаки:
— температура тела выше 38,3 °C или ниже 36 °C;
— ЧСС > 90 мин‑1 или выше возрастной нормы более чем на 2 стандартных отклонения (s);
— тахипноэ;
— нарушение сознания;
— достоверные отеки или положительный водный баланс более 20 мл/кг∙сут в течение 24 часов и дольше;
— гликемия более 7,7 ммоль/л в отсутствие диабета.
2. Проявления воспаления:
— лейкоцитоз более 12∙109/л или лейкопения менее 4∙109/л;
— нормальное содержание лейкоцитов при количестве юных форм более 10 %;
— C-реактивный белок в плазме на 2s выше нормы;
— прокальцитонин на 2s выше нормы.
3. Гемодинамические показатели:
— АДсист. < 90 мм рт.ст., среднее АД (САД) < 70 мм рт.ст. (или снижение АД более чем на 40 мм рт.ст. от исходного уровня у взрослых или на 2s ниже возрастного уровня);
— SvO2 > 70 % (у взрослых; для детей это норма);
— СИ > 3,5 л/мин∙м2 (у взрослых; у детей СИ = 3,5–5,5 л/мин∙м2)*.
4. Признаки органной дисфункции:
— гипоксемия (paO2/FiO2 < 300);
— острая олигурия (менее 0,5 мл/кг∙ч);
— концентрация креатинина превышает 120 мкмоль/л;
— АЧТВ > 60 с;
— парез кишечника;
— тромбоцитопения (менее 100∙109/л);
— общий билирубин более 70 мкмоль/л.
5. Показатели тканевой перфузии:
— гиперлактатемия более 1 ммоль/л;
— снижение капиллярного наполнения (синдром белого пятна).
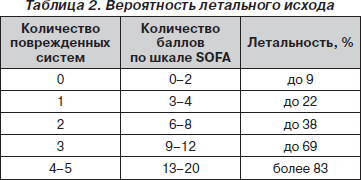
О тяжелом сепсисе говорят, когда на его фоне развивается органная дисфункция. Ее критерии определяются с помощью шкалы SOFA — Sepsis-related Organ Failure Assessment (F.L. Ferreria et al., 2002), принятой Европейским обществом интенсивной медицины (табл. 1).
Нарушение функции каждого органа или системы оценивается отдельно по 4-балльной системе, после чего баллы суммируются. По количеству поврежденных систем и сумме баллов можно оценить вероятность летального исхода (табл. 2).
Шоком называют такое критическое состояние, которое развивается вследствие гипоперфузии тканей как результата острой недостаточности кровообращения и характеризуется рядом синдромов, основными из которых являются гиповолемия, централизация кровообращения, полиорганная недостаточность (ПОН), нарушения реологических свойств крови, коагулопатия с развитием синдрома рассеянного внутрисосудистого свертывания и тромбогеморрагического синдрома, секвестрация крови в капиллярах и генерализованный протеолиз. В зависимости от первичной причины снижения сердечного выброса выделяют кардиогенный, гиповолемический и дистрибутивный виды шока.
Септический шок имеет черты всех видов шока, поскольку сам сепсис приводит к ПОН, однако его принято относить к группе дистрибутивных шоков (относительно недавно септический шок представлял отдельный, четвертый вид шока), поскольку одним из звеньев септического шока является увеличение под действием микробных токсинов объема артериоловенулярных шунтов, которое и приводит к гипоперфузии тканей. На начальных стадиях при этом сердечный выброс часто повышен, что клинически проявляется так называемой теплой фазой шока, особенно характерной для грамположительного (экзотоксического) сепсиса.
Клинически диагноз «септический шок» ставится при наличии острой недостаточности кровообращения с персистирующей артериальной гипотензией: АДсист. < < 90 мм рт.ст., САД меньше исходного на 40 мм рт.ст. и более при отсутствии других видимых причин гипотензии и несмотря на адекватное восполнение дефицита ОЦК.
Таким образом, учитывая общность многих механизмов сепсиса и шока, сепсис, тяжелый сепсис и септический шок можно рассматривать как последовательные стадии одного заболевания, проявляющегося комплексом изменений витальных функций, лабораторных показателей и сопровождающегося гипоперфузией тканей и ПОН.
Синдром полиорганной недостаточности (СПОН) является следствием острого повреждения органов и систем медиаторами критического состояния, когда организм не может поддерживать гомеостаз. Выделяют следующие механизмы СПОН (R. Cook et al., 2001):
— медиаторный — аутоиммунное поражение;
— микроциркуляторно-реперфузионный;
— инфекционно-септический (представление о кишечнике как о недренированном абсцессе);
— феномен двойного удара.
Медиаторный механизмсвязан с повреждением эндотелия и гиперпродукцией цитокинов.
Эндотелий является органом со специфическими анатомо-физиологическими особенностями в зависимости от тканей, в которых он расположен, и выполняет общие функции во всем организме. Эти функции следующие:
— изменение проницаемости сосудистой стенки для обмена водой и растворенными в ней веществами между кровотоком и тканями;
— регуляция просвета сосудов путем выработки сосудорасширяющих и сосудосуживающих веществ;
— участие в работе системы регуляции агрегатного состояния крови и в атерогенезе;
— участие в адгезии, агрегации и трансформации клеток крови;
— участие в аутоиммунных реакциях.
Цитокины — это низкомолекулярные белковые медиаторы, вырабатываемые у здоровых людей в ничтожных количествах, с помощью которых различные клетки (эндотелий, лейкоциты, фибробласты и другие) «общаются» между собой, регулируя работу друг друга. В этом цитокины сходны с гормонами. Действие цитокинов опосредуется специфическими рецепторами, расположенными на клеточных мембранах. По воздействию на клетки выделяют 5 классов цитокинов:
— интерлейкины;
— фактор некроза опухоли a (TNF-a);
— факторы роста и дифференцировки лимфоцитов;
— факторы, стимулирующие рост колоний макрофагов и гранулоцитов;
— факторы, вызывающие рост мезенхимальных клеток.
Основными функциями цитокинов являются:
— участие в воспалении;
— участие в росте и дифференцировке отдельных клеток;
— воздействие на опухолевый рост;
— обеспечение иммунной защиты;
— участие в регенерации поврежденных тканей.
Участие цитокинов в воспалении регулируется белком, называемым ядерным фактором kB (каппа Б).
Гиперпродукция цитокинов приводит к срыву саморегуляции, для которого характерны следующие явления:
— не просто увеличивается энергопродукция, а происходит «самосжигание» организма;
— воспаление, призванное ограничить повреждающий фактор, переходит в капиллярную утечку жидкости с интерстициальными отеками;
— вместо регенерации тканей и заживления развивается деструкция тканей.
Микроциркуляторно-реперфузионный механизм. Медиаторный механизм приводит к развитию гиповолемического порочного круга, являющегося следствием замедления кровотока, реологических нарушений, агрегации клеток крови, секвестрации крови и капиллярной утечки и приводящего к гипоперфузии тканей. Если адекватная интенсивная терапия восстанавливает перфузию тканей, наступают их реперфузионные повреждения. Эти повреждения сопровождаются тремя парадоксами.
Кислородный парадокс (реоксигенация). Во время ишемии тканей гипоксия повреждает клетки, так как нарушаются все энергозависимые процессы. Клеточные мембраны повреждаются таким образом, что составляющие их молекулы (в том числе фосфолипидов) становятся легкодоступными для окисления. Как известно, кислород в повышенных количествах токсичен для здоровых клеток. Для клеток же, перенесших гипоксию, даже нормальные количества кислорода являются повреждающими. Реперфузия запускает перекисное окисление липидов, которое усугубляет повреждение мембран и органелл цитоплазмы, перекисное окисление белков, инактивирующее ферменты, и перекисное окисление углеводов, деполимеризующее полисахариды, из которых состоит межклеточный матрикс.
Кальциевый парадокс. Восстановление кровотока способствует проникновению кальция в клетку в повышенных количествах, в результате чего разрушаются рибосомы и, следовательно, нарушается синтез белка и АТФ. Кроме того, кальций активирует образование медиаторов, усиливающих расстройства микроциркуляции и нарушающих проницаемость мембран.
Ионный парадокс. Во время ишемии осмолярность в тканях увеличивается на 40–50 ммоль/л (осмотическое давление на 760–950 мм рт.ст.). После восстановления кровотока ткани активно притягивают из него воду и отекают.
Инфекционно-септический механизм. ЖКТ на всем протяжении заселен микроорганизмами, и их значение общеизвестно. Существует целый ряд барьеров, отделяющих внутреннюю среду организма от содержимого кишечника. В частности, к ним относятся гликокаликс энтероцитов и тесные соединения между ними, секретируемый различными клетками IgA, лимфоциты и резидентные макрофаги подслизистого слоя кишечной стенки, биотрансформационная функция печени, лизоцим, желчные кислоты, протеолитические ферменты желудочного и кишечного сока, дефекация, снижающая внутрикишечное давление, что препятствует проникновению бактерий через эпителий кишечника, и многие другие. Слаженная работа этих барьерных систем нарушается под влиянием патологических процессов, происходящих при тяжелом сепсисе и септическом шоке. Этому способствует также нерациональная антибактериальная терапия, излишнее количество антацидных средств, нарушения иммунной реактивности, длительное парентеральное и гиперосмолярное энтеральное питание, парез кишечника и застой его содержимого. В результате этих явлений происходит транслокация микроорганизмов и развивается эндотоксемия. Эндотоксемия нарушает функции различных органов и систем, в том числе клеток Купфера, повреждает слизистый барьер. Кроме того, транслокация эндотоксинов происходит и через мезентериальные лимфатические узлы, в результате чего эндотоксины через грудной проток достигают легких, являющихся первичным фильтром, и способствуют легочной недостаточности. Таким образом, транслокация запускает синдром системного воспалительного ответа (ССВО), являющегося важнейшим звеном сепсиса.
Феномен двойного удара. ПОН имеет два основных пути развития. Первичная ПОН является результатом непосредственного воздействия какого-либо повреждающего фактора и проявляется быстро. Такой путь характерен для политравмы, тяжелых ожогов, отравлений чрезвычайно токсичными ядами и т.п. Вторичная ПОН развивается вследствие чрезмерного генерализованного ответа организма на повреждающий фактор и проявляется после латентного периода. При сепсисе ПОН является проявлением крайне выраженного системного ответа на инфекцию.
2. Лечение больных с тяжелым сепсисом
Тяжелое течение сепсиса и септического шока, высокая летальность и большая стоимость лечения при этой патологии обусловили необходимость объединения международных усилий для борьбы с этой грозной патологией. 11 медицинских организаций со всего мира развернули международное движение за выживаемость при сепсисе (Surviving Sepsis Campaign — SSC), члены которого после анализа результатов многоцентровых рандомизированных исследований в 2004 году представили ключевые рекомендации по лечению тяжелого сепсиса и септического шока, дополненные ими в 2008 году.
Ключевые рекомендации классифицируются по двум параметрам: строгости и степени доказательности. Первый параметр имеет 2 градации (то есть рекомендация может быть строгой — степень 1 и нестрогой — степень 2). Второй параметр имеет 4 градации (степень доказательности может быть высокой — степень A, умеренной — степень B, низкой — степень C и очень низкой — степень D).
Если рекомендации присваивается степень строгости 1 (рекомендация строгая), это означает, что положительные эффекты соблюдения рекомендации (благоприятный исход, облегчение для больного, снижение нагрузки на персонал, уменьшение стоимости лечения) явно преобладают над отрицательными. Если рекомендация имеет степень строгости 2 (рекомендация нестрогая), то положительные эффекты ее соблюдения, скорее всего, будут преобладать над отрицательными, но уверенности в этом из-за слабости доказательств нет, или положительные и отрицательные эффекты практически уравновешивают друг друга. Так как четкой границы между строгими и нестрогими рекомендациями нет, в ряде случаев нестрогая рекомендация может оказаться более желательной. Проще суть строгости рекомендации можно выразить следующими словами комиссии SSC: «A strong recommendation is worded as «we recommend» and a weak recommendation as «we suggest» (Строгая рекомендация сформулирована так, как «мы рекомендуем», а нестрогая — так, как «мы предлагаем»).
Что касается степени доказательности, то вначале всем рандомизированным исследованиям присваивается степень A, затем она может быть понижена из-за недостаточного для доказательности оснащения, противоречивости или неточности результатов, косвенности доказательств, возможной пристрастности при оценке результатов и т.п.
2.1. Неотложные мероприятия
Эти мероприятия необходимо проводить немедленно по установлении диагноза «септический шок», о наличии которого свидетельствует сохраняющаяся артериальная гипотензия после адекватной инфузионной терапии или уровень лактата не менее 4 ммоль/л, указывающий на тканевую гипоперфузию. Откладывать неотложные мероприятия до поступления пациента в отделение интенсивной терапии (ОИТ) недопустимо. В первые 6 часов необходимо достичь следующих показателей (степень 1C):
— ЦВД 110–160 мм вод.ст.;
— САД і 65 мм рт.ст.;
— диурез і 0,5 мл/кг∙час;
— SvO2 і 70 % в центральной вене или і 65 % в смешанной венозной крови.
Примечания: 1. Раннее целенаправленное лечение повышает выживаемость при септическом шоке и снижает летальность в первые 28 дней. 2. Измерение SvO2 в крови центральной вены равноценно с точки зрения качества диагностики его измерению в смешанной венозной крови как в непрерывном, так и в прерывистом режиме. 3. Хотя лактат и недостаточно точно отражает метаболический статус тканей, его повышенный уровень означает необходимость решительных лечебных действий. 4. При проведении ИВЛ или в случае снижения растяжимости желудочков, а также при повышенном внутрибрюшном давлении ЦВД целесообразно поддерживать на уровне 160–200 мм вод.ст. Повышенное ЦВД может наблюдаться и при предсуществующей клинически значимой легочной гипертензии. 5. Хотя причины тахикардии при септическом шоке разнообразны, снижение повышенного пульса при проведении адекватной инфузионной терапии часто является признаком, доказывающим восполнение ОЦК.
Недавно опубликованные исследования показали связь между благоприятным исходом при септическом шоке и поддержанием САД і 65 мм рт.ст., а также центрального SvO2 (ScvO2) і 70 %. Если в первые 6 часов тяжелого сепсиса или септического шока на фоне инфузионной терапии с достижением целевого ЦВД ScvO2 не достигает 65 % (70 %), необходима трансфузия эритроцитарной массы с доведением Ht до уровня не менее 30 % и/или введение добутамина вплоть до 20 мкг/кг/мин (степень 2C). Следование данной рекомендации повышало выживаемость.
2.2. Выявление возбудителя заболевания
Перед антибактериальной терапией, если только это не слишком задерживает ее начало, необходимо выполнить по крайней мере 2 посева крови, причем забор крови должен осуществляться из вены чрескожно и из каждого венозного катетера, если только он не установлен недавно (< 48 часов назад). До введения антибиотиков целесообразны также посевы мочи, раневого отделяемого, ликвора, мокроты и т.п. (степень 1C). Если в обоих посевах крови дает рост один и тот же микроорганизм, высока вероятность того, что он и является причиной сепсиса. Если в посеве, взятом через венозный катетер, рост начинается на 2 и более часа раньше, чем в посеве, взятом чрескожно из периферической вены, источником инфекции, скорее всего, является катетер.
Инвазивные исследования для выявления источника инфекции у нестабильных больных вне ОИТ часто невозможны. В таких случаях полезными могут оказаться неинвазивные исследования, например УЗИ (степень 1C).
2.3. Антибактериальная терапия
Антибактериальная терапия должна начинаться в течение часа после диагностирования септического шока (степень 1B) и тяжелого сепсиса без шока (степень 1D) после взятия материала для микробиологического исследования. Задержка антибактериальной терапии с каждым часом значительно увеличивает летальность.
Поскольку при тяжелом сепсисе и септическом шоке на первом месте стоит массивная инфузионная терапия через стационарный венозный катетер, для антибактериальной терапии целесообразна установка отдельного венозного доступа.
Начальная эмпирическая терапия должна включать один препарат или более, которые имеют активность против всех вероятных причинных микроорганизмов (бактериальных и/или грибковых) и проникают в адекватных концентрациях в предполагаемый источник сепсиса (степень 1B). Выбор эмпирического антибиотика зависит от многих привходящих обстоятельств, включая анамнез больного, непереносимость им определенных лекарственных средств, клинические проявления, степень гидратации пациента, скорость инфузии, состояние функции печени и почек, характерные для данного лечебного учреждения штаммы микроорганизмов, соотношение эффективности и токсичности препарата и т.д. Недавно примененных антибиотиков в общем следует избегать. Доза антибактериальных препаратов должна быть адекватной, но в то же время выбираться с учетом состояния функции печени и почек и объема инфузии, поэтому целесообразен постоянный контроль за концентрацией препарата в крови.
Режим введения антибиотиков необходимо оценивать ежедневно во избежание развития резистентности, токсических реакций и излишней стоимости лечения (степень 1C).
Если в качестве возбудителя сепсиса предполагается или идентифицируется Pseudomonas, а также при наличии нейтропении на фоне тяжелого сепсиса, необходимо проводить комбинированную антибактериальную терапию, но не более 3–5 дней, после чего, как только будет выявлен возбудитель, следует переходить на монотерапию для предупреждения развития резистентности к антибиотикам, снижения токсичности терапии и уменьшения стоимости лечения (степень 2D).
Как правило, длительность антибактериальной терапии должна составлять 7–10 дней; более длительный курс может проводиться при слабом эффекте лечения, наличии недренированных очагов и иммунодепрессии, в частности проявляющейся нейтропенией (степень 1D). Необходимо помнить, что более чем в 50 % случаев тяжелого сепсиса и септического шока посевы крови бывают отрицательными и вероятным возбудителем во многих таких случаях являются бактерии или грибы. Таким образом, решение о продолжении, сужении или прекращении антибактериальной терапии необходимо принимать, основываясь на оценке клинической информации.
Признаками эффективности начальной антибактериальной терапии в первые 3–5 дней являются следующие:
— улучшение общего состояния, прояснение сознания, повышение качества жизни;
— снижение количества баллов по шкале SOFA;
— снижение выраженности признаков ССВО — нормализация температуры, ЧСС, ЧДД, содержания лейкоцитов в периферической крови, концентрации биохимических маркеров ССВО;
— положительные сдвиги со стороны септических очагов и отсутствие новых.
Различают такие степени эффективности антибактериальной терапии:
— выздоровление;
— улучшение состояния без полного исчезновения симптомов заболевания при отсутствии необходимости в дополнительной антибактериальной терапии;
— отсутствие эффекта, когда необходима другая или дополнительная антибактериальная терапия;
— рецидив — ухудшение состояния или повторное появление инфекции после выздоровления или улучшения состояния.
Эффективность антибактериальной терапии невозможно оценить при прекращении лечения по какой-либо причине в период до 48 часов или при прогрессировании другого патологического процесса.
Если в процессе обследования выясняется, что причина ССВО носит неинфекционный характер, антибиотики должны быть немедленно отменены для снижения риска формирования устойчивых штаммов и уменьшения стоимости лечения.
2.4. Воздействие на септический очаг
Наличие или отсутствие очага инфекции должно быть выявлено как можно быстрее (степень 1C), и лучше это сделать в первые 6 часов (степень 1D). Очаг должен быть удален или дренирован с помощью следующих мероприятий (степень 1C):
— дренирование (забрюшинный абсцесс, эмпиема плевры, септический артрит, пиелонефрит, холангит, абсцесс или псевдокиста поджелудочной железы);
— иссечение (некротический фасциит, инфицированный панкреонекроз, инфаркт кишечника, медиастенит);
— удаление инфицированных доступов (сосудистый и мочевой катетеры, эндотрахеальная трубка, внутриматочный контрацептив);
— радикальная хирургическая санация (дивертикулит толстой кишки, гангренозный холецистит, клостридиальный мионекроз).
При наличии инфицированного перипанкреатического некроза, идентифицированного как возможный источник инфекции, вмешательство лучше отложить, пока не произойдет адекватная демаркация жизнеспособных и нежизнеспособных тканей (степень 2B).
Воздействие на источник должно быть наименее инвазивным, по возможности следует выполнять чрескожное, а не хирургическое дренирование (степень 1D).
2.5. Инфузионная терапия
Инфузионная терапия должна проводиться растворами натуральных или искусственных коллоидов или кристаллоидов. Каких-либо преимуществ у тех или иных сред не выявлено (степень 1B). Введение альбумина безопасно и так же эффективно, как кристаллоидов. Хотя введение препаратов гидроксиэтилкрахмала (ГЭК) у септических больных может вызвать почечную недостаточность, данные различных исследований позволяют их рекомендовать. Так как объем распределения является намного большим для кристаллоидов, чем для коллоидов, кристаллоидов требуется больше для достижения того же эффекта, и это может привести к большим отекам. Стоимость кристаллоидов ниже, чем коллоидов. Имеет смысл использовать разумное сочетание коллоидов и кристаллоидов.
Начальная скорость введения жидкости должна обеспечить ЦВД минимум 110 мм вод.ст. (160 мм вод.ст. при проведении ИВЛ). Как правило, в дальнейшем требуется продолжение инфузии (степень 1C).
Необходима постоянная оценка реакции на инфузию (АД, ЧСС, темп диуреза), пока не стабилизируется гемодинамика (степень 1D).
При гиповолемии скорость инфузии должна составлять по крайней мере 1000 мл кристаллоидов или 300–500 мл коллоидов за 30 мин. Большая скорость может потребоваться при наличии тканевой гипоперфузии (степень 1D). Если на фоне инфузии наблюдается рост ЦВД или давления заклинивания в легочной артерии при сохранении артериальной гипотензии, скорость инфузии следует уменьшить.
2.6. Вазопрессоры
САД следует поддерживать на уровне не менее 65 мм рт.ст. (степень 1C). Если имеет место жизнеугрожающая гипотензия с нарушением тканевой перфузии на фоне сохраняющейся гиповолемии, необходимо прибегать к помощи вазопрессоров для поддержания тканевой перфузии, линейно зависящей от САД.
Препаратами выбора для коррекции гемодинамики при септическом шоке являются норадреналин (НА) и допамин (ДА), которые должны вводиться через центральный катетер (степень 1C). При септическом шоке не следует начинать вазопрессорную терапию с адреналина, фенилэфрина или вазопрессина (степень 2C). При недостаточной эффективности НА или ДА целесообразно перейти на адреналин (степень 2B). Применение вазопрессина, скорее всего, принесет больше вреда, чем пользы (снижение сердечного выброса и гепатоспланхнического кровотока, ишемия миокарда и даже асистолия).
Введение низких, так называемых почечных, доз ДА для поддержания функции почек не имеет смысла (степень 1A), что доказано исследованиями уровня креатинина, темпа диуреза, времени восстановления функции почек.
Пациентам, нуждающимся в вазопрессорах, следует по возможности устанавливать внутриартериальные катетеры для прямого измерения АД (степень 1D).
2.7. Инотропная терапия
При сердечной слабости, проявляющейся повышением преднагрузки и снижением сердечного выброса, показано введение добутамина (степень 1C). Не следует повышать сердечный индекс выше нормы (степень 1B), так как установлено, что доставка кислорода должна быть не выше уровня, позволяющего избежать тканевой гипоксии, обусловленной нарушением кровообращения. Если нет возможности измерять сердечный индекс, целесообразно сочетание инотропных препаратов с вазопрессорами, если же такая возможность имеется, применять НА и добутамин следует, основываясь на результатах этих измерений.
2.8. Кортикостероиды
Их нужно применять только у взрослых в случаях, когда с помощью волемической терапии и вазопрессоров не удается стабилизировать гемодинамику (степень 2C).
При наличии гидрокортизона дексаметазон вводить не следует (степень 2B).
Если гидрокортизон недоступен, можно использовать пероральный флудрокортизон (50 мкг), поскольку он не обладает существенной минералокортикоидной активностью (степень 2C).
Когда отпадает необходимость во введении вазопрессоров, кортикостероиды должны быть отменены (степень 2D). Доза гидрокортизона не должна превышать 300 мг в сутки, и он не должен применяться в отсутствие шока, если нет других показаний для его введения (степень 1D).
Нет необходимости в проведении теста на ответ на АКТГ (повышение концентрации кортизола в крови выше 90 мг/л через 30–60 мин после введения АКТГ), если при септическом шоке клинически больной нуждается в кортикостероидах (степень 2B).
2.9. Рекомбинантный человеческий активированный протеин (rhAPC)
Рекомбинантный человеческий активированный протеин показан при вызванной сепсисом ПОН и высоком риске летального исхода (более 25 баллов по шкале APACHE II), если нет противопоказаний к его применению — риска кровотечений, превышающего предполагаемую пользу от его применения (степень 2B, кроме больных, которым выполнено оперативное вмешательство не более 30 дней назад, — степень 2C).
rhAPC, являясь интегральным регулятором воспаления, коагуляции и фибринолиза, увеличивает выживаемость больных с вызванной сепсисом ПОН. Показания к его применению следующие:
— активное внутреннее кровотечение;
— перенесенный до 3 месяцев назад геморрагический инсульт;
— перенесенная до 2 месяцев назад внутричерепная или спинальная операция или тяжелая черепно-мозговая травма;
— травма с высоким риском опасного кровотечения;
— наличие эпидурального катетера;
— внутричерепные опухоли или метастазы, мозговая грыжа.
Во время инфузии rhAPC уровень тромбоцитов не должен быть менее 30 000 в 1 мкл.
2.10. Препараты крови
Если тканевая гипоперфузия купирована и нет ишемии миокарда, тяжелой гипоксемии, острого кровотечения, синих пороков или лактатацидоза, эритроцитарная масса необходима только при снижении Hb до 70 г/л и менее. Ее введение должно продолжаться до достижения уровня Hb 70–90 г/л у взрослых (степень 1B).
Назначение эритропоэтина для лечения анемии, связанной с сепсисом, не рекомендуется. Он необходим, если есть другие показания для его применения, например почечная недостаточность, вызвавшая снижение продукции эритропоэтина (степень 1B).
Свежезамороженная плазма для коррекции лабораторных показателей в отсутствие кровотечений или запланированных инвазивных вмешательств не рекомендуется (степень 2D), так же как не показано введение антитромбина (степень 1B), так как эти мероприятия не улучшают исход заболевания.
Тромбоциты не должны вводиться, если их содержание превышает 5∙109/л, даже при очевидном кровотечении. Если этот показатель находится как раз на уровне около 5∙109/л, введение тромбоцитов может оказаться необходимым только при большом риске кровотечений. Высокий уровень тромбоцитов (50∙109/л) требуется для операций и инвазивных процедур (2D).
3. Управление функциями организма при тяжелом сепсисе
3.1. ИВЛ при вызванном сепсисом синдроме острого повреждения легких (СОЛП)/ респираторном дистресс-синдроме взрослых (РДСВ)
Дыхательный объем (ДО) во время ИВЛ не должен превышать 6 мл/кг должной массы тела — ДМТ (степень 1B), чтобы давление в дыхательных путях в конце вдоха не превышало 30 см вод.ст., хотя все же следует учитывать растяжимость грудной стенки (степень 1C). Если при таком ДО не удается снизить давление на вдохе, ДО нужно снизить до 4 мл/кг ДМТ. ДМТ рассчитывается по формуле:
мужчины: 50 + 0,91∙(рост в см – 152,4);
женщины: 45,5 + 0,91∙(рост в см – 152,4).
Гиперкапния, даже превышающая исходный уровень, допустима, если при СОЛП/РДСВ требуется понизить давление на вдохе. SaO2 следует удерживать на уровне 88–95 %.
Ни один из режимов вентиляции не продемонстрировал преимуществ над другими (по давлению, по объему, высокочастотная ИВЛ и т.д.).
Для предупреждения экспираторного закрытия дыхательных путей (ЭЗДП) ИВЛ нужно проводить с положительным давлением в конце выдоха (ПДКВ) (степень 1C).
При РДСВ могут потребоваться потенциально опасные уровни FiO2 или давления на вдохе. В таких случаях может оказаться полезным периодическое положение на животе при отсутствии к нему противопоказаний и наличии у лечащего врача опыта применения такого метода (2C). Положение на животе в большинстве случаев улучшает оксигенацию.
При отсутствии противопоказаний во время ИВЛ головной конец койки для предупреждения аспирации и вентилятор-ассоциированной пневмонии следует приподнимать (степень 1B) на 30–45° (степень 2C).
При умеренной гипоксемии, реагирующей на низкие уровни ПДКВ, стабильной гемодинамике, легкой разбудимости, возможности самостоятельно защищать свои дыхательные пути, очищать их от секрета возможна вентиляция через маску, тем не менее нужно быть постоянно готовым к интубации трахеи (степень 2B). Условия неинтубированной трахеи дают многочисленные преимущества: легкое общение, низкий риск инфекции, снижение потребности в седативных препаратах. К сожалению, только небольшая часть больных может вентилироваться таким способом.
Возможность начать отлучение от респиратора определяется по следующим критериям:
— разбудимость;
— стабильность гемодинамики (без вазопрессоров);
— отсутствие новых потенциально опасных состояний;
— безопасный уровень необходимого FiO2, позволяющий пользоваться маской или носовым катетером;
— основное заболевание разрешается, новые не развиваются;
— прекращение седации;
— появление кашля при санации трахеобронхиального дерева;
— paO2/FiO2 > 200 мм рт.ст., ПДКВ Ј 5 см вод.ст., МОД < 15 л/мин, отношение ЧДД к ДО не более 105 при 2-минутном самостоятельном дыхании.
Если в течение 30–120 мин спонтанного дыхания ЧДД становится выше 35 мин–1, SaO2 < 90 %, ЧСС > 140 мин–1 или увеличивается на 20 % возрастной нормы, АДсист. < < 90 или > 180 мм рт.ст., появляется беспокойство, чувство тревоги, повышается потоотделение, то необходимо возобновлять ИВЛ.
Во время отлучения от респиратора пациента можно поддерживать вспомогательной вентиляцией и постоянным положительным давлением в дыхательных путях (» 5 см H2O). Если спонтанное дыхание адекватно, нужно ставить вопрос об экстубации (степень 1A).
3.2. Седация и миорелаксанты при сепсисе
Критическим больным с сепсисом, нуждающимся в ИВЛ, необходима седативная терапия (степень 1B).
Седация может проводиться с помощью болюсных введений или непрерывно с периодическим прекращением для пробуждения больного (степень 1B), что может снизить продолжительность ИВЛ, вероятность необходимости в трахеостомии и длительность пребывания в ОИТ.
Введения миорелаксантов нужно избегать. Если они все же необходимы дольше, чем в течение часа от начала ИВЛ, их использование должно сопровождаться мониторингом глубины нейромышечного блока (степень 1B).
3.3. Контроль гликемии
В неотложные мероприятия по лечению больных сепсисом с гипергликемией необходимо включать инфузию инсулина с целью снижения гликемии до 8,3 ммоль/л (степень 2C). Одновременно с введением инсулина необходима инфузия глюкозы как источника энергии, при этом контроль гликемии следует осуществлять каждые 1–2 часа до стабилизации гликемии и скорости введения инсулина, после чего контроль должен проводиться каждые 4 часа (степень 1C).
Нужно с осторожностью относиться к низким результатам измерения гликемии в капиллярной крови. В таких случаях нужно перепроверить содержание глюкозы в артериальной крови или в плазме (степень 1B).
3.4. Терапия острой почечной недостаточности
Длительная заместительная терапия ОПН и дискретный гемодиализ равноценны при лечении больных тяжелым сепсисом (степень 2B). Первый метод облегчает коррекцию водно-электролитного баланса при нестабильной гемодинамике (степень 2D).
3.5. Применение гидрокарбоната натрия
При pH і 7,15 введение гидрокарбоната натрия не рекомендуется, поскольку это не приводит к ожидаемому улучшению состояния гемодинамики и снижению потребности в вазопрессорах. (степень 1B).
3.6. Профилактика тромбоза глубоких вен
При тяжелом сепсисе больные должны получать низкие дозы нефракционированного гепарина или низкомолекулярные фракционированные гепарины для профилактики тромбоза глубоких вен (степень 1A), если они не противопоказаны (тромбоцитопения, тяжелая коагулопатия, продолжающееся кровотечение, недавнее внутримозговое кровоизлияние). При наличии противопоказаний к гепаринам должны использоваться механические методы профилактики — перемежающаяся механическая компрессия и т.п., если они не противопоказаны (степень 1A).
При высоком риске тромбоэмболических осложнений, наличии их в анамнезе, при травматических повреждениях или после ортопедических операций нужна комбинация фармакологических и механических методов (степень 2C). В этих же случаях более показаны низкомолекулярные фракционированные гепарины, чем нефракционированные (степень 2C).
3.7. Профилактика стрессовых язв ЖКТ
Для этой цели необходимы H2-блокаторы (степень 1A) или ингибиторы протонной помпы (степень 1B). Необходимо соотносить пользу от повышения pH желудочного содержимого с риском развития вентилятор-ассоциированной пневмонии.
3.8. Вопросы ограничения поддерживающей терапии
Пациент и члены его семьи должны быть информированы о целях проводимого лечения и возможных его исходах. Решения лечащих врачей, пациента и его законных представителей должны приниматься только на основании действующего законодательства.