Международный неврологический журнал 7 (45) 2011
Вернуться к номеру
Мультимодальная терапия острого ишемического инсульта: рабочая парадигма Доклады на сателлитном симпозиуме EVER Neuro Pharma в рамках 20-й Европейской конференции по инсульту, Гамбург, 24–27 мая 2011 г.
Авторы: James Gilbart, Daniel Webber, Touch Briefings, London, UK
Рубрики: Неврология
Версия для печати
На открытии симпозиума, посвященного проблеме острых ишемических нарушений мозгового кровообращения (ОНМК), профессор Jong Kim отметил, что, несмотря на то, что клиницисты владеют методами лечения ОНМК в острой стадии, на данном этапе не существует фармакотерапевтических методов, направленных на устранение или улучшение клинической симптоматики в позднем (отдаленном) периоде. Он также отметил, что большинство восстановительных препаратов, которые были предложены для лечения данной патологии, не зарекомендовали себя с положительной стороны и поэтому существует острая необходимость в совершенствовании знаний о механизмах ОНМК, что, в свою очередь, приведет к улучшению методов лечения данной патологии. Секции симпозиума, посвященные препарату Церебролизин® (EVER Neuro Pharma, Австрия), состояли из 3 презентаций, посвященных экспериментальному изучению клинической эффективности и нейропротективных свойств данного препарата.
Доклад профессора Zheng Gang Zhang был посвящен экспериментальному обоснованию восстановительных свойств препарата при лечении ОНМК и состоял из двух частей, одна из которых основывалась на утверждении, что после перенесенного ОНМК ткань мозга подвергается процессам эндогенной репарации, а вторая — на том, что данный препарат положительно влияет на процесс регенерации, облегчая и ускоряя его. В эмбриональном и зрелом мозге человека и грызунов были выявлены нейрогенные стволовые клетки (НСК). В головном мозге грызунов существует 2 основных депо НСК: субвентрикулярная зона (СВЗ) бокового желудочка головного мозга и субгранулярная зона зубчатой извилины [1–3]. В СВЗ НСК астроцитарного ряда (Б-тип клеток) расположены под слоем реснитчатых эпендимальных клеток. Клетки типа Б, размножаясь, могут превращаться в промежуточные нейрогенные прогениторные клетки (С-тип клеток), которые, в свою очередь, превращаются в нейробласты (А-тип клеток), а они, в свою очередь, мигрируют в область обонятельной луковицы и могут размножиться и дифференцироваться в клетки нервной ткани [1–3].
Экспериментальная модель ОНМК у грызунов подтвердила значительный рост уровня даблкортина (DCX) — основного маркера нейробластов в СВЗ и стриатуме [4–7]. В нормальных условиях нейробласты мигрируют в обонятельную луковицу ростральным путем. После ишемии нейробласты мигрируют в зону ишимизированного стриатума [6]. Нейробласты выделяют DCX. У трансгенных крыс, сенсибилизированных флюоресцентным белком, в реальном времени изучали пролиферацию и миграцию нейробластов. Последние продолжают превращаться в нейроны на протяжении еще 14 дней с момента окклюзии средней мозговой артерии (СМА) в граничащей с ишемией зоне и продолжают мигрировать на протяжении еще 60 дней. В интактном мозге грызунов эндотелиальные клетки не дифференцируются. Хотя после окклюзии СМА и череды сосудистых изменений, которые следуют за этим процессом, эндотелиальные клетки размножаются и формируют большое количество новых сосудов. Нейробласты мигрируют в зону пораженной ткани через проводники из вновь сформированных сосудов и новых капилляров в зоне, граничащей с ишемией.
Данные магнитно-резонансной томографии (МРТ) позволяют оценить особенности вновь сформированных сосудов, наличие гематоэнцефалического барьера (ГЭБ) и подтверждают предположение о функциональной состоятельности данных сосудов: возможность поставки кислорода, питательных веществ, секреции факторов роста, включая клеточный стромальный фактор 1 клеток эндотелия, который обеспечивает направленную миграцию нейробластов. ОНМК обусловливает гибель предшественников олигодендроцитов. Вслед за острой фазой ОНМК усиливаются процессы олигодендрогенеза, формирования новых олигодендроцитов, а по истечении 14-го дня вновь образованные олигодендроциты могут продуцировать миелин, необходимый для нормального проведения нервного импульса по аксону. Улучшение функционального статуса после перенесенного ОНМК в эксперименте подтверждено серией проведенных двигательных и чувствительных тестов у грызунов. Показатели исполнения данных тестов улучшаются с течением времени в связи с проходящими процессами нейрогенеза и олигодендрогенеза.
Доказательства того, что препараты из группы статинов могут улучшать процессы регенерации ткани и, соответственно, исходы после перенесенного ОНМК, подтвердили необходимость их применения по данным показаниям [11]. Терапия с использованием стволовых клеток костного мозга также значительно улучшает клинические исходы после перенесенного ОНМК. Наиболее вероятно, что при этом положительный эффект обусловлен их взаимодействием с эндогенными клетками, что, в свою очередь, ведет к увеличению уровня протеинов, включая церебральный нейротрофический фактор роста и сосудистый эндотелиальный фактор роста (VEGF), и к развитию разнообразных эффектов — усилению процессов нейрогенеза, ангиогенеза и олигодендрогенеза [12].
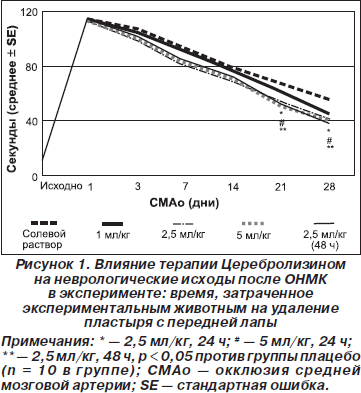
В некоторых экспериментальных исследованиях на грызунах Церебролизин оказывал выраженный восстановительный эффект после перенесенного ОНМК, и, соответственно, предпринимались попытки объяснить механизмы такого влияния. В одном из исследований, в котором использовали модель ОНМК с перевязкой средней мозговой артерии [13], значительные улучшения неврологических показателей были отмечены уже на 28-й день после применения Церебролизина через 24 или 48 часов после инсульта (рис. 1). Применение Церебролизина привело к значительному (р < 0,05) сокращению времени, через которое грызун ощущал клейкий пластырь на своей передней лапе и отклеивал его, в сравнении с аналогичным показателем при использовании плацебо. Более того, терапия Церебролизином приводила к значительному (р < 0,05) увеличению количества нейробластов в СВЗ по сравнению с плацебо [13]. Этот эффект осуществлялся через сигнальный путь PI3K/Akt. Последнее подтверждается тем, что при его специфическом блокировании нейрогенез, индуцированный Церебролизином, прекращался.
Для подтверждения того, что Церебролизин повышает количество нейробластов, их предшественники брали из мозга взрослых грызунов и культивировали in vitro. Церебролизин увеличивал количество пролиферирующих предшественников нервных клеток и индуцировал их направленную миграцию. В проведенном in vitro анализе способности клеток к формированию капиллярных трубок Церебролизин усиливал процессы ангиогенеза путем усиления синтеза РНК-мессенджера для продукции проангиогенного фактора, VEGF и ангиопротеина-1. Непосредственное добавление Церебролизина в суспензию клеток-предшественников in vitro привело к увеличению популяции олигодендроцитов [13].
Одним из важнейших путей контролирования пролиферации НСК является сигнальный путь sonic hedgehog (Shh, названный в честь компьютерного персонажа ежа Соника) [14]. Это главный путь, через который Церебролизин может влиять на нейрогенез. Этот путь регулирует нейрогенез и олигодендрогенез при развитии головного мозга [15, 16]. В данный процесс вовлечены два вида рецепторов — patched-1 и smoothened. При отсутствии Shh рецептор patched-1 угнетает smoothened, что подавляет сигналы активации процессов нейрогенеза и олигодендрогенеза. Когда путь Shh свободен, происходит связывание рецептора patched-1 и активация smoothened, что в конечном итоге приводит к транскрипции фактора Gli1, который активирует гены-мишени, особенно те, которые принимают участие в увеличении популяции клеток. Церебролизин активирует Shh и 2 вышеупомянутых рецептора в клеточной культуре (Zhang, неопубликованные данные). Для подтверждения роли Shh в процессе нейрогенеза и олигодендрогенеза в клеточную культуру НСК добавляли циклопамин в комбинации с Церебролизином, при этом циклопамин блокирует smoothened-рецепторы. При добавлении циклопамина в клеточную культуру НСК в комбинации с Церебролизином пролиферативный эффект последнего блокируется и, следовательно, процессы нейрогенеза и олигодендрогенеза тоже прекращаются. Однако данные результаты требуют подтверждения in vivo.
Профессор Zhang пришел к следующему выводу: «Церебролизин влияет на нейрогенез, ангиогенез и олигодендрогенез, с двусторонним усилением одного процесса другим, что в конечном счете приводит к восстановлению ткани мозга и улучшению неврологических функций».
Во второй презентации профессор Michael Brainin представил текущее состояние проблемы лечения ОНМК, которое включает применение тканевого активатора плазминогена в течение первых 4,5 часа после ОНМК в специализированном инсультном отделении, проблемы использования аспирина при ОНМК и нейрохирургические мероприятия, направленные на борьбу с отеком мозга у пациентов в возрасте старше 60 лет. Несмотря на все достижения в лечении ОНМК, на сегодняшний день остается пробел в этой области — отсутствует терапия, которая имела бы нейропротективный характер и могла быть использована в подостром периоде. Нейропротективная терапия защищает ткань мозга в переходной зоне НМК — зоне ишемических нарушений, а в данной ситуации время решает все, поскольку с течением времени с момента катастрофы количество гибнущих клеток увеличивается и зона инфарцирования растет. Поэтому необходимо расширить понимание и распознавание симптомов ОНМК, ускорить транспортировку больных в специализированные инсультные отделения, уменьшить временной интервал до момента постановки диагноза, используя современные методы визуализации, и, что особенно важно, проводить свое-временное, а значит, эффективное лечение. Более того, специфическое окружение и расширенные программы реабилитации могут улучшать неврологические исходы у пациентов, перенесших ОНМК [17, 18].
Недавно ряд препаратов из группы нейропротекторов, которые должны были быть внедрены в клиническую практику, не подтвердили свою эффективность в клинических испытаниях. Наиболее значимым был NXY-059 (дисуфентон натрия) — первый нейропротектор, эффективность которого соответствовала критериям STAIR (Stroke Treatment Academic Industry Roundtable) (табл. 1)[19–22]. Экспериментальные данные показали, что непосредственно после ОНМК запускается каскад ишемических, реперфузионных процессов, повышается содержание свободных радикалов, которые блокируются препаратом NXY-059, поскольку данный препарат является антиоксидантом. На основании полученных экспериментальных данных и критериев STAIR была инициирована 3-я фаза клинического испытания. Исследование SAINT (The Stroke Acute Ischemic NXY-059 Trial) представляло собой рандомизированное исследование, целью которого было определение эффективности NXY-059 при использовании его у пациентов с ОНМК по ишемическому типу. Пациенты получали данный препарат в первые 6 часов после катастрофы, у них существенно уменьшилась степень инвалидизации по истечении 90 дней с момента ОНМК по сравнению с теми, которые получали плацебо. NXY-059 существенно не влиял на другие исходы, включая неврологические функции по шкале NIHSS (National Institutes of Health Stroke Scale) [23]. Хотя данные проведенного позже исследования SAINT II (исследование в отдаленном периоде) оказались отрицательными [24]. Изучение результатов позволило определить особенности дизайна, который необходимо улучшить, и предположить, что критерии STAIR должны быть изменены, т.е. должны содержать биологически релевантные конечные точки, исследования мультимодальных фармакологических препаратов и систематические обзоры всей информации перед проведением клинических испытаний [25].
Профессор Brainin также говорил о препарате цитиколин, который ингибирует высвобождение глутамата [26]. Данные МРТ подтвердили уменьшение кортикальной зоны инфарцирования мозгового вещества под влиянием заместительного эффекта цитиколина [27]. Хотя ранее предполагалось, что цитиколин не оказывает существенного влияния на процессы восстановления у пациентов, перенесших ОНМК, метаанализ всех клинических испытаний цитиколина подтвердил возможное уменьшение смертности у пациентов с ОНМК [28]. Данные результаты стали толчком для проведения нового клинического исследования — International Citicoline Trial on Acute Stroke, которое еще не завершено.
Профессор Brainin продолжил свое выступление описанием недавних исследований препарата DP-b99 — липофильного хелатного соединения ионов цинка и кальция. Данный препарат селективно действует внутри клеточной мембраны и направлен на устранение процессов токсичности, апоптоза и воспаления [29]. Небольшое (n = 150) плацебо-контролируемое исследование 2b фазы, в котором пациенты получали 1 мг/кг DP-b99 в виде 2-часовой инфузии на протяжении 4 дней (препарат начинали вводить в течение первых 9 часов с момента наступления ОНМК), показало, что первичные клинические исходы на 90-й день соответствовали таковым при использовании плацебо (р < 0,04) [30].
Сульфат магния имеет следующие сосудистые эффекты: увеличивает сердечный выброс, регионарный мозговой кровоток и оказывает некоторые нейрональные влияния (усиливает процессы восстановления АТФ и блокирует N-метил-D-аспартатные каналы). Исследование The Field Administration of Stroke Treatment, плацебо-контролируемое двойное слепое мультицентровое региональное рандомизированное, включало 1298 пациентов, перенесших ОНМК. Пациенты, которые принимали участие в исследовании, получали 4 мг сульфата магния до момента поступления в инсультное отделение, с последующим введением 16 г на протяжении 24 часов. Исследование продолжается и в настоящее время, по предварительным результатам сообщается об улучшении показателей исхода, причем особенное внимание уделяется ключевому фактору — временному интервалу. Так, среднее время от наступления ОНМК до получения первой дозы исследуемого препарата составляло 46 минут, причем 72 % пациентов получали лечение в течение 1-го часа после ОНМК, а 24 % — в течение 1–2 часов с момента наступления катастрофы (неопубликованные данные). Средний интервал от момента прибытия бригады скорой медицинской помощи до введения первой дозы препарата составлял 25 мин.
Профессор Brainin пришел к выводу, что «нейропротективный препарат открывает большое количество новых подходов, включая возможность начинать лечение на догоспитальном этапе, позволяет охватить большую популяцию пациентов и потенцировать процессы восстановления, в частности, через факторы роста, нейротрофические факторы и стволовые клетки. Хотя экспериментальные исследования на животных должны проводиться с более высокой тщательностью, с обязательным использованием методов визуализации для подтверждения процессов восстановления».
Профессор Natan Bornstein продолжил обсуждение нейропротективных препаратов для лечения ОНМК. Профилактика и реперфузия являются современными стандартами в лечении ОНМК по ишемическому типу. Ключевые вопросы касаются способности нейротрофического лечения поддерживать процессы восстановления, а также того, что может нейропротекция дать пациентам с ОНМК. Механизмы гибели нейронов вследствие ОНМК по ишемическому типу включают токсичность, процессы деполяризации в околоинфарктной зоне, воспаление, повреждение вследствие реперфузии и апоптоз. Эти процессы являются хорошими мишенями для лечения в остром периоде [31]. Несмотря на наличие потенциальных терапевтических мишеней и положительных исходов лечения в экспериментальных работах, проведенных на животных моделях, на сегодняшний день ни один из методов нейропротективного лечения, который изучался в 3-й фазе клинических исследований, не подтвердил своего положительного терапевтического эффекта. Анализ доклинических исследований, проведенных на животных моделях при лечении ОНМК, направленных на изучение эффективности нейропротективных свойств препаратов, показал, что современные клинические фармпрепараты обладают не большей эффективностью, чем некоторые другие средства, применявшиеся только в эксперименте на животных. Эти неудачи привели к тому, что академические эксперты и фармацевтические представители разработали рекомендации типа STAIR [20, 33].
Обзор всех клинических исследований нейропротективных препаратов в терапии ишемических ОНМК показал, что существует только 2 препарата, которые способны положительно влиять на исходы лечения, — это Церебролизин и цитиколин [34]. Что не менее важно, в руководствах American Heart Association/American Stroke Association по лечению взрослых пациентов с ишемическими ОНМК в раннем периоде отмечаются преимущества Церебролизина, что основано на данных клинических и экспериментальных исследований [35].
Церебролизин — это нейротропный белковый препарат, который состоит из смеси нейропептидов низкой молекулярной массы и свободных аминокислот, достаточно маленьких по своим размерам, что позволяет им проникать через ГЭБ и имитировать эффекты эндогенных нейротропных факторов. Большой объем доклинических данных указывает на то, что Церебролизин может стабилизировать структуру цитоскелета путем ингибирования калпаина, стимулировать нейрогенез, уменьшать объем инфарцирования мозговой ткани, способствовать процессам функционального восстановления и пролиферации, дифференциации и миграции клеток-предшественников нейронов [13, 36–38]. Плейотропные эффекты Церебролизина имеют непосредственное клиническое значение при лечении других неврологических расстройств — деменции и травмы головного мозга. Церебролизин продемонстрировал свою эффективность при лечении ОНМК по ишемическому типу, препарат характеризуется отличным профилем безопасности, что подтверждается его применением в рамках расширенного временного терапевтического окна [39–41].
Исследование CASTA (The Cerebrolysin in Patients with Acute Ischemic Stroke in Asia) представляло собой большое двойное слепое плацебо-контролируемое рандомизированное исследование, которое основывалось на критериях STAIR и было направлено на определение безопасности и эффективности 10-дневного курса лечения Церебролизином в сравнении с плацебо (табл. 2) [40]. Больные принимали аспирин каждый день на протяжении полных 90 дней исследования, в то время как Церебролизин (n = 529) или плацебо (n = 540) пациенты получали на протяжении только первых 10 дней [40]. В исследовании CASTA средний балл по шкале NIHSS равнялся 9, что соответствует инсульту умеренной тяжести.
Предварительные результаты, основанные на данных о первичных исходах, показали, что не было существенной разницы между пациентами, которые получали Церебролизин и плацебо. Возможным объяснением данного явления (нейтральных результатов) является то, что в исследовании CASTA оценка по шкале NIHSS при лечении Церебролизином (среднее значение 9) была значительно ниже таковой в подобных исследованиях (среднее значение 12) [42–44]. У большинства пациентов имел место ишемический тип ОНМК средней степени тяжести, после которого естественное восстановление наступало быстрее, что может отражать эффект «потолка», граничного показателя восстановления, причем дальнейшее восстановление функций под влиянием препарата Церебролизин невозможно. Анализ подгрупп пациентов выявил наличие 3 групп тяжести заболевания в рамках исследования CASTA. Анализ группы пациентов с тяжелым ишемическим ОНМК (оценка > 12 по шкале NIHSS, исходные данные) показал значительное различие результатов у пациентов, которые получали Церебролизин (n = 125), по сравнению с теми, кто получал плацебо (n = 121).
Профессор Bornstein пришел к выводу, что анализ первичных результатов CASTA не выявил статистически достоверных данных о пользе и преимуществах Церебролизина. Пациенты, которые перенесли ишемическое ОНМК средней степени тяжести, характеризовались наличием эффекта «потолка», хотя в группе пациентов с оценкой > 12 по шкале NIHSS (тяжелое ОНМК) прослеживались положительные эффекты терапии Церебролизином в плане оценок по шкалам NIHSS и mRS. Важно то, что Церебролизин безопасен и хорошо переносится, с минимальным количеством побочных эффектов. Все пациенты одинаково строго соблюдали назначенный режим лечения.
В свете положительных результатов предыдущих исследований и положительных тенденций, которые четко прослеживаются в подгруппах пациентов в исследовании CASTA, управленческий комитет пришел к выводу, что «есть необходимость изучения отдаленных результатов применения Церебролизина с использованием добавочного протокола, который может привести к клинически значимому исходу». В таком исследовании будет применяться комбинированное лечение в остром периоде и долговременное лечение для потенцирования процессов восстановления, а при помощи оценки по шкале NIHSS будут исключены пациенты с ишемическим ОНМК средней степени тяжести.
В заключение проф. Bornstein отметил, что «Церебролизин является безопасным препаратом и хорошо переносится, может быть использован для лечения пациентов с ишемическим ОНМК средней степени тяжести, значительно улучшает клинические исходы у пациентов с более тяжелыми ишемическими ОНМК».
Заключительные ремарки
На этом симпозиуме обсуждали экспериментальные и клинические данные, поддерживающие применение нейропротекторов и многоцелевых фармакологических препаратов для лечения пациентов с ОНМК. Принимая во внимание огромный объем положительной информации из многих клинических исследований, можно сделать вывод, что Церебролизин может применяться в лечении ОНМК, однако необходимо учитывать измененные критерии оценки. Как было отмечено в 3 презентациях, существует необходимость в углублении нашего понимания патологических процессов и фундаментальных механизмов ОНМК с тем, чтобы обеспечить развитие новых и улучшенных методов лечения для дальнейшего переноса последних из эксперимента к постели больного, направленных на решение важных задач в лечении ОНМК.
Перевод Константина Кремца
Список литературы находится в редакции


