Газета «Новости медицины и фармации» Офтальмология (417) 2012 (тематический номер)
Вернуться к номеру
Ретинопатия недоношенных
Авторы: Н.В. Пасечникова, д.м.н., профессор, ГУ «Институт глазных болезней и тканевой терапии им. В.П. Филатова НАМН Украины», г. Одесса
Версия для печати
Ретинопатия недоношенных (РН) — тяжелое заболевание недоношенных младенцев, связанное с нарушением развития сосудистой системы сетчатки. На сегодняшний день это одна из главных причин, которая может привести к необратимой потере зрения у детей с раннего возраста. Несмотря на то что вопросами своевременной диагностики и лечения занимаются ученые по всему миру, многие аспекты этой проблемы остаются малопонятными и требуют тщательного изучения. Необходимо отметить, что через 70 лет после первых случаев слепоты в результате РН мы продолжаем борьбу с эпидемией РН. В 1950 году количество случаев РН в США достигло 7000, при этом она составила 30 % в структуре детской слепоты. В мировой литературе это упоминается как первая классическая эпидемия РН. В начале 70-х гг. прошлого столетия неонатология была выделена в педиатрическую субспециальность. Это повлекло появление новых неонатологических технологий, что привело к увеличению выживаемости детей с экстремально низкой массой тела при рождении. Это обусловило повторение пика заболеваемости, наблюдавшегося в 1943–1953 годах. Второй всплеск заболеваемости продолжается и по сегодняшний день, в литературе он получил название второй эпидемии РН.
Этиопатогенез
Васкуляризация (формирование сосудов) сетчатки плода начинается на 16-й неделе внутриутробного развития и заканчивается к моменту рождения, то есть к 39–40-й неделе. Соответственно, чем раньше родился ребенок, тем меньше площадь сетчатки покрыта сосудами. У 7-месячного плода отмечается концентрическое недоразвитие сосудов сетчатки, так как кровоснабжается только ее центральный отдел. После рождения на процесс образования сосудов у недоношенного малыша действуют различные факторы: внешняя среда, свет, кислород, которые могут привести к развитию ретинопатии недоношенных.
Впервые это заболевание было описано в 1942 году американским офтальмологом Т. Терри. Тогда он описал позднюю клиническую картину заболевания и дал ему название «ретролентальная фиброплазия». Спустя 6 лет американские офтальмологи описали ранние сосудистые изменения заднего отдела глаза при этой патологии и выделили этапы морфологических изменений сетчатки. Позднее врачами была установлена связь между нарушением роста сосудов и высокой концентрацией кислорода в инкубаторах для выхаживания новорожденных.
Известно, что гестационный возраст и вес ребенка являются определяющими факторами риска в частоте возникновения РН, в то время как характер течения заболевания может зависеть от наличия множества факторов риска, отражающих соматическую отягощенность. К ним относятся внутриутробная задержка развития плода, выраженные колебания оксигенации, наличие тяжелых кардиоваскулярных и респираторных расстройств, тяжелые внутриутробные инфекции, гипоксия мозга в результате осложнений беременности и родов, внутрижелудочковые кровоизлияния, анемия, многоплодная беременность, генетическая предрасположенность и др.
Классификация РН
В 2005 году была пересмотрена и опубликована Международная классификация ретинопатия недоношенных (МКРН). Сегодня в ней сочетаются как система начальной МКРН, так и рекомендуемые дополнительные изменения. Основными критериями регистрации патологического процесса при РН являются: локализация, распространенность, активность, форма РН, стадия заболевания, наличие дополнительных признаков.
Для определения локализации и распространенности заболевания необходимо охарактеризовать три концентрические зоны вовлечения сетчатки (рис. 1).
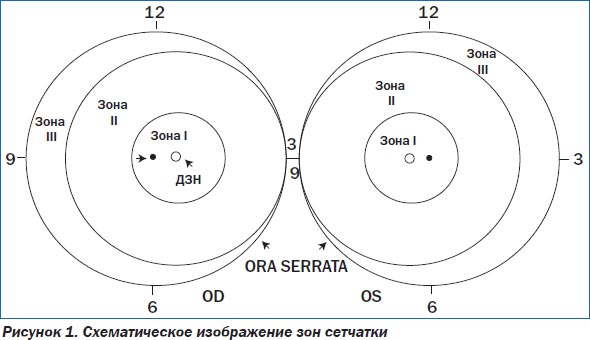
Зона I (наиболее дальняя внутренняя зона) представляет собой круг, радиус которого равен удвоенному расстоянию от центра диска зрительного нерва до центра макулы (рис. 1). Зона II распространяется центробежно от края зоны I с темпоральной стороны до зубчатой линии назальной стороны. Зона III — остаточный полумесяц сетчатки, находящейся спереди зоны II. Зоны II и III являются взаимоисключающими. Считается, что ретинопатия недоношенных находится во второй зоне, пока не определена полная васкуляризация назальной стороны сетчатки.
Распространенность РН записывают в соответствии с часами циферблата или как сектора по 30°. Границы между секторами находятся в положениях часов циферблата, т.е. один сектор соответствует одному часовому промежутку (рис. 1).
Для характеристики ненормальной васкулярной реакции на границе васкуляризированной и аваскулярной сетчатки выделяют пять стадий активной РН.
Стадия 1. Демаркационная линия, разделяющая васкуляризированную и аваскулярную сетчатку. Линия тонкая, относительно плоская, белая и находится в пределах плоскости сетчатки. Кроме этого, определяется ненормальное разветвление сосудов, направленных к демаркационной линии. Нужно отметить, что васкулярные изменения могут проявиться до образования демаркационной линии в виде расширения периферических ретинальных сосудов.
Стадия 2. На месте демаркационной линии образуется так называемый гребень, это признак второй стадии РН. Гребень выглядит шире и начинает проминировать в стекловидное тело. Он располагается над плоскостью сетчатки. Его цвет может меняться с белого на розовый. На данном этапе формирования РН определяется выраженная сосудистая реакция в виде извитости и расширения ретинальных сосудов, формирования артериовенозных шунтов. Позади гребневой структуры нередко определяются отдельные пучки неоваскулярной ткани, лежащие на поверхности сетчатки. Нужно отметить, что в 70–80 % случаев первая и вторая стадия РН регрессируют самопроизвольно.
Стадия 3. Экстраретинальная фиброваскулярная пролиферация или неоваскуляризация — основной критерий третьей стадии РН. При незначительной распространенности неоваскуляризации возможен самопроизвольный регресс РН. Однако не исключены поздние осложнения ввиду остаточных изменений на сетчатке.
Стадия 4. Частичная отслойка сетчатки. Разделяется на экстрафовеальную, без вовлечения макулярной области (стадия 4А), и фовеальную, с вовлечением макулярной области (стадия 4В), частичную отслойку сетчатки. Площадь отслойки сетчатки зависит от степени выраженности и распространенности патологического процесса. Обычно отслойка сетчатки начинается на границе фиброваскулярной пролиферации и васкуляризованной сетчатки.
Стадия 5. Полная отслойка сетчатки. В большинстве случаев тракционная, а иногда может быть экссудативной. Обычно ее форма напоминает воронку, которая разделена на переднюю и заднюю части.
Наряду с изменениями, описанными выше, могут наблюдаться дополнительные признаки, указывающие на тяжесть активной РН.
Симптом «плюс болезнь»
В начальной классификации набор признаков, в число которых входили венозное расширение и артериолярная искривленность задних ретинальных сосудов, закупорка сосудов радужки, плохое расширение зрачка (ригидный зрачок) и помутнение стекловидного тела, назывался симптомом «плюс болезнь». В пересмотренной классификации симптом «плюс болезнь» устанавливался при наличии расширенных и искривленных сосудов как минимум в 2 квадрантах глаза.
Пре-«плюс болезнь»
Симптом, который определяется как промежуточное состояние между «плюс болезнью» и нормальными сосудами заднего полюса. Минимальные изменения сосудов заднего полюса соответствует пре-«плюс болезни». Со временем пре-«плюс болезнь» может прогрессировать до явного симптома «плюс болезнь» по мере того, как сосуды расширяются и становятся более извитыми.
 Агрессивная задняя РН
Агрессивная задняя РН
Редко встречающаяся, быстро прогрессирующая, тяжелая форма РН обозначена как АЗ-РН. Без лечения она обычно развивается до пятой стадии РН. Характерная особенность этого типа РН — ее локализация в первой или задней второй зоне, явное наличие симптома «плюс болезни» и слабовыраженная природа характерных для классической формы РН изменений (рис. 2). Ранее эту быстро прогрессирующую ретинопатию называли «РН типа II», или «лихорадочной болезнью», но ее не указывали в первом варианте МКРН. АЗ-РН характеризуется плоской, почти неприметной неоваскуляризацией между васкуляризованной и неваскуляризированной зонами сетчатки. Нужно отметить, что АЗ-РН является той формой заболевания, которая наиболее часто становится причиной необратимой слепоты.
Регресс РН
Большая часть случаев РН первой, второй стадии регрессирует сама по себе. Один из первых признаков стабилизации острой фазы РН — отсутствие перехода активной РН в следующую стадию. Для начала регресса характерны определенные морфологические признаки. Цвет гребня может меняться с оранжево-розового на белый. Чем тяжелее острая фаза ретинопатии, тем выше вероятность тяжелых инволюционных изменений по мере вступлении болезни в фазу, которую назвали «рубцовой». Тракция и регматогенная отслойка сетчатки, редко — экссудативная отслойка могут развиться как поздние осложнения регрессировавшей РН.
Особенности скрининга недоношенных детей с РН
Активный скрининг — единственный способ ранней диагностики РН. Своевременное выявление и профилактическое лечение детей с РН — основные составляющие благоприятного исхода заболевания. В настоящее время во всех развитых странах существуют национальные программы по РН. Разработаны и строго выполняются стандарты по выявлению и оказанию плановой и неотложной медицинской помощи недоношенным детям с ретинопатией недоношенных. Результатом такого многолетнего подхода к решению проблемы РН в странах Западной Европы стало снижение частоты возникновения и развития тяжелых форм РН. В Великобритании PН составляет 3 % от всей детской слепоты, в США — 13 %. В среднеразвитых странах более зрелые дети с большей массой при рождении находятся в группе риска развития этой болезни. В различных областях Мексики 62 % детской слепоты возникает из-за PН. Для многих стран в настоящее время PН становится огромной проблемой. Для этого существует целый ряд возможных причин, включая большое количество родов и большую частоту недоношенности. Недостаточная медицинская помощь новорожденным вследствие нехватки средств приводит к большей частоте тяжелой РН не только у глубоко недоношенных младенцев, но и у более зрелых детей.
Основными критериями проведения скрининга остаются гестационный возраст и вес ребенка при рождении. Схема скрининговых осмотров в развитых и развивающихся странах различна. У младенцев развивающихся стран наблюдается тенденция к возникновению РН в более зрелом состоянии, нежели у таких же детей в западных странах.
Большинство развитых стран (США, Великобритания, Канада, Швеция) имеют схожие нормы скрининга. Дети весом менее 1500 г при рождении или гестационным возрастом менее 32 недель должны быть скринированы на предмет РН. В странах с развивающейся экономикой критерии скрининга несколько отличаются. Например, в Индии осмотр проходят дети с массой тела при рождении менее 1700 г и/или гестационным возрастом менее 35 недель. В России группу риска развития РН составляют недоношенные дети, родившиеся в сроки до 35 недель беременности с массой тела до 2500 г. В соответствии с протоколом осмотра офтальмологом недоношенных детей в Украине дети с гестационным возрастом менее 37 недель должны быть осмотрены на предмет РН.
Первое скрининговое обследование на предмет РН должно быть проведено настолько рано, насколько возможно будет выявить первые признаки РН, угрожающие зрению. Как правило, первый осмотр должен произойти к 4–5-й неделе послеродового возраста. На основании первого скринингового осмотра можно определить, когда нужны последующие обследования и нужны ли они вообще. Благодаря исследованию по раннему лечению РН (РЛРН) обнаружили, что наличие симптома «плюс болезнь», обширных аваскулярных зон сетчатки (сосуды, заканчивающиеся в I или задней II зоне), РН 3-й стадии связано с вероятным последующим лечением ребенка с РН. На основании этих данных можно сделать вывод о том что, признаки быстро развивающегося заболевания свидетельствуют о необходимости более тщательного динамического наблюдения, то есть скрининг должен проводиться как минимум еженедельно. В других ситуациях, когда отсутствуют признаки 3-й стадии РН, не наблюдаются явления «плюс» и пре-«плюс болезни», РН (1–2-я стадия) локализуется в 3-й зоне, скрининг можно проводить каждые две недели, так как риск прогрессирования РН, угрожающей зрению, невысок. Скрининг можно прекратить на этапе полной васкуляризации сетчатки для детей, у которых не была диагностирована РН. Окончание скрининга обычно приходится на 42-ю полную неделю постконцептуального возраста.
Золотым стандартом выявления РН является бинокулярная непрямая офтальмоскопия, однако в последние годы новые технологии дали возможность применения альтернативных вариантов для скрининга РН, таких как цифровая фотография глазного дна с широким полем.
После проведенного обследования необходимо вести офтальмологические дневники, где детально должны быть указаны зона, стадия и протяженность любой РН, наличие симптома пре-«плюс болезни» или «плюс болезни», рекомендация по определению времени следующего обследования. В обязательном порядке необходимо информировать родителей о том, что их ребенка будут осматривать на предмет РН, а также предоставить письменную информацию о процедуре скрининга и о риске и последствиях развития тяжелой формы РН.
Тактика наблюдения недоношенных детей без РН и детей с 1–2-й стадией РН схожа. Детей осматривают между 1 и 5 годами в соответствии с плановыми осмотрами офтальмолога. Всех детей с 3-й стадией РН, регрессировавшей самопроизвольно, и детей, которым проводилось лечение, необходимо осматривать до пятилетнего возраста в специализированном офтальмологическом учреждении.
Лечение
Лечение РН — это хирургическая процедура. Эффективный скрининг и профессионализм персонала во время лечения может свести к минимуму риск и степень тяжести возможных осложнений.
Первые данные успешного лечения РН стали известны благодаря многоцентровому исследованию КРИО-РН. B этом исследовании было проведено сравнение результатов лечения РН на пороговой стадии методом криотерапии с естественным течением заболевания. Наблюдение длилось 15 лет (осмотры проводились через 3 месяца, 1, 3,5; 5,5; 10 и 15 лет), таким образом были получены первые данные о долговременных структурных и функциональных показателях. Данные исследования КРИО-РН показали, что нежелательных структурных результатов, в число которых входит отслойка сетчатки, было меньше в группе, где применялось лечение, чем в группе с естественным течением РН. Однако процентная доля глаз с нежелательными результатами увеличилась со временем в обеих группах с 25,1 % через один год до 30,0 % через 15 лет в группе детей, которым проводили лечение, и с 44,7 до 51,9 % в группе с естественным течением РН.
Благодаря данным исследования КРИО-РН через 10 лет возникла необходимость нового исследования раннего лечения ретинопатии недоношенных, в ходе которого оценили результаты лечения на предпороговой стадии по сравнению с традиционным лечением.
В 2006 году были опубликованы результаты наблюдения после раннего лечения ретинопатии недоношенных с использованием лазерного излучения. Целью данного исследования было выяснить влияние раннего лечения ретинопатии недоношенных с высоким уровнем риска на структурный результат сетчатки в возрасте 2 лет. Детям с двусторонней предпороговой РН (табл. 1), с высоким уровнем риска прогрессирования процесса лечили один глаз.

Второй глаз лечили традиционно, то есть на этапе развития пороговой стадии заболевания. В возрасте 2 лет детей обследовали для определения структурного результата. В результате проведенного исследования были получены данные по 339 из 374 (90,6 %) выживших детей. При осмотре детей в возрасте 2 лет показатель неблагоприятных структурных результатов уменьшился с 15,4 % (глаза, которые лечили традиционно) до 9,1 % (глаза, для которых применили раннее лечение) (р = 0,002). Осложнения в виде катаракты, глаукомы и повреждения роговицы были схожими при раннем и традиционном лечении. На этапе двухлетнего исследования не учитывались функциональные критерии (например, острота зрения). Однако, учитывая связь между структурой и функцией, известную по предыдущим исследованиям, можно предположить, что глаза после лазерного лечения предпороговой РН с высоким риском прогрессирования отличаются лучшими функциональными результатами, чем глаза, леченные традиционно.
Результаты состояния сетчатки спустя 6 лет подтвердили эффективность раннего лечения. Эта эффективность была отмечена в 6- и 9-месячном возрасте и сохранялась до 6 лет. Благодаря применению раннего лечения было отмечено улучшение остроты зрения, однако в 65,4 % случаев ее значения составляли не более 0,5. Связано это с ретинальными, кортикальными или обеими группами факторов, остается невыясненным.
Таким образом, раннее лечение РН является предпочтительным для ряда пациентов, хотя не всегда способствует нормальному развитию остроты зрения.
Практикуемые схемы лазерной коагуляции менялись за последние 15 лет. Наиболее предпочтительна схема нанесения прижогов сливного характера, нежели разбросанного.
Самое распространенное осложнение при лазерном вмешательстве — это «пропущенные зоны», которые приводят к продолжительной ненормальной васкуляризации, влекущей за собой отслойку сетчатки. Другие осложнения возникают редко. К показаниям для криопексии вместо лазерной коагуляции при РН относятся плохая видимость глазного дна (кровоизлияние в стекловидное тело или проблемы с передним сегментом) и недоступность лазерного лечения. При этом криокоагуляция остается альтернативным методом лечения РН.
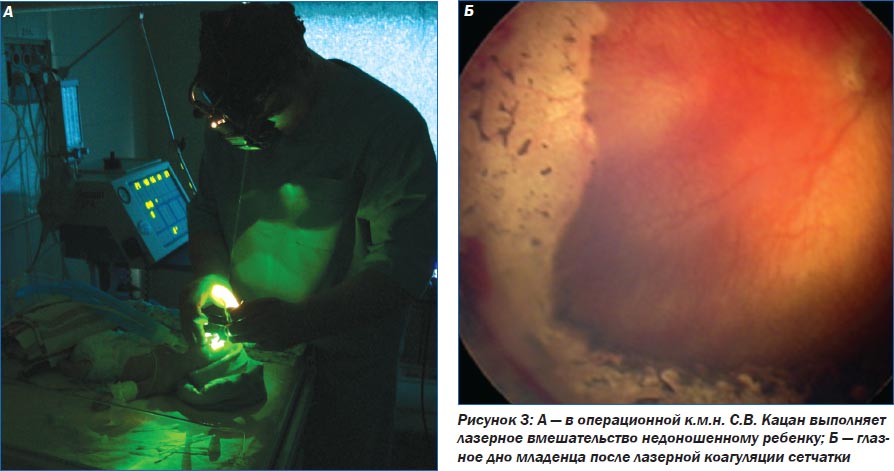
В настоящее время лазерная коагуляция (рис. 3) считается наиболее эффективным методом лечения РН. Она приводит к меньшему числу осложнений, чем криотерапия, и отличается как минимум такими же хорошими результатами с точки зрения анатомии и зрения.
Данные исследования КРИО-РН указывают на связь быстрого прогрессирования РН и роста риска развития неблагоприятного результата. Был утвержден стандарт 48 часов между определением агрессивной задней формы РН и осуществлением лечения. В случае классического типа течения РН лазерная коагуляция осуществляется обычно в пределах 72 часов. Лечение должно проводиться в неонатальном учреждении, где гарантирована немедленная скорая помощь и необходимый уход за детьми.
Таким образом, РН является комплексной проблемой. Функциональные исходы зависят не только от степени остаточных изменений после перенесенной РН, но и от сопутствующей патологии и поздних осложнений.
При неуклонном росте не только числа детей с РН, но и тяжести этого заболевания, необходимы пожизненное динамическое наблюдение и дифференцированная тактика профилактического и реабилитационного лечения всех пациентов, перенесших даже легкую степень РН, с целью предотвращения развития поздних осложнений.
1. Наследственные и врожденные заболевания сетчатки и зрительного нерва / Под ред. A.M. Шамшиновой. — М.: Медицина, 2001. — 528 с.
2. Пасечникова Н.В., Боброва Н.Ф., Кацан С.В., Уманец Н.Н. Опыт лазерного лечения ретинопатии недоношенных детей // XII Съезд офтальмологов Украины. — 2010. — 260-261.
3. Ретинопатия недоношенных 2011: сборник трудов Всероссийской научно-практической конференции с международным участием. Москва, 7 апреля 2011 г. — М.: ФГУ «МНИИ ГБ им. Гельмгольца» Минздравсоцразвития России, 2011. — 247 с. + цв. вклейка 8 с.
4. Рыков С.А. Ретинопатия недоношенных / С.А. Рыков, С.А. Сук, Н.В. Пасечникова // Офтальмологический журнал. — 2003. — Т. 1. — С. 57-60.
5. A classification of retrolental fibroplasia // Am. J. Ophthalmol. — 1953. — 36. — 1333-1335.
6. Darlow B.A. et al. Promise and potential pitfalls of anti-VEGF drugs in retinopathy of prematurity // Br. J. Ophthalmol. — 2009. — 93. — 986. doi:10.1136/bjo.2008.156208.
7. Committee for the Classification of Retinopathy of Prematurity. An International Classification of Retinopathy of Prematurity // Arch. Ophthalmol. 1984. — 102. — 1130-134.
8. Connolly B.P., McNamara J.A., Sharma S., Regillo C.D., Tasman W. A comparison of laser photocoagulation with trans-scleral cryotherapy in the treatment of threshold retinopathy of prematurity // Ophthalmology. — 1998. — 105(9). — 1628-1631.
9. Cryotherapy for Retinopathy of Prematurity Cooperative Group. Multicenter trial of cryotherapy for retinopathy of prematurity. One-year outcome-structure and function // Arch. Ophthalmol. — 1990. — 108(10). — 1408-1416.
10. Cryotherapy for Retinopathy of Prematurity Cooperative Group. Multicenter trial of cryotherapy for retinopathy of prematurity. Preliminary results // Arch. Ophthalmol. 1988. — 106(4). — 471-479.
11. Efficacy and safety of green laser photocoagulation for threshold retinopathy of prematurity // Arq. Bras. Oftalmol. — 2008. — 71(1). — 49-51.
12. Fielder A.R., Shaw D.E., Robinson J., Ng Y.K. Natural history of retinopathy of prematurity: a prospective study // Eye. — 1992. — 6 (Pt 3). — 233-242.
13. Final Visual Acuity Results in the Early Treatment for Retinopathy of Prematurity Study // Arch. Ophthalmol. — 2010. — 128(6). — 663-671.
14. Gilbert C., Rahi J., Eckstein M., O’Sullivan J., Foster A. Retinopathy of prematurity in middle-income countries // Lancet. — 1997. — 350. — 12-4.
15. Good W.V. Early Treatment for Retinopathy of Prematurity Cooperative Group. Final results of the Early Treatment for Retinopathy of Prematurity (ETROP) randomized trial // Trans. Am. Ophthalmol. Soc. — 2004. — 102. — 233-248.
16. Good W.V., Hardy R.J., Dobson V., Palmer E.A., Phelps D.L., Quintos M. et al. The incidence and course of retinopathy of prematurity: findings from the early treatment for retinopathy of prematurity study // Pediatrics. — 2005. — 116(1). — 15-23.
17. Haines L., Fielder A.R., Baker H., Wilkinson A.R. UK population based study of severe retinopathy of prematurity: screening, treatment, and outcome // Arch. Dis. Child Fetal Neonatal. Ed. — 2005. — 90(3). — F240-F24420.
18. ICROP Committee for Classification of Late Stages ROP. An international classification of retinopathy of prematurity. II: the classification of retinal detachment // Arch. Ophthalmol. — 1987. — 105. — 906-912.
19. International Committee for the Classification of Retinopathy of Prematurity. The international classification of retinopathy of prematurity revisited // Arch. Ophthalmol. — 2005. — 123(7). — 991-999.
20. Lambert S.R., Capone A. Jr., Cingle K.A. Cataract and phthisis bulbi after laser photoablation for threshold retinopathy of prematurity // Am. J. Ophthalmol. — 2000. — 129(5). — 585-591.
21. Marek E. Prost. Problems of the pathogenesis of ROP. — 2009. — Р. 5.
22. McNamara J.A., Tasman W., Brown G.C., Federman J.L. Laser photocoagulation for stage 3+ retinopathy of prematurity // Ophthalmology. — 1991. — 98(5). — 576-580.
23. McNamara J.A., Tasman W., Vander J.F., Brown G.C. Diode laser photocoagulation for retinopathy of prematurity. Preliminary results // Arch. Ophthalmol. — 1992. — 110(12). — 1714-1716.
24. Nagata M. Treatment of acute proliferative retrolental fibroplasia with xenon arc photocagulation: its indications and limitation // Jpn J. Ophthalmol. 1970. — 21. — 435-459.
25. Ola Didrik Saugstad. Retinopathy of Prematurity: What Is New? — Oslo, Norway.
26. Palmer E., Flynn J., Hardy R, et al. Incidence and early course of retinopathy of prematurity // Ophthalmology. — 1991. — 98. — 1628-1638.
27. Palmer E.A., Hardy R.J., Dobson V., Phelps D.L., Quinn G.E., Summers C.G. et al. Cryotherapy for Retinopathy of Prematurity Cooperative Group. 15-year outcomes following threshold retinopathy of prematurity: final results from the multicenter trial of cryotherapy for retinopathy of prematurity // Arch. Ophthalmol. — 2005. — 123(3). — 311-318.
28. Repka M.X., Palmer E.A., Tung B.; on behalf of the CRYO-ROP Cooperative Group. Involution of retinopathy of prematurity // Arch. Ophthalmol. — 2000. — 118. — 645-649.
29. Retinopathy of prematurity in Asian Indian babies weighing greater than 1250 grams at birth: Ten year data from a tertiary care center in a developing country // Indian J. Ophthalmol. — 2007. — 55. — 331-6.
30. Reynolds J.D., Dobson V., Quinn G.E., Fielder A.R., Palmer E.A., Saunders R.A. et al. Evidence-based screening criteria for retinopathy of prematurity: natural history data from the CRYOROP and LIGHT-ROP studies // Arch. Ophthalmol. — 2002. — 120(11). — 1470-1476.
31. Roth D.B., Morales D. Screening for retinopathy of prematurity employing the RetCam 120: sensitivity and specificity [abstract] // Invest. Ophtalmol. Vis. Sci. — 1999. — Vol. 40. — P. 2997-3003.
32. Royal College of Paediatrics and Child Health, Royal College of Ophthalmologists & British Association of Perinatal Medicine 2007.
33. Screening for retinopathy of prematurity — a comparison between binocular indirect ophthalmoscopy and RetCam 120 / Parag K. Shah, DNB; V. Narendran, DNB; V.R. Saravanan, FRCS; A. Raghuram, FRCS; Abhijit Chattopadhyay, MS; Maithreyi Kashyap, DNB // Indian J. Ophthalmol. — 2006. — 54. — 35-8.
34. Terry T.L. Extreme prematurity and fibroplastic overgrowth of persistent vascular sheath behind each cristalline lens. Preliminary report // Am. J. Ophtalmol. — 1942. — Vol. 25. — P. 203-204.
35. The International Classification of Retinopathy of Prematurity Revisited // Arch. Ophthalmol. — 2005. — 123. — 991-999.
36. The STOP-ROP Multicenter Study Group. Supplemental therapeutic oxygen for prethreshold retinopathy of prematurity (STOP-ROP): a randomized, controlled trial, l: primary outcomes // Pediatrics. — 2000. — 105. — 295-310.
37. Trese M.T. Retinopathy of prematurity // Retina / Ed. by S.J. Ryan. — 4th ed. — Philadelphia: Elsevier-Mosby, 2006. — P. 2463-76.
38. Wilkinson A.R., Haines L., Head K., Fielder A.R. UK retinopathy of prematurity guideline // Early Human Development. — 2008. — 84. — 71-74.
39. Vander J., Handa J., McNamara A. et al. Early Treatment of posterior retinopathy of prematurity: a controlled trial // Ophthalmology. — 1997. — 104. — 1731-1736.
40. Wagner R.S. Increased incidence and severity of retinopathy of prematurity in developing nations // J. Pediatr. Ophthalmol. Stradismus. — 2003. — 40. — 193.