Журнал «Травма» Том 14, №2, 2013
Вернуться к номеру
Остеопороз: механизм лечебного действия бисфосфонатов и клинические перспективы
Авторы: Дедух Н.В., ГУ «Институт патологии позвоночника и суставов им. проф. М.И. Ситенко НАМН Украины», г. Харьков
Рубрики: Ревматология, Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
В статье описаны эффекты бисфосфонатов в отношении увеличения прочности структуры и качества кости, особое внимание уделено ибандронату. Представлен обзор многоцентровых клинических исследований эффективности ибандроната у женщин с постменопаузальным остеопорозом. Данные этих исследований позволяют сделать вывод, что длительное применение ибандроната в комплексной терапии постменопаузального остеопороза приводит не только к прогрессивному повышению минеральной плотности костной ткани в поясничном отделе позвоночника и проксимальном отделе бедренной кости, но и к снижению маркеров костной резорбции и повышению качества костной ткани.
У статті описані ефекти бісфосфонатів щодо збільшення міцності структури і якості кістки, особливу увагу приділено ібандронату. Наведений огляд багатоцентрових клінічних досліджень ефективності ібандронату в жінок із постменопаузальним остеопорозом. Дані цих досліджень дозволяють зробити висновок, що тривале застосування ібандронату в комплексній терапії постменопаузального остеопорозу призводить не тільки до прогресивного підвищення мінеральної щільності кісткової тканини в поперековому відділі хребта і проксимальному відділі стегнової кістки, але й до зниження маркерів кісткової резорбції і підвищення якості кісткової тканини.
This article describes the effects of bisphosphonates in increasing the strength of the structure and quality of the bone, special attention is paid to ibandronate. The review of multi-center clinical trials of ibandronate efficacy in women with postmenopausal osteoporosis is given. Data from these studies suggest that prolonged use of ibandronate in complex treatment of postmenopausal osteoporosis leads not only to a progressive increase in bone mineral density at the lumbar spine and proximal femur, but to decrease in markers of bone resorption and increased bone quality.
остеопороз, постменопаузальный период, лечение, ибандронат.
остеопороз, постменопаузальний період, лікування, ібандронат.
osteoporosis, postmenopause, treatment, ibandronate.
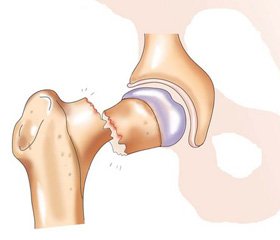
Остеопороз — одно из наиболее распространенных заболеваний, частота которого повышается с возрастом. Во всем мире более 200 млн человек страдают остеопорозом [1, 2]. Тяжелые осложнения остеопороза — остеопоротические переломы проксимального отдела бедра, позвоночника, костей предплечья и др. относят к низкоэнергетическим, в основном они происходят при падении человека с высоты роста. Несмотря на совершенствование диагностической техники и имеющихся эффективных программ профилактики и лечения остеопороза, около 75 % пациентов не лечатся, хотя адекватная медикаментозная терапия с позиции доказательной медицины снижает риск переломов от 30 до 60 % [3].
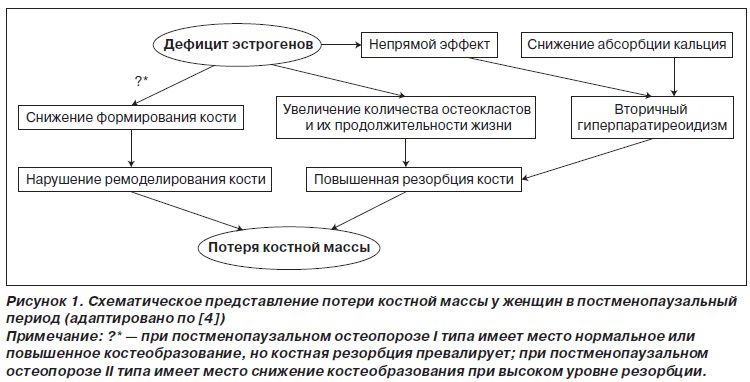
Вторая половина XX века ознаменовалась созданием новой группы препаратов — бисфосфонатов, рекомендованных для лечения остеопороза и других метаболических заболеваний. Бисфосфонаты широко используются в лечении постменопаузального остеопороза, характеризующегося прогрессивной потерей губчатой кости, связанной с дефицитом эстрогенов, который проявляется прямым и непрямым воздействием на костную ткань (рис. 1). Прямое действие при недостатке эстрогенов связано с нарушением остеобластической функции — пула остеобластов и их метаболической активности, что приводит к снижению формирования кости. Увеличение активности остеокластов сопровождается повышением резорбции кости. Это способствует нарушению баланса костного ремоделирования. Непрямой эффект эстрогенов связан со снижением абсорбции кальция и повышением биосинтеза паратгормона. Суммарное действие этих факторов приводит к снижению костной массы.
Бисфосфонаты супрессируют резорбцию кости, снижают уровень костного метаболизма, увеличивают минеральную плотность костной ткани (МПКТ), прочность структуры и качество кости, что снижает риск переломов. В Украине зарегистрировано несколько бисфосфонатов — алендронат, ризендронат, памидронат, ибандронат и золендронат, три из которых — памидронат, ибандронат и золендронат — относятся к группе аминобисфосфонатов.
Механизм влияния. Азотсодержащие бисфосфонаты характеризуются высокоселективным действием на костную ткань, отличаются от других бисфосфонатов более выраженным влиянием на остеокласты и остеолиз [5–7]. Отличительной особенностью бисфосфонатов этого класса является наличие нитратной группы. Широкие клинические перспективы имеет ибандронат (препарат Бонвива®).
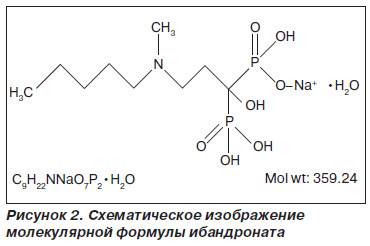
Антирезорбтивный эффект ибандроната как представителя бисфосфонатов имеет сходный механизм действия с другими азотсодержащими бисфосфонатами и направлен на снижение костного ремоделирования путем угнетения резорбции кости [8]. Структурная формула ибандроната представлена на рис. 2.
Ибандронат после введения в организм накапливается на поверхности кости. Его селективное действие основывается на высокой аффинности бисфосфонатов к гидроксиапатиту, минеральной составляющей матрикса костной ткани. Бисфосфонат распределяется по поверхности кости, но наиболее высокая концентрация препарата обнаруживается в очагах резорбции. Основной механизм влияния ибандроната на костную ткань заключается в подавлении активности остеокластов и, соответственно, проявляется снижением резорбции костной ткани. Ибандронат захватывается остеокластами и разрушает их цитоскелет, что сопровождается нарушением подвижности этих клеток и их неспособностью прикрепиться к кости и выполнить функцию резорбции [5, 9]. Под воздействием ибандроната снижается биосинтез и секреция лизосомальных ферментов, подавляется активность протонового насоса. Потенциальные возможности ибандроната в резорбции кости значительно превышают таковые алендроната, памидроната и хлородроната [10].
Отличительной особенностью азотсодержащих бисфосфонатов, в том числе и ибандроната, является блокирование биосинтеза ферментов мевалонатного пути посредством ингибирования фарнезилсинтетазы, важной составляющей для продукции холестерола и изопреноидных липидов [11, 12]. Как результат, имеет место редукция липидов, которые осуществляют пренуляцию ГТФазы, необходимой для организации цитоскелета и везикулярного движения в остеокластах, что приводит к нарушению их функции [13]. Характерной особенностью бисфосфонатов является снижение формирования клетокпредшественников остеокластов, а также нарушение белковых молекул, что ведет к апоптозу зрелых клеток.
Анаболическое действие ибандроната. Азотсодержащие бисфосфонаты стимулируют дифференцировку остеобластов, в то время как бисфосфонаты, не содержащие нитрогенной группы, оказывают слабое влияние на этот процесс [14]. Достоверно установлено, что ибандронат расширяет дифференцировку остеобластов путем повышения экспрессии генов Dlx5, Runx2, OCN, MSX1 и MSX2 [15]. Кроме того, бисфосфонаты ингибируют апоптоз остеоцитов и остеобластов [14, 16].
Ибандронат не метаболизируется. Были проведены исследования как в культуре клеток печени, так и на животных. Доказано, что даже повышение концентрации ибандроната в 1000 раз по отношению к клинически рекомендованным дозам не нарушает изоформы цитохрома Р450 [17]. В целом подобное свойство присуще и другим бисфосфонатам [18].
При применении бисфосфонатов одним из актуальных вопросов является перспективность их прерывистого использования. Для доказательства были проведены исследования на овариэктомированных животных: крысах, собаках и обезьянах [19, 20]. Было выявлено, что интермиттирующий прием препарата способствует сохранению показателей минеральной плотности и повышает качество костной ткани, что было выявлено при морфометрическом исследовании.
Клинические результаты лечения женщин с постменопаузальным остеопорозом показали, что таблетированная форма ибандроната эффективно ингибирует резорбцию кости, увеличивает минеральную плотность и снижает маркеры костного метаболизма [21, 22].
Клиническая эффективность ибандроната была подтверджена данными многоцентровых исследований по изучению его влияния на минеральную плотность костной ткани, качество кости, риск развития переломов и переносимости препарата. В многоцентровом рандомизированном двойном слепом одногодичном исследовании MOBILE (Monthly Oral iBandronate In LadiEs) была дана оценка влияния различных доз ибандроната при частоте приема 1 раз в месяц (150 мг) и при ежедневном приеме (2,5 мг) [23]. В двухлетнем исследовании выявлено, что в обоих случаях имело место повышение минеральной плотности тел позвонков и снижение маркеров костного метаболизма через 3 мес. после приема. Низкий уровень маркеров резорбции сохранялся на протяжении двух лет лечения. В продолжение исследования (трехлетний период) пациентки получали перорально 100 мг (n = 359) или 150 мг (n = 360) ибандроната [24]. После одного дополнительного года лечения установлено, что у пациентов, получавших 150 мг ибандроната ежемесячно, средняя МПКТ поясничного отдела позвоночника повышена на 7,6 % (по сравнению с исходной), а у пациентов, получавших 100 мг в месяц, — на 6,4 % (по сравнению с исходной). Через 3 года в обеих группах пациенток зафиксировано увеличение суммарной минеральной плотности в области проксимального отдела бедренной кости по сравнению с исходной (3,4 % — 100 мг и 4,1 % — 150 мг). Сывороточный Cтелопептид альфацепи коллагена I типа значительно снизился в течение периода лечения, что также свидетельствует о замедлении процесса резорбции.
В последующем исследование MOBILE было продлено (MOBILE LTE) до 5 лет [23]. Установлено, что через 5 лет в поясничном отделе позвоночника показатели МПКТ были повышены на 8,2 и 8,4 % при лечении пациентов ибандронатом в дозе 100 и 150 мг соответственно. Эффективность лечения была также подтверждена при исследовании маркеров костного метаболизма.
Высокая эффективность ибандроната была доказана и при оценке риска снижения остеопоротических переломов в исследовании BONE (Oral iBandronate Osteoporosis Vertebral Fracture Trial in North America and Europa). Выявлено, что риск переломов тел позвонков и внепозвоночных переломов был снижен в двух популяциях — Северной Америки и Европы [25]. Риск переломов тел позвонков у женщин с ежедневным и ежемесячным приемом ибандроната в Северной Америке был снижен на 60 и 54 % соответственно. У женщин европейской популяции зафиксировано снижение риска переломов на 50 и 48 % соответственно. То есть обе схемы лечения пациенток ибандронатом (ежедневный или ежемесячный прием) значительно снижали частоту новых компрессионных переломов тел позвонков. Кроме того, у женщин двух популяций как при ежедневном, так и при ежемесячном приеме ибандроната отмечено значительное увеличение МПКТ по сравнению с исходными показателями в телах позвонков на 5,4 и 4,4 % (популяция Северной Америки) и на 7,1 и 6,3 % (популяция Европы). Повышение на 2,6 и 3,7 % МПКТ при ежедневном приеме отмечено в проксимальном отделе бедренной кости и на 2,5 и 3,1 % — при ежемесячном приеме (пациентки североамериканской и европейской популяции). Наряду с повышением МПКТ отмечено значительное снижение биохимических маркеров костного метаболизма. Так, выявлено снижение на 53,5 и 67,1 % экскреции с мочой Cтелопептида по сравнению с базовым ежедневным приемом, на 50,0 и 53,8 % — при ежемесячном приеме для женщин североамериканской и европейской популяции соответственно. Профиль безопасности ибандроната был сходным с плацебо.
В рамках этого же исследования (BONE) проводилось изучение биоптатов из крыла подвздошной кости пациенток через 22 мес. или через 34 мес. после ежедневного и интермиттирующего (более 2 мес.) приема ибандроната [26]. Была проведена оценка толщины остеоида в губчатой кости, которая была измерена, чтобы исключить возможное нарушение минерализации костной ткани. Кроме того, были оценены объем кости и ее микроархитектура. Во всех костных биоптатах новообразованная губчатая кость сохраняла нормальную структуру без какихлибо признаков деструкции. Фиброза костного мозга и признаков гибели остеоцитов и остеобластов не наблюдалось. Количественные методы оценки не выявили нарушений в минерализации матрикса кости: толщина остеоида, как правило, была аналогичной у пациенток, принимавших ибандронат и плацебо, что свидетельствует о нормально протекающих процессах минерализации. Долгосрочная терапия с применением ибандроната, даже при его введении с интервалом более 2 месяцев, способствует увеличению минеральной плотности кости и сохранению ее микроархитектурной организации.
В двойном слепом исследовании MOTION (Monthly Oral Therapy with Ibandronate for Osteoporosis iNtervention) была оценена эффективность приема 150 мг ибандроната 1 раз в месяц и 70 мг алендроната 1 раз в неделю с дополнительной поддержкой препаратом кальция (500 мг) и витамина D (400 МЕ) [27, 28]. В исследование вошло 1760 женщин в возрасте 55–84 года с остеопорозом (показатели МПКТ тел позвонков L2–L4 были в пределах Tкритерия < –2,5 и ≥ –5,0). Через 1 год лечения у пациенток в поясничном отделе позвоночника МПКТ была повышена на 5,1 и 5,8 %, а также на 2,9 и 3,0 % для проксимального отдела бедра (показатели для ибандроната и алендроната соответственно). Полученные данные свидетельствуют о том, что ежемесячный прием ибандроната и еженедельный прием алендроната являются клинически сопоставимыми с точки зрения повышения МПКТ у женщин с постменопаузальным остеопорозом, но лечение ибандронатом имеет определенные преимущества по снижению частоты гастроэнтерологических расстройств.
Важному вопросу влияния частоты приема ибандроната на комплайентность было посвящено исследование BALTO (Bonviva Alendronate Trial in Osteoporosis). В рамках этого исследования пациенты перекрестно получали ибандронат, а затем алендронат, или вначале алендронат, а затем ибандронат. Было выявлено, что в обоих исследованиях пациенты в 74,6 % случаев высказались за ибандронат как препарат, удобный по способу применения (один раз в месяц), по сравнению с алендронатам (четыре раза в месяц), а 77 % женщин отметили, что у них улучшилось качество жизни по сравнению с приемом алендроната [29].
Имеется доказательная база, что ибандронат в дозе 2,5 и 5 мг при лечении пациенток с остеопорозом наряду со снижением на 70 % маркера костной резорбции Cтелопептида коллагена I типа снижает деструкцию суставного хряща по показателю деградации Cтелопептида коллагена II типа при оценке его концентрации в моче [30]. Полученные данные свидетельствуют, что ибандронат может оказывать хондропротекторный эффект. Однако на сегодняшний день механизм влияния ибандроната на суставной хрящ (прямой или непрямой) не известен.
В доклинических и клинических исследованиях была изучена возможность использования ибандроната в виде внутривенных инъекций. В нескольких рандомизированных клинических исследованиях было показано, что при лечении пациенток в постменопаузальном периоде инъекционной формой ибандроната имеет место сходное с таблетированной формой влияние на минеральную плотность костной ткани и маркеры костного метаболизма [7]. Для определения оптимальной дозы при внутривенном режиме лечения женщин с постменопаузальным остеопорозом ибандронатом было проведено исследование DIVA (Dosing IntraVenous Administration). В результате двухгодичного исследования в группах пациенток, получавших 2 и 3 мг ибандроната внутривенно, выявлено, что МПКТ в поясничном отделе позвоночника была повышена на 6,4 и 6,3 %, а при ежедневном приеме 2,5 мг препарата — на 4,8 %. Кроме того, обе дозы ибандроната обеспечили положительный прирост МПКТ в области проксимального отдела бедренной кости по сравнению с исходными показателями и с ежедневным приемом препарата. При сравнении маркера костной резорбции Cтелопептида коллагена I типа в сыворотке крови перед внутривенным введением ибандроната и после лечения было выявлено значительное снижение этого показателя, которое было аналогичным при приеме 3 мг 1 раз в три месяца или 2,5 мг ежедневно перорально (55,6; 53,4; 59,9 % соответственно). Таким образом, двухгодичное исследование DIVA показало, что внутривенное введение ибандроната является эффективным, хорошо переносится пациентами и представляет собой альтернативу пероральной форме. Для последующей оценки МПКТ, маркеров костного метаболизма и безопасности при длительном использовании внутривенной формы ибандроната у пациенток с постменопаузальным остеопорозом исследование DIVA было продлено на 3 года (DIVA LTE — longterm extension). В пятилетний анализ было включено 497 пациенток. К концу исследования отмечено увеличение на 8,4 и 8,1 % показателей МПКТ в области позвоночника в группах женщин, получавших ибандронат в дозах 2 и 3 мг соответственно [31].
По результатам исследования DIVA положительно ответили на лечение ибандронатом как при внутривенном, так и при пероральном приеме 9 из 10 пациенток [32].
Таким образом, следует отметить, что современная медицина имеет в своем арсенале эффективные методы профилактики и лечения остеопороза. В повседневной клинической практике существенно возрастают возможности остеотропной терапии при применении ибандроната (зарегистрированного в Украине как препарат Бонвива®) — азотсодержащего бисфосфоната, который, как показали преклинические и клинические исследования, высокоэффективен в профилактике и лечении остеопороза. Длительное его применение в комплексной терапии постменопаузального остеопороза приводит не только к прогрессивному повышению МПКТ в поясничном отделе позвоночника и проксимальном отделе бедренной кости, но и к снижению маркеров костной резорбции и повышению качества костной ткани.
- Efficasy end tolerability of oncemonthly oral ibandronate in postmenopausal osteoporosis: 2 year results from the MOBILE study / J.Y. Reginster, S. Adami, P. Lakatos et al. // Ann. Rheum. Dis. — 2006. — Vol. 65. — P. 654661.
- Reginster J.Y. Clinical utility of a pharmacostatistical model for ibandronate in postmenopausal osteoporosis / J.Y. Reginster, R. Gieschke // Curr. Drug Metab. — 2006. — Vol. 7. — P. 827836.
- Nguyen T.V. Osteoporosis: underrated, underdiagnosed and undertreated / T.V Nguyen, J.R Center, J.A. Eisman // MJA. — 2004. — Vol. 180. — S18S22.
- Riggs B.L. A unitary model for involutional osteoporosisestrogen deficiency causes both type I and type II osteoporosis in postmenopausal women and contributes to bone loss in aging men / B.L. Riggs, S. Khosla, L.I. Melton // J. Bone Miner. Res. — 1998. — Vol. 13. — P. 763773.
- Rogers M.J. New insights into molecular mechanisms of action of bisphosphonates / M.J. Rogers // Curr. Pham. Des. — 2003. — Vol. 9. — Р. 26432458.
- Papapoulos S.E. Changes in bone remodelling and antifracture efficacy of intermittent bisphosphonate therapy: implications from clinical studies with ibandronate / S.E. Papapoulos, R.C. Schimmer // Ann. Rheum. Dis. — 2007. — Vol. 66. — P. 853858.
- Papapoulos S.E. Ibandronate: a potent new bisphosphonate in the management of postmenopausаl osteoporosis / S.E. Papapoulos // IJCP. — 2003. — Vol. 57. — P. 417422.
- Bisphosphonates: an update on mechanisms of action and how these relate to clinical efficacy / R.G. Russell, Z. Xia, J.E. Dunford et al. // Ann. NY Acad. Sci. — 2007. — Vol. 1117. — P. 209257.
- Bone safety of longterm bisphosphonate treatment / G. Rodan, A. Reszka, E. Golub, R. Rizzoli // Curr. Med. Res. Opin. — 2004. — Vol. 20, № 8. — P. 12911300.
- BM 21.0955, a potent new bisphosphonate to inhibit bone resorption / R.C. Muаhlbauer, F. Bauss, R. Schenk et al. // J. Bone Miner. Res. — 1991. — Vol. 6. — P. 10031011.
- Nitrogencontaining bisphosphonates inhibit the mevalonate pathway and prevent posttranslational prenylation of GTPbinding proteins, including RAS / S.P. Luckman, D.E. Hughes, F.P. Coxon et al. // J. Bone Miner. Res. — 1998. — Vol. 13. — P. 581589.
- Structureactivity relationships for inhibition of farnesyl diphosphate synthase in vitro and inhibition of bone resorption in vivo by nitrogencontaining bisphosphonates / J.E. Dunford, K. Thompson, F.P. Coxon et al. // J. Pharmacol. Exp. Ther. — 2001. — Vol. 296. — P. 235242.
- Rodan G.A. Bisphosphonate Mechanism of Action / G.A. Rodan, A.A. Reszka // Current Molecular Medicine. — 2002. — Vol. 2. — P. 571577.
- Bisphosphonates: effects on osteoblast / N. Maruotti, A. Corrado, A. Neve, F.P. Cantatore // Eur. J. Clin. Pharmacol. — 2012. — Vol. 68, № 7. — P. 10131018.
- Zoledronate, ibandronate and clodronate enhance osteoblast differentiation in a dose dependent manner — a quantitative in vitro gene expression analysis of Dlx5, Runx2, OCN, MSX1 and MSX2 / F.P. Koch, C. Merkel, B. AlNawas et al. // J. Craniomaxillofac. Surg. — 2011. — Vol. 39, № 8. — P. 562569.
- Prevention of osteocyte and osteoblast apoptosis by bisphosphonates and calcitonin / L.I. Plotkin, R.S. Weinstein, A.M. Parfitt et al. // J. Clin. Invest. — 1999. — Vol. 104. — P. 13631374.
- Ibandronate: a clinical pharmacological and pharmacokinetic update / J. Barrett, E. Worth, F. Bauss, S. Epstein // J. Clin. Pharmacol. — 2004. — Vol. 44. — P. 95165.
- Ibandronate in the Management of Postmenopausal Osteoporosis / J.Y. Reginster, M. Hiligsmann, V. Rabenda et al. // Clinical Medicine: Therapeutics. — 2009. — Vol. 1. — Р. 14091421.
- Russell R.G.G. Ibandronate: pharmacology and preclinical studies / R.G.G. Russell // Bone. — 2006. — Vol. 38. — P. 712.
- Intermittent and continuous administration of the bisphosphonate ibandronate in ovariectomized beagle dogs: effects on bone morthometry and mineral properties / M.C. MonierFaugere, Z. Geng, E.P. Paschalis et al. // J. Bone Miner. Res. — 1999. — Vol. 14. — P. 17681778.
- Ibandronate: a comparison of oral daily dosing versus intermittent dosing in postmenopausal osteoporosis / B.J. Riis, J. Ise, von T. Stein et al. // J. Bone Miner. Res. — 2001. — Vol. 16. — P. 18711878.
- Efficacy and safety of oral weekly ibandronate in the treatment of postmenopausal osteoporosis / C. Cooper, R.D. Emkey, R.H. McDonald et al. // J. Clin. Endocrinol. Metab. — 2003. — Vol. 88. — P. 46094615.
- Monthly oral ibandronate therapy in postmenopausal osteoporosis: 1 year results from the MOBILE study / P.D. Miller, M. McClung, I. Macovei et al. // J. Bone Miner. Res. — 2005. — Vol. 20. — P. 13151322.
- Monthly oral ibandronate is effective and well tolerated after 3 years: the MOBILE longterm extension / J.A. Stakkestad, P. Lakatos, R. Lorenc, F. Sedarati, C. Neate, J.Y. Reginster // Clin. Rheumatol. — 2008. — Vol. 27, № 8. — P. 955960.
- Ibandronate produces significant, similar antifracture efficacy in North American and European women: new clinical findings from BONE / C.H. Chesnut, M.P. Ettinger, P.D. Miller et al. // Curr. Med. Res. Opin. — 2005. — Vol. 21, № 3. — P. 391401.
- Histomorphometric evaluation of daily and intermittent oral ibandronate in women with postmenopausal osteoporosis: results from the BONE study / R.R. Recker, R.S. Weinstein, C.H. Chesnut et al. // Osteoporos Int. — 2004. — Vol. 15, № 3. — P. 231237.
- Oncemonthly oral ibandronate compared with weekly oral alendronate in postmenopausal osteoporosis: results from the headtohead MOTION study / P.D. Miller, S. Epstein, F. Sedarati, J.Y. Reginster // Curr. Med. Res. Opin. — 2008. — Vol. 24. — P. 207213.
- Patient preference for oncemonthly ibandronate versus onceweekly alendronate in a randomised, openlabel, crossover trial: the Bonviva Alendronate trial in osteoporosis // Curr. Med. Res. Opin. — 2005. — Vol. 21. — P. 18951903.
- Effect of bisphosphonates on cartilage turnover assessed with a newly developed assay for collagen type II degradation products / H.J. Lehmann, U. Mouritzen, S. Christgau et al. // Ann. Rheum. Dis. — 2002. — Vol. 61. — P. 530533.
- Efficacy and tolerability of oncemonthly oral ibandronate (150 mg) and onceweekly oral alendronate (70 mg): additional results from the Monthly Oral Therapy With Ibandronate For Osteoporosis Intervention (MOTION) study / R. Emkey, P.D. Delmas, M. Bolognese et al. // Clin. Ther. — 2009. — Vol. 31, № 4. — P. 751761.
- Bianchi G. Longterm administration of quarterly IY ibandronate is effective and well tolerated in postmenopausal osteoporosis: 5year data from the DIVA study longterm extension / G. Bianchi, E. Czerwinski, A. Kenwright et al. // Osteopor. Int. — 2011.
- Eisman J.A. Intermittent intravenous ibandronate injections are an effective treatment in postmenopausal osteoporosis: 2year results from DIVA / J.A. Eisman, P.A. GarciaHernandez, G. OrtizLuna et al. // Osteoporos. Int. — 2006. — Vol. 17, Suppl. 2. — SS. 212.