Журнал «Здоровье ребенка» 2 (61) 2015
Вернуться к номеру
Насущные вопросы рациональной антибиотикотерапии воспалительных заболеваний нижних дыхательных путей в детской практике
Авторы: Охотникова Е.Н., Поночевная Е.В., Шарикадзе Е.В., Усова Е.И. — Национальная медицинская академия последипломного образования имени П.Л. Шупика, г. Киев
Рубрики: Педиатрия/Неонатология
Разделы: Справочник специалиста
Версия для печати
В течение последних 30 лет большую тревогу вызывает высокая частота острых инфекций нижних дыхательных путей бактериальной этиологии, прежде всего пневмоний и бронхитов, лечение которых в условиях распространенной устойчивости к антибиотикам нередко представляет трудную задачу. Бронхиты — одни из наиболее частых после острых респираторных вирусных инфекций заболеваний органов дыхания в детском возрасте. Применение антибиотиков при остром бронхите у детей не рекомендуется, но их назначают при выраженной интоксикации и длительной гипертермии (более 3 дней), особенно у больных раннего возраста, у детей с неблагоприятным преморбидным фоном и высоким риском развития пневмонии. Антибиотикотерапия признана единственным научно обоснованным методом лечения пневмонии. C учетом широкого спектра действия современных антибиотиков наиболее целесообразна монотерапия. При необходимости большего расширения спектра их действия предпочтение отдается комбинации амоксициллина/клавуланата с макролидами, к которым чувствительны все основные возбудители инфекций органов дыхания.
Упродовж останніх 30 років велику тривогу викликає висока частота гострих інфекцій нижніх дихальних шляхів бактеріальної етіології, насамперед пневмоній і бронхітів, лікування яких в умовах поширеної стійкості до антибіотиків нерідко становить складне завдання. Бронхіти — одні з найчастіших після гострих респіраторних вірусних інфекцій захворювань органів дихання в дитячому віці. Застосування антибіотиків при гострому бронхіті в дітей не рекомендується, але їх призначають при вираженій інтоксикації та тривалій гіпертермії (понад 3 дні), особливо у хворих раннього віку, у дітей із несприятливим преморбідним фоном і високим ризиком розвитку пневмонії. Антибіотикотерапія визнана єдиним науково обґрунтованим методом лікування пневмонії. З урахуванням широкого спектра дії сучасних антибіотиків найбільш доцільна монотерапія. За потреби більшого розширення спектра їх дії перевага надається комбінації амоксициліну/клавуланату з макролідами, до яких чутливі всі основні збудники інфекцій органів дихання.
Over the past 30 years, high incidence of acute lower respiratory tract infections of bacterial origin, primarily pneumonia and bronchitis, treatment of which under the spread of antibiotic resistance is often a difficult task, cause alarm. Bronchitis — one of the most common respiratory diseases in childhood after acute respiratory viral infections. Application of antibiotics for acute bronchitis in children is not recommended, but they are prescribed for severe intoxication and prolonged hyperthermia (over 3 days), especially in infants, children with poor premorbid background and high risk of pneumonia. Antibiotic therapy is considered as the only science-based treatment of pneumonia. Taking into account the broad spectrum of modern antibiotics, monotherapy is most suitable. If it is necessary to extend their effect, combination of amoxicillin/clavulanate with macrolides, to which all the major respiratory pathogens are sensitive, is preferred.
острые бронхиты, внебольничные пневмонии, эмпирическая антибиотикотерапия.
гострі бронхіти, позалікарняні пневмонії, емпірична антибіотикотерапія.
acute bronchitis, community-acquired pneumonia, empirical antibiotic therapy.
Статья опубликована на с. 141-148
Конец ХХ — начало ХХІ столетия ознаменовались беспрецедентным ростом инфекционной патологии во всем мире. Это произошло за счет как возврата ранее побежденных инфекций, так и эволюции прежних пневмотропных патогенов [1], а главным образом за счет получения неопровержимых доказательств роли инфекционных патогенов в этиологии многих так называемых соматических заболеваний, в первую очередь практически всей бронхолегочной патологии. Так, внебольничные пневмонии (ВП) у детей в настоящее время обусловлены преобладанием резистентных к традиционной антимикробной терапии пневмококков и условно-патогенной (а сейчас потенциально-патогенной) микрофлоры — микоплазм, хламидий, легионелл, бранхамелл, моракселл, а также различных вирусно-бактериальных ассоциаций [17, 25].
Особую тревогу в этом плане вызывает высокая частота острых инфекций нижних дыхательных путей бактериальной этиологии, прежде всего пневмоний и бронхитов, лечение которых в условиях распространенной устойчивости к антибиотикам нередко представляет трудную задачу.
Бронхиты — одни из наиболее частых после ОРВИ заболеваний органов дыхания в детском возрасте, достигающих среди грудных детей 220 случаев на 1000 в популяции. Среди госпитализированных в стационар число детей с бронхитом составляет 1/2–3/4 от всех больных [20]. Современная этиология острого бронхита представлена в табл. 1 [3].
Заболеваемость ВП у детей повышается в период эпидемий гриппа и имеет тенденцию к устойчивому росту с увеличением тяжелых и осложненных форм. Это обусловлено морфофункциональными и иммунологическими особенностями органов дыхания у детей, а также широчайшим спектром инфекционных патогенов. Даже в экономически развитых странах пневмонии остаются одной из частых причин смертности (13,1 на 100 тыс. детского населения) [23]. К сожалению, погибают в основном дети раннего возраста, а также дети и подростки с низкой антиинфекционной защитой [3].
Распространенность пневмонии в Украине колеблется от 4 до 20 случаев на 1000 детей в возрасте от 1 месяца до 15 лет. Пневмония занимает 3-е место в структуре детской смертности (после заболеваний новорожденных) [2]. Среди всех госпитализированных по поводу пневмонии детей новорожденные составляют менее 1 %, дети в возрасте от 1 до 12 месяцев — 29 %, от 1 года до 5 лет — 50 % и дети старше 5 лет — 20 % [2]. Таким образом, основную группу риска по развитию ВП составляют дети в возрасте от 1 года до 5 лет.
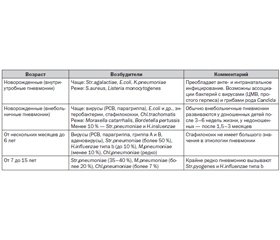
Этиологическая структура ВП весьма разнообразна и зависит от возраста детей (табл. 2).
Несмотря на вышеперечисленные различия пневмоний в зависимости от этиологии, только по данным клинико-лабораторного и рентгенологического обследований трудно четко определить вариант возбудителя. Из 300 видов бактерий заболевания могут вызвать лишь S.pneumoniae, H.influenzae, Moraxella catarrhalis, S.аureus или Chl.pneumoniae, M.pneumoniae, Legionella pneumophila [19, 23]. К сожалению, наличие микроорганизмов в секрете из горла и даже мокроте не доказывает участия данного возбудителя в развитии бронхита или ВП, за исключением случаев, когда обнаруживают редко выявляемые микроорганизмы — клебсиеллу, протей, синегнойную палочку. Единственным надежным методом определения возбудителя является легочная пункция — инвазивная манипуляция, применение которой встречает немало возражений и которая не получила широкого распространения в практической деятельности. Обнаружение микроорганизмов в плевральном выпоте или в лаважной жидкости при бронхоскопии также является диагностически значимым [3].
Поскольку ни один из микробиологических методов ввиду существенных ограничений не может идентифицировать всех потенциальных возбудителей бронхолегочной инфекции, у 30–50 % больных этиологию инфекционного процесса установить не удается, и назначение антимикробных препаратов как в начале, так и в течение заболевания осуществляется в большинстве случаев эмпирически. В связи с этим важно на начальном этапе лечения правильно выбрать лекарственное средство для подавления инфекции с учетом современных данных об этиологии острых бронхитов и пневмоний в зависимости от возраста и фармакологических свойств химиопрепаратов [4].
При адекватном лечении большинство неосложненных ВП разрешаются в течение 2–4 недель, осложненных ВП — 1–2 месяцев. При затяжном течении болезни положительная динамика процесса (чаще сегментарного) отсутствует в сроки от 1,5 до 6 месяцев.
Действующий Протокол диагностики и лечения заболеваний по специальности «детская пульмонология» (приказ № 18 от 13.01.2005 г.) [14] уже не соответствует новым научным данным в отношении лечения бронхитов и пневмоний и не удовлетворяет требованиям, предъявляемым детским здравоохранением. К большому сожалению, в настоящее время новые отечественные клинические рекомендации и унифицированные клинические протоколы по диагностике и лечению острого бронхита и ВП еще находятся в стадии разработки. В связи с этим приходится использовать приемлемые для Украины положения ряда национальных руководств других стран.
Так, применение антибиотиков при остром бронхите у детей Американским колледжем пульмонологов (2006) не рекомендуется, но их назначают при выраженной интоксикации и длительной гипертермии (более 3 дней), особенно у детей раннего возраста, у больных с неблагоприятным преморбидным фоном и высоким риском развития пневмонии [9].
Согласно Британским рекомендациям (2002) по ведению детей с пневмонией, подозрение на бактериальную ее этиологию у всех детей до 3 лет должно возникнуть при лихорадке более 38,5 °С, втяжении грудной клетки и частоте дыхания более 50 в минуту [3, 8, 11, 23, 24]. Антибиотикотерапия признана единственным научно обоснованным методом лечения. Вместе с тем отмечается, что отсутствуют доказательства эффективности применения биогенных стимуляторов, витаминов и иммуномодуляторов (кроме внутривенного иммуноглобулина (IgG) и гранулоцитоколониестимулирующего фактора), повышающих риск нежелательных лекарственных эффектов и увеличивающих стоимость лечения [3, 7, 11, 18]. Назначение Н1-антигистаминных препаратов для предупреждения аллергических реакций на антибиотики не оправданно, поскольку аллергический процесс может развиться независимо от их приема, а клинические его проявления могут быть завуалированы, что в итоге приведет к более тяжелым последствиям. К тому же применение Н1-антигистаминов 1-го поколения тем более нежелательно в связи с их атропиноподобным (подсушивающим) эффектом, что приводит к образованию густой, вязкой мокроты и затрудняет ее эвакуацию. Нестероидные противовоспалительные средства назначают только до достижения жаропонижающего и обезболивающего эффектов. Также нет доказательств в отношении эффективности применения дециметроволновой терапии, токов ультравысокой частоты, магнитотерапии, электро- и фонофореза. Что касается дыхательной гимнастики, то она признается эффективной в случае повышения объема эвакуируемой мокроты более 30 мл в сутки.
С учетом эмпирического назначения антибиотиков решение, с какого препарата следует начать лечение, остается за врачом. Для оптимального выбора антибиотика на этапе стартовой терапии целесообразно выяснить следующие пункты анамнеза:
— где в течение 1–4 недель был ребенок (уезжал ли в другой город или другую страну, болел ли там чем-либо);
— перенесенные инфекции за последние 1–3 месяца;
— применялись ли за последние 3 месяца антибиотики;
— особенности эпидситуации в окружении ребенка (в семье, детском коллективе, в доме).
При эмпирическом выборе стартового антибиотика следует также руководствоваться следующими основными критериями [3]:
1. Эффективность по отношению к основным возбудителям (S.pneumoniae, H.influenzae и внутриклеточные патогены). Если микроорганизм нечувствителен к препарату, то, насколько бы безопасным или доступным по цене он ни был, его применение не показано. Часто очень сложно определить штамм возбудителя, поэтому на практике используют следующее правило: если через 48 часов после начала применения нет признаков улучшения состояния, то необходимо произвести замену антибиотика.
2. Безопасность антибиотика, пренебречь которой можно лишь в случае угрожающих жизни ситуаций.
3. Комплайенс (удобство приема для пациента, обеспечивающее приверженность к лечению). Оптимальным вариантом является однократный (максимум — двухкратный) пероральный прием в течение не более чем 10 суток.
4. Экономическая целесообразность применения.
С учетом оценки состояния ребенка выбор антибактериального препарата должен предусматривать ряд ситуаций (табл. 3).
Рассмотрим основные группы антибиотиков, чтобы определить, насколько целесообразно их применение у пациентов с инфекцией органов дыхания.
Природные пенициллины эффективны против пневмококков, но неэффективны в отношении гемофильной палочки и внутриклеточных возбудителей. Аминопенициллины эффективны против S.pneomoniae и H.influenzae, но к ним устойчивы внутриклеточные возбудители. Цефалоспорины чувствительны только к S.pneomoniae и H.influenzae, но к ним также устойчивы внутриклеточные возбудители [10]. Кроме того, большинство цефалоспоринов применяется в инъекциях, что затрудняет амбулаторное лечение.
Назначение аминогликозидов, цефалоспоринов III поколения и фторхинолонов в качестве стартовой терапии не обосновано. Фторхинолоны уже несколько лет запрещены к применению у детей до 18 лет в связи с их высокой токсичностью. Их используют лишь в крайне тяжелых случаях в качестве резерва при госпитальных инфекциях [18, 22].
Благодаря широкому спектру действия подавляющего большинства современных антибиотиков целесообразно проведение монотерапии. При необходимости большего расширения спектра действия антибиотиков предпочтение отдается комбинации амоксициллина/клавуланата с макролидами, к которым чувствительны все основные возбудители инфекций органов дыхания [3].
В амбулаторной практике в настоящее время нашли широкое применение препараты современных макролидов и защищенные клавулановой кислотой аминопенициллины.
Макролиды обладают высокой эффективностью и в то же время считаются одной из наиболее безопасных групп антибактериальных препаратов: не оказывают токсического влияния на органы и ткани макроорганизма и реже в сравнении с другими антибиотиками вызывают аллергические реакции, что является важным для детской практики. Обладая бактериостатическим механизмом антимикробного действия, современные макролиды отличаются по своим фармакокинетическим качествам, антимикробной активности и переносимости. Им свойственна высокая активность в отношении S.pneumoniae, S.pyogenes, M.pneumoniae, Chl.pneumoniae, Legionella рneumophila, Branchamella catarrhalis, S.aureus и др. Азитромицин и кларитромицин действуют и на H.Influenzae. Ряд штаммов бактерий, устойчивых к пенициллину и другим антибиотикам, сохраняют при этом чувствительность к макролидам [15]. С учетом клинической ситуации (эмпирическое назначение или с учетом бактериологического обследования) азитромицин может использоваться и как препарат первой линии, и как альтернативный антибиотик, и в сочетании с бета-лактамными формами амоксициллина и цефалоспоринов.
Стартовая антибиотикотерапия нетяжелых ВП проводится, как правило, в амбулаторных условиях, даже у дошкольников. Наиболее частым бактериальным возбудителем ВП является S.рneumoniaе [21, 25], реже — H.Іnfluenzae, которые часто устойчивы к природным пенициллинам, поэтому препаратом выбора начальной терапии нетяжелых ВП являются аминопенициллины (амоксициллин, амоксициллин/клавуланат) в пероральных формах. При ВП у ребенка, не получавшего ранее пенициллины, стартовым препаратом служит амоксициллин в суточной дозе 30–60 мг/кг, разделенной на 3 приема. Если ВП вызвана пенициллин-устойчивым пневмококком, его назначают в высоких дозах (90 мг/кг/сут) или используют цефалоспорины ІІІ генерации (цефтриаксон, цефотаксим) в обычных дозах. Аминопенициллины не показаны при аллергии на пенициллин. В этих случаях используют макролиды или цефалоспорины ІІ–ІІІ поколения (риск перекрестной аллергии с пенициллином — 1–3 %) [7]. При подозрении на микоплазменную и хламидийную ВП терапия проводится современными макролидами.
Аминопенициллины и защищенные аминопенициллины. По данным исследования антимикробной резистентности ПеГАС-III (2006–2009 гг.), высокую активность против S.pneumoniae сохраняют амоксициллин и амоксициллин/клавуланат, лишь 0,4 % штаммов проявляют умеренную устойчивость.
Амоксициллин — производное ампициллина, которому присущи бактерицидное действие и широчайший спектр активности в отношении грамположительных кокков (стафилококки, стрептококки, пневмококки, энтерококки) и палочек (листерии, возбудители дифтерии и сибирской язвы), грамотрицательных кокков (менингококки и гонококки), спирохет (трепонемы, лептоспиры, боррелии), спорообразующих (клостридии) и большинства неспорообразующих (исключая Bacteroides fragilis) анаэробных бактерий и актиномицетов. В отличие от пенициллинов аминопенициллины обладают расширенным спектром действия за счет активности в отношении таких грамотрицательных палочек, как H.influenzae, H.рylori, E.coli, Pr.mirabilis, Salmonella spp. и отдельных шигелл [11]. Амоксициллин имеет существенно лучшую фармакокинетику: при пероральном введении его биодоступность составляет более 90 % и не зависит от приема пищи (у ампициллина соответственно 40 % и снижается в 2 раза при одновременном приеме пищи), в результате чего создаются более высокие и стабильные концентрации в крови. Важная особенность амоксициллина — высокое содержание в бронхиальном секрете, в 2 раза превышающее концентрацию в крови [10, 13].
Сочетание амоксициллина с клавуланатом восстанавливает активность амоксициллина против первоначально чувствительных к аминопенициллинам бактерий [16]: пенициллинрезистентных стафилококков, бета-лактамазопродуцирующих штаммов грамотрицательных бактерий — H.influenzae, E.coli и других [18]. Кроме того, добавление клавуланата придает амоксициллину активность в отношении микроорганизмов с природной устойчивостью к аминопенициллинам — бактерий рода Klebsiella, Pr.vulgaris, B.fragilis и некоторых других.
Выбор пути введения препарата зависит от многих факторов. Если ребенок не может принимать препарат внутрь (рвота, психологические проблемы, отсутствие пероральной формы выбранного антибиотика), следует вводить препарат парентерально. Начинать же лечение сразу с инъекционного пути введения антибиотика нецелесообразно, так как наряду с психотравмирующим эффектом происходит и удорожание лечения, повышается опасность развития постинъекционных осложнений [18]. Мнение о более частом развитии дисбактериоза кишечника при пероральном пути введения антибиотиков не имеет никаких реальных доказательств. Независимо от пути введения в итоге они попадают в кровоток, и только таким путем антибиотики воздействуют на микрофлору кишечника, а не влияют на нее непосредственно при прохождении транзитом через весь желудочно-кишечный тракт. При правильно подобранных дозах и сроках антибиотикотерапии дисбиоз кишечника, как правило, не развивается, поэтому назначение пробиотиков и нистатина не является обязательным при применении антибиотиков [3]. При невозможности приема препаратов внутрь следует проводить ступенчатую антибиотикотерапию, предусматривающую парентеральное введение антибиотика в начале лечения с последующим переходом на пероральную форму того же препарата при ее наличии.
Оценку эффективности антибиотикотерапии проводят через 48 часов. В течение 2 суток происходит подавление роста и размножения чувствительных микроорганизмов. Ожидать уменьшения выраженности за это время всех симптомов не стоит: в течение нескольких дней могут сохраняться слабость, снижение аппетита и кашель. По мере угасания проявлений интоксикации улучшается самочувствие ребенка, нормализуется температура тела и постепенно приходят к норме лабораторные показатели. Рентген-признаки ВП угасают медленнее (в среднем 3–4 недели при типичной пневмонии и более длительно при атипичных), чем наступает клиническое выздоровление. Следует помнить о том, что регулярное применение антипиретиков создает ложное впечатление улучшения состояния больного, что затрудняет оценку эффекта антибиотикотерапии.
Длительность антибиотикотерапии в случае типичных возбудителей обычно составляет 3 дня после нормализации температуры (в целом 5–7 дней), а при атипичных патогенах требуется более длительный курс лечения (14 дней) [19, 22]. При низком эффекте лечения необходима замена антибиотика, при этом сроки лечения определяются по той же схеме.
Основным критерием отмены антибиотиков является регресс клинических симптомов. Сохранение отдельных лабораторных и/или рентгенологических изменений не является основанием к продолжению антибиотикотерапии [12].
Назначение антибиотиков при ОРВИ с профилактической целью не предотвращает возможность развития бактериальных осложнений. Частое их применение при вирусных инфекциях приводит лишь к формированию устойчивости к ним бактерий.
Из существующих антибактериальных препаратов для лечения острых бронхитов у детей привлекательны препараты азитромицина, в частности АзитроСандоз®.
АзитроСандоз® — это единственная на украинском рынке суспензия азитромицина моногидрата, растворимость которой в воде на 9,1 % ниже, чем у азитромицина дигидрата, что обеспечивает более быстрое всасывание (повышение биодоступности при приеме внутрь примерно на треть) и лучшее проникновение в клетки в очаге инфекции.
Важными достоинствами суспензии АзитроСандоз® являются удобство в применении (ее легко приготовить, добавив 10 мл воды независимо от дозы) и приятный вкус крем-карамели. Для удобства дозирования прилагается специальный дозировочный шприц АзитроСандоз® объемом 10 мл с небольшим шагом (0,25–0,5 мл), что позволяет точно дозировать препарат и всю его дозу дать за один прием.
Преимуществами суспензии АзитроСандоз® являются также европейское качество и доступная стоимость препарата. Перечисленные достоинства АзитроСандоз® позволяют рассматривать его в качестве препарата выбора для стартовой антибиотикотерапии острого бронхита.
Амоксиклав® (амоксициллин/клавуланат) представлен в виде 2 лекарственных форм — пероральной (суспензия, таблетки в оболочке, диспергируемые таблетки) и парентеральной форме для инъекций, что позволяет индивидуально подобрать лечение для каждого ребенка и в случае его эффективности проводить ступенчатую терапию одним препаратом [SmPC]. Специальная детская форма (суспензия) укомплектована пипеткой-дозатором, что обеспечивает максимально точное дозирование у детей: 2,5 мг по амоксициллину для суспензии 125 мг/31,25 мг в 5 мл и 5 мг для суспензии 250 мг/62,5 мг в 5 мл. Важно отметить, что одной упаковки (флакона) препарата в большинстве случаев достаточно для полного курса лечения. Другая пероральная форма Амоксиклава Квиктаб® (растворимые таблетки) обладает высокой биодоступностью (94 %), сопоставимой с таковой у инъекций (100 %), и лучшей переносимостью (риск диареи в 3 раза ниже в сравнении с приемом таблеток в оболочке). Благодаря относительно невысокой цене Амоксиклав® доступен для большинства украинских пациентов, а замкнутый цикл производства (от субстанции до упаковки производится на одном предприятии — заводе «Лек» в Словении) гарантирует его высокое качество. Следовательно, Амоксиклав®, благодаря своим высоким качествам и будучи защищенным амоксициллином, является препаратом выбора в лечении ВП у детей.
В качестве иллюстраций успешного применения препаратов АзитроСандоз® и Амоксиклав® приводим 2 клинических случая из собственной практики.
Клинический случай 1
Мальчик Павел, 6 лет, поступил в стационар НДСБ «ОХМАТДЕТ» с жалобами:
— на повышение температуры тела до 37,8 °С, умеренную вялость;
— навязчивый сухой кашель и нерезкое затруднение дыхания;
— незначительный насморк, покраснение склер без отделяемого из глаз (рис. 1).
Краткий анамнез болезни: болен в течение 3 дней, когда появились температура тела до 37,4–37,9 °С, легкий насморк, покашливание, перешедшее в частый, навязчивый сухой кашель со скудно отделяемой мокротой, ощущение тяжести в грудной клетке, затруднение выдоха. За 2 недели до начала данного случая перенес ОРВИ средней степени тяжести, в это время болели ОРЗ и старшие члены семьи. Последние 2 года ОРЗ болел редко. Аллергологический семейный и индивидуальный анамнез не отягощены.
Данные осмотра ребенка при поступлении: физическое развитие соответствует возрасту, общее состояние средней тяжести за счет умеренной интоксикации. Частый малопродуктивный кашель с отхождением скудной вязкой слизистой мокроты. Инъекция сосудов склер, умеренная шейная лимфоаденопатия, гиперемия и зернистость слизистой ротоглотки. Одышки нет. ЧДД — 28 в минуту. ЧСС — 88 в минуту. Зев спокоен. Перкуторно над легкими — легочной звук, аускультативно — на фоне жесткого дыхания с удлиненным выдохом обилие сухих свистящих хрипов по всем полям обоих легких, умеренное количество малозвучных средне- и мелкопузырчатых влажных хрипов в обоих легких без четкой их локализации.
Данные рентгенографии органов грудной клетки (для исключения пневмонии): легочный рисунок усилен, корни легких уплотнены, четких инфильтративных теней нет (рис. 2).
В гемограмме патологии не обнаружено, за исключением СОЭ (25 мм/ч).
Заподозрена вирусно-микоплазменная инфекция, которая подтверждена методом полимеразной цепной реакции (ПЦР) назофарингеальной слизи (обнаружен материал антигенов парагриппа ІІІ типа и M.рneumoniae).
Диагноз: острый обструктивный бронхит смешанной этиологии (парагрипп ІІІ типа и микоплазменная инфекция с подтверждением ПЦР), обструктивный синдром, назофарингит, катаральный конъюнктивит.
Лечение:
— С учетом резистентности M.рneumoniae к пенициллинам и цефалоспоринам и высокой ее чувствительности к макролидам, особенно к азалидам, создающим высокие концентрации в очаге воспаления и обладающим иммуномодулирующим действием, препаратом выбора в данном случае является АзитроСандоз®. В связи с высокой адаптацией микоплазм к иммунной системе человека курс лечения препаратом АзитроСандоз® при микоплазмозе должен быть более длительным (5–10 суток). В данном случае АзитроСандоз® назначен в режиме 10 мг/кг/сут в 1–е сутки, затем по 5 мг/кг/сут в течение 4 суток.
— Поскольку у ребенка отмечалось скудное отделение вязкой мокроты, целесообразным было использование муколитиков. Данному ребенку показаны активные муколитики прямого действия, среди которых препаратом выбора является N-ацетилцистеин (АЦЦ). АЦЦ обладает мощным муколитическим и мукокинетическим эффектом, а также антимикробным, антиоксидантным, противовоспалительным, иммуномодулирующим, гепатопротективным и антитоксическим действиями и, кроме этого, уменьшает образование биопленок, в которых микроорганизмы защищаются от воздействия антибиотиков, повышая тем самым эффект антибиотикотерапии. В данном случае назначена жидкая пероральная форма — АЦЦ в растворе (20 мг в 1 мл) в режиме 5 мл 2 раза в день, причем последний прием в 18 часов с последующим откашливанием перед сном.
— Обильное питье минеральной воды без газа.
— Стимуляция откашливания мокроты (при необходимости дренажные положения и вибрационный массаж).
Клинический случай 2
Мальчик Артем, 5 лет, поступил в стационар НДСБ «ОХМАТДЕТ» с жалобами:
— на повышение температуры тела до 39,3 °С;
— частый влажный кашель;
— вялость, отказ от еды.
Краткий анамнез болезни: болен 3 дня, заболевание началось с заложенности носа, появления субфебрильной температуры тела и редкого сухого кашля. Мать самостоятельно использовала растительный сироп от кашля, однако появились признаки интоксикации, кашель усилился, беспокоил в ночное время. Родился в асфиксии средней степени тяжести. С момента посещения детского сада (1,5 года) страдает частыми обострениями рецидивирующего бронхита на фоне ОРЗ (7–8 эпизодов за год длительностью 20–30 дней). Семейный анамнез не отягощен.
Данные осмотра ребенка при поступлении: общее состояние ребенка тяжелое за счет интоксикации (вялость, слабость, бледность с мраморным рисунком кожи), температура кожи 39,4 °С. Одышки нет. ЧДД — 26 в минуту. ЧСС — 130 в минуту. Кашель влажный, но малопродуктивный. Носовое дыхание затруднено, зев несколько гиперемирован, чист. Перкуторный тон над легкими не изменен, выслушиваются влажные малозвучные средне- и крупнопузырчатые хрипы, рассеянные по обоим полям легких на фоне жесткого дыхания. Со стороны сердечно-сосудистой системы — без особых изменений. Живот мягкий. Стул, диурез в норме.
Данные обзорной рентгенографии органов грудной клетки (для исключения пневмонии): инфильтративных теней нет, легочный рисунок усилен, корни легких расширены.
В гемограмме: лейкоцитоз нейтрофильного характера, повышение СОЭ до 28 мм/ч.
Урограмма — без патологических изменений.
Диагноз: рецидивирущий бронхит, обострение на фоне ОРВИ.
Лечение (согласно Протоколу МЗ Украины № 18 от 13.01.2005 г.):
— Поскольку у ребенка 5 лет бронхит имел рецидивирующий характер, предполагалось назофарингеальное носительство пневмококка, поэтому в данном случае был выбран защищенный амоксициллин в пероральной форме — суспензия Амоксиклав® в суточной дозе 40 мг/кг за 3 приема каждые 8 часов во время еды в течение 10 дней.
— С учетом наличия интоксикации и малопродуктивного кашля для лучшего разжижения мокроты и ее эвакуации, а также для лизиса биопленок данному ребенку показан муколитический препарат АЦЦ в растворе.
— При повышении температуры тела более 38,0 °C рекомендован нурофен.
— Оральная регидратация.
На фоне проведенной терапии состояние ребенка быстро улучшилось. Мальчик выписан из стационара на 5-е сутки.
При выписке рекомендовано:
1. Продолжить прием суспензии Амоксиклав® в прежней дозе до 10 дней.
2. С целью профилактики обострений принимать Бронхо-Мунал® П по 1 капсуле утром натощак 10 дней, затем после месяца перерыва продолжить прием препарата по 10 дней с 20-дневными перерывами еще в течение 2 месяцев. В соответствии с действующим Протоколом МЗ Украины № 18 от 13.01.2005 г. в лечении детей с рецидивирующим бронхитом рекомендуется использовать иммуноактивные средства, одним из которых является бактериальный лизат Бронхо-Мунал® — иммуномодулятор, обладающий высокой эффективностью, подтвержденной внушительной доказательной базой.
В заключение необходимо еще раз подчеркнуть, что определяющими для благоприятного течения и исхода острых бронхитов и пневмоний у детей являются ранняя диагностика заболевания, своевременно назначенная и оптимально выбранная стартовая антимикробная терапия, правильная оценка ее эффективности и проведенная вовремя ротация препаратов при ее безуспешности.
1. Абатуров А.Е. Рациональная антибиотикотерапия в педиатрии / А.Е. Абатуров, С.П. Кривопустов // Здоров’я України. — 2010. — Тематичний номер, жовтень. — С. 17–18.
2. Антипкин Ю.Г. Принципы диагностики и лечения негоспитальных пневмоний у детей / Ю.Г. Антипкин, В.Ф. Лапшин, Т.Р. Уманец // Здоров’я України. — 2008. — № 24/2. — С. 11–13.
3. Геппе Н.А. Внебольничные пневмонии. Диагностика и лечение / Н.А. Геппе, М.Н. Снегоцкая, Е.М. Евдокимов // Практика педиатра. — 2005. — № 10, октябрь.
4. Зубков М.Н. Внебольничные пневмонии: этиологическая диагностика и антимикробная терапия / М.Н. Зубков // РМЖ. — 2004. — № 5. — 290. — Электронный ресурс: режим доступа: http://www.rmj.ru/articles_417.htm
5. SmPC AZITHRO SANDOZ®
6. SmPC AMOKSIKLAV®
7. Короид Н.В. Внебольничные пневмонии у детей: диагностика и лечение / Н.В. Короид, А.Л. Заплатников, Г.А. Мингалимова и др. // РМЖ. — 2011. — № 22. — С. 1365–1369.
8. Левенець С.С. Пневмонія у дітей: настанови, реалії, можливості / С.С. Левенець, С.О. Ренчковська, Н.О. Пранік // Актуальні питання педіатрії, акушерства та гінекології. — 2014. — № 2. — С. 30–31.
9. Лечение внебольничных пневмоний у детей старше 3 месяцев. Рекомендации Общества педиатрических инфекций и Общества инфекционистов Америки // Болезни и антибиотики. — 2011. — № 02(05). — Электронный ресурс: режим доступа: http://www.mif.ua.com/archive/article/24910
10. Майданник В.Г. Современные критерии оценки эффективности использования цефодокса у детей с затяжными бронхитами и нетяжелым течением пневмоний / В.Г. Майданник, И.О. Митюряева, И.О. Борзенко и др. // Международный журнал педиатрии, акушерства и гинекологии. — 2014. — Т. 6, № 3. — С. 19–26.
11. Малахов А.Б., Дронов И.А., Волков И.К., Геппе Н.А. Оптимальный выбор терапии внебольничной пневмонии у детей / А.Б. Малахов, И.А. Дронов, И.К. Волков, Н.А. Геппе и др. // Лечащий врач. — 2011. — № 1. — Электронный ресурс: режим доступа: http://www.lvrach.ru/2011/01/15435103/
12. Малюжинская Н.В. Лечение внебольничной пневмонии у детей старше 5 лет на амбулаторном этапе / Н.В. Малюжинская, О.В. Полякова // Лекарственный вестник. — 2014. — Т. 8, № 1(53). — С. 39–42.
13. Пневмония. Информационный бюллетень № 331, ноябрь 2013 г. — Электронный ресурс: режим доступа: who.int/mediacentre/factsheets/fs331/ru/
14. Про затвердження протоколів надання медичної допомоги дітям за спеціальністю «дитяча пульмонологія». Наказ МОЗ України № 18 від 13.01.2005.
15. Середа Е.В. Место азитромицина в педиатрической практике / Е.В. Середа, Л.К. Катосова // Лечащий врач. — 2009. — № 8. — С. 36–38.
16. Середа Е.В. Применение новой лекарственной формы амоксициллина/клавуланата при болезнях органов дыхания у детей / Е.В. Середа, Л.К. Катосова // Российский педиатрический журнал. — 2009. — № 4. — С. 55–60.
17. Страчунский Л.С., Веселов А.В. Спирамицин: место в современной химиотерапии (классика и современность) // Клиническая микробиология и антимикробная химиотерапия. — 2005. — Т. 7, № 3. — С. 1–12.
18. Таточенко В.К. Значение лекарственной устойчивости микроорганизмов в педиатрической практике / В.К. Таточенко, М.Д. Бакрадзе // Практика педиатра. — 2009, декабрь. — С. 5–11.
19. Хайтович Н.В. Рациональная антибиотикотерапия респираторной инфекции у детей / Н.В. Хайтович // Здоровье ребенка. — 2013. — № 8(51). — С. 139–146.
20. Чернышева О.Е. Острые бронхиты у детей / О.Е. Чернышева, Л.Л. Поповиченко // Здоровье ребенка. — 2009. — № 6(21).
21. Чернишова Л.І. Назофарингеальне носійство Streptococcus pneumoniae у вихованців будинків дитини: серотиповий репертуар та чутливість до антимікробних препаратів / Л.І. Чернишова, А.М. Гільфанова // Здоровье ребенка. — 2014. — № 6(57). — С. 9–14.
22. Юлиш Е.И. Возможности «новых» макролидов в лечении бактериальных заболеваний органов дыхания / Е.И. Юлиш // Здоровье ребенка. — 2013. — № 7(50). — С. 109–114.
23. Bennett N.J. Pediatric pneumonia // Ed. by Russell W. Steele. — Электронный ресурс: http://emedicine.medscape.com/article/967822–overview#a0156
24. British Thoracic Society Guidelines for the Management of Community Acquired Pneumonia in Childhood, 2002.
25. Don M. Community-acquired pneumonia in children: what’s old What’s new / M. Don, M. Canciani, M. Korppi // Acta Paediatr. — 2010. — № 99(11). — Р. 1602–1608.
26. Nelson F. Textbook of Pediatrics. Philadelphia — London — Toronto — Montreal — Sydney — Tokyo, 1992. — 14th ed.

/69/69.jpg)
/70/70.jpg)