Газета «Новости медицины и фармации» 10 (543) 2015
Вернуться к номеру
Сучасні погляди на онтогенез респіраторної системи.
Авторы: Сенаторова Г.С., Логвінова О.Л., Лапшин В.Ф., Муратов Г.Р., Башкірова Н.В.
Харківський національний медичний університет
Рубрики: Семейная медицина/Терапия, Педиатрия/Неонатология, Пульмонология
Разделы: Клинические исследования, Справочник специалиста
Версия для печати
Статья опубликована на с. 30-32 (Укр.)
1. Стадії онтогенезу легень
Органогенез респіраторного тракту — складний процес диференціювання зародкових листків і мезодерми, який контролюється генетично запрограмованою координованою передачею сигналів. На початкових стадіях розвитку клітини ембріона неспецифічні й здатні створювати декілька тканин. З приєднанням комітування починається гальмування можливих шляхів розвитку клітин із тенденцією до їх спеціалізації. У результаті блокування й деблокування ізольованих генів виникають морфологічні та хімічні відмінності між клітинами організму, що мають однаковий геном. Організація та розміщення клітин забезпечують правильну будову легенів (Афанасьєва Ю.І., Кузнецов С.Л., Юріна Н.О., 2006; Гречаніна О.Я., Богатирьова Р.В., Волосовець О.П., 2007). В ембріогенезі на основі анатомічних і гістологічних ознак виділено п’ять стадій (рис. 1) (Афанасьєва Ю.І., Кузнецов С.Л., Юріна Н.О., 2006).
Ранні (ембріональна і псевдогландулярна) стадії формування дихальних шляхів змінюються каналікулярною, саккулярною та альвеолярною стадіями, що характеризуються зменшенням мезенхіми й васкуляризації для формування альвеолярно-капілярної мембрани.
Народження доношеної дитини не свідчить про закінчення розвитку легенів. Існує постійний складний процес їх росту, що дозволяє збільшити розмір дихальних шляхів і площу альвеол (Wigglesworth J.S., 2007). У доношеного новонародженого близько 50 млн альвеол з потенціалом до збільшення їх числа до 300 млн і площі з 3 до 70 м2. Відомо більше ніж 40 різних типів клітин у легені з різними функціями. Яким чином вони контактують, поки досконально невідомо.
Ембріональна стадія
Ембріональна стадія розвитку легенів триває 3–7 тижнів і починається на 21-шу добу з випирання нижнього відділу перед–ньої кишки під глотковою кишенею з утворенням гортанотрахеальної борозни (рис. 2) (Афанасьєва Ю.І., Кузнецов С.Л., Юріна Н.О., 2006).
Гортанотрахеальна борозна виділяється від кишки й перетворюється на гор–танотрахеальну трубку на 28-му добу (Афанасьєва Ю.І., Кузнецов С.Л., Юріна Н.О., 2006; Wigglesworth J.S., 2007). Гортань утворюється з краніального відділу, трахея — з каудального. З 33 діб каудальний кінець труби розширюється й ділиться на правий та лівий зачатки — початок головних бронхів і легень. Лівий зачаток спрямований латерально й завжди менший за правий, правий — каудально. Асиметрія проявляється і в розподілі на частки.
Перший дихальний рух може бути зареєстрований наприкінці ембріонального періоду. Однак ці дихальні рухи парадоксальні тим, що коли діафрагма скорочується, грудна клітка втягується, і навпаки. Даний факт цікавий для вивчення ролі в координації руху грудної клітки й діафрагми нарівні з рестрикцією легень, у виникненні дихання типу «гойдалки» у глибоко недоношених новонароджених із респіраторним дистрес-синдромом.
Зачаток легенів забезпечується кров’ю через парні сегментарні артерії, що входять до дорсальної частини аорти. Поступово легеневі капіляри втрачають зв’язок із сегментарними артеріями, і їх забезпечення кров’ю відбувається через гілки легеневої артерії (ЛА), що розміщені за поділом дихальної трубки (рис. 3). Анастомози між системою легеневої та бронхіальної артерій зберігаються до народження й функціонують у недоношених на перших тижнях життя, що обумовлює ризик шунтування крові.
Псевдогландулярна стадія
Псевдогландулярна стадія триває з 7-го по 16-й тиждень із формуванням повітроносних шляхів до термінальних бронхіол (близько 25 тис.). Хрящі, гладка мускулатура утворюються з мезенхіми (рис. 4).
Хрящова тканина розвивається навколо дихальних шляхів і гладкої мускулатури. З 8-го по 9-й тиждень гестації формується дистальна циркуляція, що з’єднує проксимальну легеневу артерію з венами опору (Wigglesworth J.S., 2007). На даний час визначено, що периферичні частини легені взаємопов’язані тільки з легеневою артерією. Стан бронхіальних також важливий для легеневої диференціації.
Каналікулярна стадія
Каналікулярна стадія (16–24-й тижні) характеризується утворенням каналів у мезенхімі легені (рис. 5). На 16-му тижні закінчується формування бронхів 20–24-го порядку (Wigglesworth J.S., 2007). Розвиваються термінальні бронхіоли й ацинуси — газообмінні структури легень. Кожен ацинус складається з 3–4 респіраторних бронхіол, альвеолярної протоки, альвеолярних сакул альвеол. Спочатку майбутні ацинуси вистелені кубічним епітелієм. На 20-му тижні починають з’являтися гранулярні пневмоцити — альвеолоцити1.
На 19–20-му тижні виникає контакт мембран альвеол і капілярів, що є основою постнатального життя (Wigglesworth J.S., 2007). До 24-го тижня альвеолярно-капілярний бар’єр недостатній. Альвеолоцити I типу покривають 95 % поверхні альвеол (рис. 5). Залишок площі займають аль–веолоцити II типу, з розвиненим комплексом Гольджі, мітохондріями2. Основна функція альвеолоцитів II порядку — продукція сурфактанту, що складається з фосфоліпідів (головним чином дипальмітіолфосфатидилхоліну), утворюючи тонку плівку та зменшуючи поверхневий натяг альвеол. Сурфактант з’являється у плодів масою 500–1000 г.
Дефіцит сурфактанту тим більший, чим менший гестаційний термін новонародженого, і є причиною респіраторного дистрес-синдрому новонароджених, який потребує збільшення тиску й об’єму повітряної суміші в дихальних шляхах, що призводить до формування бронхолегеневої дисплазії.
Сакулярна стадія
Сакулярна стадія починається з 24-го тижня й характеризується потенціалом до зростання числа альвеол і площі респіраторної поверхні легенів. Здорові доношені новонароджені народжуються в альвеолярній стадії. У недоношених дітей сакулярна фаза проходить позаутробно, що порушує нормальний хід онтогенезу. Гальмування росту альвеол, ймовірно, призводить до затримки онтогенезу в сакулярній стадії, відсутність адекватної васкуляризації й чітких перегородок між ацинусами призводить до тривалого збереження інтерстиціальних порушень.
Сакулярна стадія триває від 24-го до 36-го тижнів гестації й характеризується диференціюванням і дозріванням легеневих структур, формуванням на кінцях альвеолярних ходів мішечків — тонкостінних однокамерних альвеол (рис. 6) (Афанасьєва Ю.І., Кузнецов С.Л., Юріна Н.О., 2006).
Наприкінці 27-го тижня утворюється близько 25 тис. термінальних бронхіол. Протягом сакулярної стадії поступово зменшується інтерстицій, формуються термінальні гребені.
Термінальні гребені є джерелом альвеол і морфологічно являють собою дрібні виступи вздовж основної перегородки, які розподіляються на більш дрібні альвеоли, що розмежовані вторинною перегородкою. Зростання альвеол тісно пов’язане з еластином і протеогліканами інтерстицію, які є субстратом для альвеолярної тканини, що індукується активацією сигнальних рецепторів і ростових факторів.
Саме гальмування потенціалу термінальних гребенів у глибоко недоношених дітей призводить до пригнічення легеневого онтогенезу й обумовлює клініку нової форми БЛД. Тому більшість досліджень причин формування нової БЛД і розробки лікування даного захворювання спрямовані саме на сакулярну стадію.
У сакулярну стадію відбувається постійне диференціювання I і II типів альвеолярних клітин — дистального дихального епітелію. Існує ряд доказів, що клітини Клара і II тип альвеолярних клітин є первинними клітинами — попередниками легеневого епітелію після пошкодження3.
Альвеолярна стадія
Альвеолярна стадія зазвичай починається після народження і триває до 3 років (згідно з деякими джерелами — до 8 років) (Cirulli V., Yebra M., 2008). У перші шість місяців кількість альвеол збільшується суттєво, а до 1,5 року утворюються вторинні перегородки. Основним завданням онтогенезу в альвеолярну стадію є збільшення кількості, поглиблення й розширення альвеол, зміцнення стінки капілярів. Зростання дихальних шляхів відбувається пропорційно росту альвеолярно-капілярної тканини, через утворення численних гребенів у мішечках, які збільшуються за рахунок їх внутрішньої поверхні (рис. 7).
З 26-го тижня капілярна мережа легенів тісно змикається з альвеолами, що забезпечує здатність до ефективного газообміну. Ультраструктурні дослідження показують, що альвеоли оточені еластичними волокнами, що утворюють інтерстиціальні перегородки між капілярними мережами.
Розвиток артерій супроводжується прогресивним збільшенням їх просвіту, який спочатку не перевищує кілька мікрометрів. Просвіт часточкових артерій збільшується з 10-го тижня, а термінальних і респіраторних артеріол — тільки з 36–38-го тижнів.
2. Молекулярні основи онтогенезу легень
До сьогодні тривають пошуки молекулярних мішеней активації росту альвеолярних гребенів для поліпшення виживаності та якості життя дітей із новою бронхолегеневою дисплазією. Закладання, розгалуження й ріст легенів відбуваються під впливом мезенхіми. Це показано на експериментах, у яких трахеальний епітелій починає розгалужуватися, якщо його вирощують на шарі мезенхіми (Santos I.S., Matijasevich A., Silveira M.F., 2008). Знайдено скупчення рецепторів білка внутрішнього сигнального шляху (Wnt/β-catenin-2) у тому місці передньої кишки, де надалі формуються легені. Активація Wnt/β-catenin-2 перепрограмує розвиток стравоходу на легені через транскрипційні сигнали, активуючи Nkx2.1 (NK2 homeobox) для стимуляції ростових факторів (Chen H., 2005). Таким чином, Nkx2.1 функціонує як майстер-ген, що індукує й підтримує диференціацію епітеліальних клітинних ліній. Ірландські дослідники в 2010 році через 3D-томографію легенів мишей виявили зв’язок експресії транскрипційного фактора диференціації (Foxa2) (HNF3β) на епітеліальних клітинах і фактора росту фібробластів-10, який впливає на поділ бронхіальних зачатків (Cirulli V., Yebra M., 2010). Для регуляції онтогенезу легенів важливий рівень Achaete-Scute гомолог-1 (Ascl1), пронейрального фактора транскрипції «спіраль — петля — спіраль», що важливий для розвитку нейроендокринних клітин (PNECs), хоча вони являють собою лише невелику частину інтерстицію. Важливий не тільки якісний склад транскрипційних сигналів, а й час їх активації. Клітини Клара, помічені на 9,5 день ембріонального періоду, формували альвеоли й дихальні шляхи, тоді як на 11,5 добу — тільки дихальні шляхи (Santos I.S., Matijasevich A., Silveira M.F., 2008).
Доведено, що, згідно з загальним принципом формування патерна, клітини, розташовані вздовж градієнта сигналу, поділяються відповідно до фенотипу, причому скупчення специфічних клітин у певній зоні обумовлює активацію зростання епітелію або мезенхіми. Більше того, зростання дистального і проксимального відділів визначається специфічними клітинами й сигналами. Наприклад, клітини Клара загалом відповідальні за повітроносний сегмент легенів, а макрофаги розташовані переважно в дистальній частині і забезпечують формування респіраторного відділу. Визначено, що макрофаги є індукторами зростання мезенхіми й епітелію на периферії. Уведення макрофагального колонієстимулюючого фактора 1 (MCSF-1) новонародженим мишам сприяло збільшенню кількості макрофагів і багатого цистеїном протеїну, що знайдений у зоні запалення (Fizz-1) (Retnla), інсуліноподібного фактора росту 1 (IGF-1). Fizz-1 є важливим медіатором альвеоло-, ангіогенезу, а також активатором виробництва сурфактанту. IGF-1 посилює альвеоляризацію у присутності ретиноєвої кислоти й дексаметазону. Інтерстиціальні фібробласти виробляють позаклітинний матеріал в інтрадуктальний і інтрасакулярний простори (Groenman F., 2007).
У сакулярну стадію секреторний білок клітин Клара і нуклеарний транскрипційний фактор (HFH-4) впливають на клітини, локалізовані в проксимальній частині легенів, що доводить їх роль як дозозалежного фактора сигналізації зростання трахеї й бронхів. Рецептори тиреоїдного транскрипційного фактора 1, судинного ендотеліального фактора росту (VEGF) і трансформуючого фактора росту (TGF) 1β виявляються в дистальній частині легені й зумовлюють зростання альвеол (Galambos C., Levy H., 2010; Minoo P., 2010).
Таким чином, будь-які зміни сигналізації можуть порушувати структурування осі легенів. Доведено роль генних транс–крипційних факторів Нomeоbox у проксимально-дистальній орієнтації легенів. Нomeоbox-4 і Нomeоbox-3 відповідає за проксимальне й дистальне розгалуження, а Нomeоbox-2 і Нomeоbox-5 — тільки за дистальні ділянки. Нomeоbox-5 індукується ретиноєвою кислотою, у той час як негативно регулюється TGF-1β, VEGF і епідермальний фактор росту (EGF). Фактор росту фібробластів (FGF) регулює альвеоляризацію, стимулює синтез еластину, гладком’язових волокон міо–фібробластами й паренхіми. TGF-β, будучи регулятором позаклітинної матриці, активації відкладення колагену, фібронектину й протеогліканів, інгібує проліферацію епітеліальних клітин, які локалізуються на кордоні епітеліальних і мезенхімальних клітин, особливо навколо бронхоальвеолярних проток. При гіперпродукції TGF-β порушується регуляція TGF-β/Smad, що сприяє затримці альвеолярного зростання (Hajduk P., 2010; Leppäranta O., 2010). Крім цього, TGF-β через активацію N-Myc (мієлоцитоматозні вірусні онкогени) відіграють роль підтримки клітин легенів у недиференційованому стані і пригнічують розгалуження дихальних шляхів.
Визначена медіаторна роль цинкового пальчикового протеїну (Gli) 2 і 3 в активації трансдукційних сигналів на фактори росту (TGF-β1 і FGF-7, FGF-10)(Morrisey E.E., 2009; Rutter M., 2010). Активовані фактори росту є тригерами –правильного поділу бронхів через Netrin-1 і Netrin-4 (протеїн нетрин) рецептори епітеліальних клітин і протеїн Semaphorin-3a мезенхіми, який відповідає за формування ацинусів. Блокада рецепторів до TGF-β1, FGF-7, FGF-10 порушує взаємодію епітелію й мезенхіми, поділ бронхів і формування ацинусів, зменшує періальвеолярну мезенхіму, що відповідає за газообмін (Morrisey E.E., 2009; Rutter M., 2010).
VEGF відіграє важливу роль у формуванні адекватно функціонуючої перфузії в ході ембріогенезу й у ранньому постнатальному періоді. Індуктором експресії VEGF є гіпоксія. Учені виявили зв’язок активації гіпоксіяіндукованого фактора з активацією VEGF в ембріона (Rutter M., 2010). Ймовірно, помірна гіпоксія активує зростання легеневих судин у недоношених дітей. Проте до цього часу не виявлено залежності ступеня гіпоксії від рівня VEGF, впливу ростового фактора на правильність ангіогенезу, що важливо для тактики ведення дітей із новою формою БЛД. Відомий вплив факторів транскрипції (TF), мікро-РНК-221 та проангіогенних мікро-РНК-130а на розвиток судин бронхів у легенях плода миші. Неправильна експресія VEGF викликає аномалії морфогенезу судин легенів, дистальних канальців і ацинарної мезенхіми (Кетлинский С.А., 2008; Harkaitz B., 2008).
Інтерстиційний простір — матриця, що відіграє важливу роль для росту й диференціювання легенів. Характерною особ–ливістю БЛД є можливість відновлення міжклітинних взаємин і репарації легеневої тканини в альвеолярній стадії онто–генезу. Разом із тим у частини дітей зберігається зменшений респіраторний простір, у частини — профіброзуюча направленість, а в деяких пацієнтів загострення захворювання перебігає з перевагою інтерстиційного компонента й обструкції бронхіол.
Нарівні з тим дослідження стану інтерстицію, наведені в літературі, здебільшого проведені на тваринах. Поки недостатньо даних для з’ясування основних механізмів гальмування онтогенезу легенів, не знайдений ланцюг регуляторних сигналів і цитокінів, відповідальних за зростання альвеол і судин у дітей із БЛД. Навіть у новій формі має місце фіброзування легеневої тканини, ймовірною причиною якого є запалення. Таким чином, дослідження функції та потенціалу інтерстицію легень досить актуально для з’ясування причин позаутробного гальмування онтогенезу легень із метою запобігання зниженню життєвого об’єму легенів і розвитку дифузійно-перфузійних порушень при новій формі бронхолегеневої дисплазії.
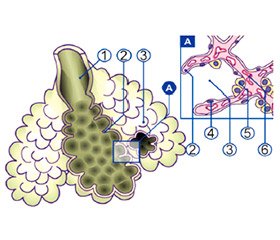
(1) — Альвеолоцити I типу — плоскі, або респіраторні, покривають більшу частину (95–97 %) поверхні альвеол, є компонентом аеро–гематичного бар’єру, через них здійснюється газообмін. Мають неправильну форму і стоншену цитоплазму (менше 0,2 мкм), яка містить слаборозвинені органели й велику кількість піноцитозних бульбашок. Пов’язані між собою і з альвеолоцитами II типу щільними сполуками. Ці клітини дуже чутливі до токсичних речовин.
(2) — Альвеолоцити II типу — великі, або гранулярні. Кількість їх приблизно дорівнює кількості альвеолоцитів I типу, серед альвеолоцитів І типу вони лежать поодинці або дрібними групами, покривають 2–5 % поверхні альвеол. Мають округлу або кубічну форму, виступають у просвіт альвеол, на поверхні мають мікроворсинки. У цитоплазмі альвеолоцитів II типу багато мітохондрій, добре розвинений апарат Гольджі та інші органели, серед яких найбільш характерні осмофільні тільця, оточені мембраною. Останні складаються з електронно-щільної шаруватої речовини, що включає фосфоліпіди, білкові та вуглеводні компоненти. Пластинчасті тільця, подібно секреторним гранулам, виділяються з альвеолоцитів II типу й утворюють на поверхні альвеолярного епітелію сурфактантну плівку завтовшки 0,05 мкм. Крім вироблення сурфактанту альвеолоцити II типу виконують й інші функції: регуляція транспорту води та іонів через альвеолярний епітелій; синтез і секреція інтерферону й лізоциму; участь в обміні ксенобіотиків; є камбіальними елементами альвеолярного епітелію; знешкодження окиснювачів.
Альвеолоцити III типу — щіткові. Відрізняються наявністю на апікальній поверхні коротких мікроворсинок, а в цитоплазмі — численних везикул і пучків мікрофібрил. Передбачається, що альвеолоцити III типу здійснюють всмоктування рідини й концентрують сурфактант. Також висловлюється припущення про їх ней–росекреторну функцію, хеморецепцію.
(3) — Клітини Клара були описані в 1937 році Максом Кларом (1899–1966), на честь якого вони й були названі. Макс Клар був нацистським лікарем, який використав останки жертв Третього рейху для своїх досліджень у Лейпцигу, у тому числі для роботи, що призвела до відкриття клітин Клара. Клітини Клара — це опуклі клітини з короткими мікроворсинками, знайдені в бронхіолах легень, у війчастому епітелії. Клітини Клара можуть виділяти глікозаміноглікани, щоб захищати епітелій бронхіол. Якщо кількість келихоподібних клітин зменшується, кількість клітин Клара зростає. Головна функція клітин Клара — захист епітелію бронхіол. Захист здійснюється через виділення деяких речовин, зокрема секреторного білка клітин Клара (CCSP — Clara Cell Secretory Protein) і речовини, схожої на один із компонентів сурфактанту легень. Клітини Клара також відповідальні за зниження токсичності шкідливих речовин, що проникають у легені при вдиху. Відбувається це за допомогою цитохрому Р450. Клітини Клара також виступають у ролі стовбурових клітин, диференціюючись у війчасті клітини епітелію, щоб відновлювати епітелій бронхіол.


/30-1.jpg)
/30-2.jpg)
/31.jpg)