Газета «Новости медицины и фармации» 11 (544) 2015
Вернуться к номеру
Сурфактант (компоненти, синтез, функції)
Авторы: Сенаторова Г.С., Логвінова О.Л., Лапшин В.Ф., Муратов Г.Р., Башкірова Н.В.
Харківський національний медичний університет
Рубрики: Семейная медицина/Терапия, Педиатрия/Неонатология, Пульмонология
Разделы: Медицинское образование
Версия для печати
Статья опубликована на с. 31 (Укр.)
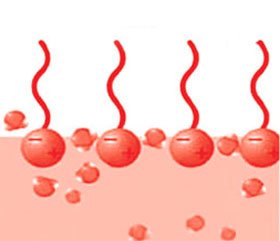
Сурфактант — ліпідно-білковий комплекс, що покриває плівкою альвеоли й має властивість знижувати їх поверхневий натяг. Сурфактант продукується альвео–лоцитами II типу. Основу сурфактанту становлять фосфоліпіди (переважно дипальмітоїлфосфатидилхолін). Будова сурфактанту наведена на рис. 1.
Компоненти сурфактанту:
— власне сурфактант — поверхнево-активна плівка у вигляді одношарової мономолекулярної мембрани, розташована в альвеолах, альвеолярних ходах і респіраторних бронхіолах 1–3-го порядку;
— гіпофаза (підстильний гідрофільний шар) — рідке середовище, розташоване під зрілим сурфактантом, заповнює нерівності власне сурфактанту й містить резервний зрілий сурфактант; осмофільні тільця і їх фрагменти (продукти секреції альвеолоцитів II типу); макрофаги.
— власне сурфактант — поверхнево-активна плівка у вигляді одношарової мономолекулярної мембрани, розташована в альвеолах, альвеолярних ходах і респіраторних бронхіолах 1–3-го порядку;
— гіпофаза (підстильний гідрофільний шар) — рідке середовище, розташоване під зрілим сурфактантом, заповнює нерівності власне сурфактанту й містить резервний зрілий сурфактант; осмофільні тільця і їх фрагменти (продукти секреції альвеолоцитів II типу); макрофаги.
1. Синтез сурфактанту
Існують два шляхи синтезу основного фосфоліпідного компонента сурфактанту — фосфатидилхоліну:
— метилювання фосфатидилетанол–аміну за допомогою метилтрансферази;
— синтезування з цитидиндифосфатхоліну в присутності фосфохолінтрансферази.
— метилювання фосфатидилетанол–аміну за допомогою метилтрансферази;
— синтезування з цитидиндифосфатхоліну в присутності фосфохолінтрансферази.
Установлено, що до 35-го тижня внутрішньоутробного розвитку синтез сурфактанту в основному здійснюється через метилювання етаноламіну, а пізніше — за допомогою фосфатидилхолінтрансферази. Перший шлях синтезу сурфактанту легко виснажується під впливом гіпоксії, ацидозу, гіпотермії. Тому вважають, що повністю система сурфактанту дозріває на 35–36-му тижнях внутрішньоутробного розвитку (Lucas M.G., 2008). У дитини, народженої до цього терміну, наявні запаси сурфактанту забезпечують початок дихання й формування функціонального залишкового об’єму (ФЗО) легень, але через його незрілість, відставання синтезу сурфактанту від темпів його розпаду виникає брак цієї речовини. Дефіцит сурфактанту призводить до спадання альвеол на видиху, різкого зростання роботи дихальних м’язів, оскільки через нестачу функціонального залишкового об’єму легень, підвищеної їх жорсткості зусилля, необхідні для кожного наступного роздування легень, повинні бути такими ж, як і для першого подиху. Крім того, унаслідок спадання альвеол безперервного газообміну в легенях не відбувається, що провокує розвиток гіпоксемії й гіперкапнії. Поряд із фосфатидилхоліном для нормального функціонування сурфактанту мають значення й інші компоненти, особливо фосфатидилгліцерин і фосфатидилінозитол. Наприклад, у недоношених дефіцит фосфатидилгліцерину є фактором ризику смерті від респіраторного дистрес-синдрому. При низькому рівні лецитину в навколоплідних водах, але нормальному вмісті фосфатидилгліцерину респіраторний дистрес-синдром не розвивається (Николаев А.Я., 2007; Афанасьева Ю.И., Кузнецова С.Л., Юрина Н.А., 2006).
2. Функції сурфактанту
Сурфактант:
— захищає альвеолярний епітелій від пошкоджень;
— сприяє мукоциліарному кліренсу;
— має бактерицидну активність проти грампозитивних мікробів і стимулює макрофагальну реакцію в легенях;
— стабілізує термінальний повітряно–вмісний простір1;
— бере участь у регуляції мікроциркуляції в легенях і проникності стінок альвеол, перешкоджає розвитку набряку легенів.
— захищає альвеолярний епітелій від пошкоджень;
— сприяє мукоциліарному кліренсу;
— має бактерицидну активність проти грампозитивних мікробів і стимулює макрофагальну реакцію в легенях;
— стабілізує термінальний повітряно–вмісний простір1;
— бере участь у регуляції мікроциркуляції в легенях і проникності стінок альвеол, перешкоджає розвитку набряку легенів.
Важливу роль відіграють білки сурфактанту2. Найбільш важливим серед цих білків є сурфактантний протеїн В, бо його спадковий або вроджений дефіцит є летальним для людини. Успадковується дефіцит SpB за aвтосомно-рецесивним типом і проявляється в доношених дітей клінічною картиною типового респіраторного дистрес-синдрому недоношених. Замісна терапія сурфактантом при спадковому дефіциті справляє лише транзиторний ефект, радикальне лікування — трансплантація легенів.
3. Утворення сурфактанту
Сурфактант починає вироблятися у плода з 20–24-го тижня внутрішньоутробного розвитку альвеолярними клітинами II типу. Він накопичується в них як осмофільні гранули, що мігрують на поверхню альвеол, де утворює тонку плівку — гіпофазу.
У першу чергу сурфактант утворюється у верхніх частках легень, а потім — у нижніх. На 36-му тижні гестації кількість сурфактанту достатня для забезпечення дихання. Інтенсивний викид сурфактанту відбувається в момент пологів, що сприяє процесу первинного розправлення легень. Період напіврозпаду сурфактанту — 10–20 годин (Lucas M.G., 2008).
4. Інгібітори та інактиватори синтезу сурфактанту
— Холодова травма, у тому числі при використанні при штучній вентиляції –легень непідігрітої киснево-повітряної суміші;
— ацидоз;
— гіпоксемія або гіпероксія;
— гіповолемія;
— поліцитемія;
— баротравма й волюмотравма легенів;
— плазмові протеїни;
— інфекції.
— ацидоз;
— гіпоксемія або гіпероксія;
— гіповолемія;
— поліцитемія;
— баротравма й волюмотравма легенів;
— плазмові протеїни;
— інфекції.
Перераховані фактори пошкоджують альвеоли, активують синтез прозапальних цитокінів, систему комплементу й хемо–кінів (анафілотоксинів, брадикініну та ін.), що призводить до підвищеної проникності ендотелію й набряку альвеол.
1 Сурфактант утворює поверхнево-активну плівку та змінює поверхневий натяг залежно від радіуса альвеол. При збільшенні радіуса альвеол на вдиху поверхневий натяг зростає до 40–50 • 10–3 Н/м, істотно підвищуючи еластичний опір диханню. При малому діаметрі альвеол натяг знижується до 1–5 • 10–3 Н/м, що забезпечує стабільність альвеол на видиху.
2 Білки сурфактанту A (Sp-A) і D (Sp-D) гідрофільні, вони залучаються до захисних механізмів організму дитини (не містяться в сурфактанті легенів тварин), а протеїни В (Sp-B) і С (Sp-C) — гідрофобні, вони знижують поверхневий натяг альвеол за рахунок стимуляції абсорбції фосфоліпідів на поверхні аерогематичного бар’єра і сприяють рівномірному розподілу сурфактанту на поверхні альвеол. Sp-A кодований двома тісно зчепленими високополіморфними генами на 10-й хромосомі в ділянці q22-q23. Чотири алелі Sp-A1 і п’ять алелей Sp-A2 зустрічаються з середньою частотою (фінська популяція), тоді як інші 30 алелей виявляються рідше. Sp-B сприяє поверхневій абсорбції ліпідів та посилює здатність фосфоліпідів знижувати поверхневий натяг в альвеолах. Sp-B ген локалізований у хромосомі 2 p12-p11.2 і складається з 79 амінокислот (2 % маси сурфактанту). Дефіцит SP-B найбільш поширений та успадковується за автосомно-рецесивним типом за умови мутації обох алелей. Найбільш поширена мутація включає 2 базові вставки в кодон 121 (121ins2), у результаті чого виникає мутація зі зсувом рамки зчитування і передчасно стоп-кодон. Sp-С ген локалізований на короткому плечі 8-ї хромосоми. Sp-D ген локалізується на 10-й хромосомі в районі q22-q23 поруч із генами сурфактанту Sp-A. SpA з’являється в навколоплідній рідині людини на 19-му тижні гестації, a SpB — на –31-й; надалі рівень їх безупинно наростає (Афа–насьева Ю.И., 2006).


/32-1.jpg)