Журнал «Здоровье ребенка» Том 14, №6, 2019
Вернуться к номеру
Особенности течения болезни Кавасаки у детей раннего возраста
Авторы: Коренюк Е.С.(1), Крамаренко Н.Н.(1), Иванусь С.Г.(2)
(1) — ГУ «Днепропетровская медицинская академия МЗ Украины», г. Днепр, Украина
(2) — КУ «ДДГКБ № 2 ДГС», г. Днепр, Украина
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
Актуальність. Своєчасній діагностиці синдрому Кавасакі перешкоджає велика кількість клінічних масок хвороби, а також недостатня настороженість лікарів щодо цього захворювання у дітей із тривалою лихоманкою. Мета: підвищити ефективність діагностики хвороби Кавасакі на підставі ретроспективного аналізу клінічного перебігу та результатів захворювання у дітей, які перебували під нашим спостереженням. Матеріали та методи. Проведено аналіз історій хвороби 7 дітей віком від 7 місяців до 6 років із хворобою Кавасакі, які перебували на лікуванні в кардіопульмонологічному відділенні МДКЛ № 2 м. Дніпра. Діагноз хвороби Кавасакі був верифікований на підставі діагностичних критеріїв згідно з чинним клінічним протоколом. До всіх хворих були застосовані рутинні методи дослідження, ЕхоКГ (Д). Результати. Під час дослідження відзначено пізню діагностику хвороби Кавасакі (на етапі формування аневризм коронарних артерій) в 43 % спостережуваних випадків. Складність діагностики синдрому Кавасакі була обумовлена відсутністю повного комплексу типових ознак. Неповний варіант відзначався переважно в дітей перших трьох років життя і включав такі симптоми, як кон’юнктивіт, плямисто-папульозне висипання й ураження ротової порожнини в різноманітних комбінаціях. ЕхоКГ-дослідження виявило аневризми коронарних артерій у 57 % випадків, переважно у дітей раннього віку з неповним варіантом хвороби Кавасакі. На тлі проведеної терапії (внутрішньовенний імуноглобулін та аспірин) ми спостерігали значний регрес аневризм коронарних артерій у всіх пацієнтів. Висновки. У дітей раннього віку найбільш часто спостерігається неповний варіант синдрому Кавасакі, що ускладнює його діагностику. У зв’язку з цим тривала лихоманка в поєднанні навіть з 2–3 типовими ознаками повинна бути абсолютним показанням до проведення ЕхоКГ з обов’язковою візуалізацією коронарних артерій.
Актуальность. Своевременной диагностике синдрома Кавасаки препятствует большое количество клинических масок болезни, а также недостаточная настороженность врачей в отношении этого заболевания у длительно лихорадящего ребенка. Цель: повысить эффективность диагностики болезни Кавасаки на основании ретроспективного анализа клинического течения и исходов заболевания у детей, находившихся под нашим наблюдением. Материалы и методы. Проведен анализ историй болезни 7 детей в возрасте от 7 месяцев до 6 лет с болезнью Кавасаки, находившихся на лечении в кардиопульмонологическом отделении ДГКБ № 2 г. Днепр. Диагноз болезни Кавасаки был верифицирован на основе диагностических критериев в соответствии с действующим клиническим протоколом. Всем больным были проведены рутинные методы исследования, ЭхоКГ (Д). Результаты. В ходе исследования отмечена поздняя диагностика болезни Кавасаки (на этапе формирования аневризм коронарных артерий) в 43 % наблюдаемых случаев. Сложность диагностики синдрома Кавасаки была обусловлена отсутствием полного комплекса типичных клинических признаков. Неполный вариант отмечался преимущественно у детей первых трех лет жизни и включал такие симптомы, как конъюнктивит, пятнисто-папулезная сыпь и поражение ротовой полости в различных комбинациях. ЭхоКГ-исследование выявило наличие аневризм коронарных артерий в 57 % случаев, преимущественно у детей раннего возраста с неполным вариантом болезни Кавасаки. На фоне проводимой терапии (внутривенный иммуноглобулин и аспирин) мы наблюдали значительный регресс аневризм коронарных артерий у всех пациентов. Выводы. У детей раннего возраста наиболее часто встречается неполный вариант синдрома Кавасаки, что затрудняет его диагностику. В связи с этим длительная лихорадка в сочетании даже с 2–3 типичными признаками должна быть абсолютным показанием к проведению ЭхоКГ с обязательной визуализацией коронарных артерий.
Background. A large number of clinical masks and also insufficient vigilance of doctors regarding Kawasaki syndrome in a child with long-term fever impede timely diagnosis of Kawasaki syndrome. The purpose of the study was to increase the diagnostic efficiency of Kawasaki disease based on a retrospective analysis of its clinical course and outcomes in children under our supervision. Materials and methods. Case histories were analyzed in 7 children aged from 7 months to 6 years, who were treated in the cardiopulmonary department of Children’s Clinical Hospital 2 in Dnipro. The diagnosis of Kawasaki disease was verified based on diagnostic criteria in accordance with the current clinical protocol. Routine research methods and echocardiography were performed for all patients. Results. The study revealed late diagnosis of Kawasaki disease, already at the stage of formation of coronary artery aneurysms, in 43 % of cases. The complexity of diagnosing Kawasaki syndrome was due to the lack of a full range of typical symptoms. The incomplete presentation was noted mainly in children of the first three years of life and included symptoms such as conjunctivitis, maculopapular rash, and oral lesions in various combinations. Echocardiography revealed coronary artery aneurysms in 57 % of cases, mostly in infants with incomplete presentation of Kawasaki disease. Against the background of therapy (intravenous immunoglobulin and aspirin), we observed a significant regression of coronary artery aneurysms in all patients. Conclusions. Infants most often have incomplete presentation of Kawasaki syndrome, which complicates its diagnosis. In this regard, prolonged fever in combination even with 2–3 typical signs should be an absolute indication for echocardiography with mandatory visualization of the coronary arteries.
хвороба Кавасакі; особливості перебігу; діти
болезнь Кавасаки; особенности течения; дети
Kawasaki disease; course features; children
Введение
Синдром Кавасаки редко встречается в нашей стране, но знание его проявлений и умение своевременно поставить диагноз очень важны для педиатров, так как именно это заболевание является одной из причин острых сердечно-сосудистых осложнений и внезапной смерти у детей [1].
Болезнь Кавасаки (БК) (слизистокожный лимфонодулярный синдром, МКБ-10; М30.3) — это остро протекающее системное заболевание, характеризующееся морфологически преимущественным поражением средних и мелких артерий, с развитием деструктивно-пролиферативного васкулита, а клинически — лихорадкой, изменениями слизистых оболочек, кожи, лимфатических узлов, возможным поражением коронарных и других висцеральных артерий [2–4].
Сегодня синдром Кавасаки стал ведущей причиной появления приобретенных заболеваний сердца у детей, оставив позади такое широко известное, но в последние десятилетия редкое заболевание, как острая ревматическая лихорадка. Поражение сосудов коронарного русла, характерное для синдрома Кавасаки, может сохраняться длительное время, приводя к развитию ишемической болезни сердца, в том числе к инфаркту миокарда. Согласно многочисленным исследованиям, вероятность поражения коронарных артерий напрямую зависит от срока установления правильного диагноза и начала лечения.
Ранняя диагностика синдрома Кавасаки важна именно с позиции предотвращения долгосрочных осложнений этого острого заболевания. Своевременной диагностике БК препятствует большое количество клинических масок заболевания (в первую очередь, инфекционных), наличие нетипичных форм (представляющих при этом наибольший риск поражения коронарных сосудов), а также недостаточная настороженность врачей в отношении этого заболевания в процессе курации длительно лихорадящего ребенка. Вероятно, именно низкая информированность врачебного сообщества об основных диагностических критериях заболевания является главной причиной гиподиагностики синдрома Кавасаки [2].
Эпидемиологические данные болезни имеют ряд особенностей, наиболее важной из которых является резкая диспропорция заболеваемости по возрасту и этническому составу. Так, БК преимущественно наблюдается у детей в возрасте до 5 лет (80–85 %), 2–3 % приходится на возрастную группу старше 5 лет, а пик заболеваемости — на возраст 1–2 года. Вместе с тем случаи заболевания детей более старшего возраста и даже подростков не казуистичны [5]. Важно подчеркнуть, что дебют заболевания позже 5 лет является неблагоприятным признаком в плане развития поражения коронарного русла, в последующем — более частого рецидивирования заболевания, а также поздней диагностики вследствие частой встречаемости неполных форм заболевания [6].
Этиология синдрома Кавасаки до настоящего времени окончательно не установлена. Авторы большинства многочисленных эпидемиологических и иммунологических исследований склоняются к тому, что наиболее вероятным причинным фактором может служить инфекционный агент (вирус Эпштейна — Барр, ретровирус, парвовирус В19, стрептококк, стафилококк, кандида, риккетсия, спирохеты), не исключается роль суперантигенов токсинпродуцирующих стрептококков и стафилококков [7]. Кроме того, немаловажными факторами в развитии синдрома Кавасаки могут быть аутоиммунные механизмы и генетическая предрасположенность. На сегодня установлена связь с антигенами комплекса гистосовместимости HLA B22, B22J2, BW22, а также с рядом генетических полиморфизмов, чаще встречающихся в азиатской популяции, таких как полиморфизмы генов, кодирующих кальцинейрин/NFAT, TGF, транспортера простагландина ABCC4 [7, 8]. Патоморфологически синдром Кавасаки характеризуется развитием некротизирующего васкулита с преимущественным поражением сосудов коронарного русла, при этом в воспалительный процесс могут вовлекаться все слои сосудистой стенки [9].
Поражение сердечно-сосудистой системы встречается в 12–50 % случаев и может протекать в различных клинических вариантах. Наиболее типичное проявление синдрома Кавасаки — это поражение коронарных сосудов (коронарит) в виде их дилатации за счет изменения упругости и эластичности сосудистой стенки на фоне протекающих в ней воспалительных процессов. Дилатационные изменения формируются начиная с 7–10-го дня заболевания, именно с таким сроком связана важность ранней диагностики заболевания [2].
Важно отметить, что большое количество симптомов заболевания, возникающих не одновременно, а последовательно друг за другом, могут создавать у лечащего врача ощущение клинического хаоса. Избежать этого помогает понятие о цикличности течения синдрома Кавасаки, включающего три стадии, для каждой из которых характерна своя совокупность симптомов: острая лихорадочная стадия протяженностью 1–2 недели (иногда до 4–5 недель); подострая стадия — 3–5 недель; выздоровление — через 6–10 недель с момента начала болезни. Понимание последовательности возникновения симптомов при синдроме Кавасаки позволит правильно установить диагноз.
Необходимо также учитывать большое количество инфекционных и неинфекционных заболеваний, клинические проявления которых могут быть похожими на синдром Кавасаки (энтеровирусная, герпетическая инфекция, корь, краснуха, геморрагические лихорадки, паразитозы, острая ревматическая лихорадка, системные васкулиты другой этиологии, лейкоз, туберкулез, неопластические процессы) [10]. Отдельную проблему представляет диагностика неполной формы БК, при которой чаще формируется поражение коронарного русла и чаще наблюдается рецидив заболевания [11].
Основные цели терапии синдрома Кавасаки — устранение клинических проявлений, уменьшение воспаления в стенке коронарной артерии, предупреждение развития тромбоза, нормализация лабораторных показателей, отражающих активность болезни, предотвращение угрожающих жизни состояний (формирование и разрыв сосудистых аневризм), а также восстановление качества жизни, соответствующего возрасту, предупреждение ишемии и инфаркта миокарда [3].
Лечению подлежат как манифестные, так и неполные случаи, поскольку последние чаще приводят к изменению коронарных артерий. При условии ранней (в пределах первых 10 дней болезни) терапии внутривенным иммуноглобулином (ВВИГ) риск развития повреждения коронарных артерий уменьшается более чем в 5 раз [4].
Таким образом, своевременно установленный диагноз и раннее начало специфической терапии БК снижают риск осложнений, развития сердечно-сосудистой патологии и являются залогом благоприятного исхода заболевания.
Цель исследования: повысить эффективность диагностики болезни Кавасаки на основании анализа клинического течения и исходов заболевания у детей, находившихся на лечении в кардиопульмонологическом отделении ДГКБ № 2 г. Днепр.
Материалы и методы
Данная работа проводилась в рамках кафедральной НИР (регистрационный номер 0116U004962), согласована с ЛЭК (протокол № 111), при наличии информированных согласий пациентов и их родителей на проведение исследования.
Проведен ретроспективный анализ историй болезни 7 детей с болезнью Кавасаки, находившихся на стационарном лечении в кардиопульмонологическом отделении за период 2015–2018 годы. Диагноз болезни Кавасаки был верифицирован на основе диагностических критериев в соответствии с действующим клиническим протоколом. Были рассмотрены особенности клинического течения болезни Кавасаки у детей раннего возраста, частота развития осложнений. Особое внимание уделялось оценке своевременной диагностики заболевания и эффективности проводимой терапии.
Всем больным проведены рутинные исследования: общий анализ крови, общий анализ мочи, протеинограмма, печеночный и почечный комплексы, коагулограмма, исследование маркеров аутоиммунного заболевания (LE-клетки, антинуклеарные антитела, антитела к двуспиральной ДНК), электрокардиограмма, УЗИ органов брюшной полости. ЭхоКГ (Д) проводилась на аппарате Sonos-7500 в Днепропетровском областном клиническом центре кардиологии и кардиохирургии.
Результаты
Среди обследованных детей было 4 мальчика и 3 девочки в возрасте от 7 месяцев до 5 лет 10 месяцев. Возрастная структура больных была представлена следующим образом: 1 ребенок — первого года жизни, 3 детей — от 1 до 4 лет и 3 детей — от 5 до 6 лет.
Основными критериями при верификации диагноза болезни Кавасаки были такие клинические проявления, как лихорадка свыше 5 дней; поражение слизистых оболочек в виде конъюнктивита; изменения губ и слизистой оболочки ротовой полости (сухость, эритема или трещины губ (хейлит), малиновый/клубничный язык с выраженными сосочками, диффузная гиперемия слизистой полости рта и глотки); изменения периферических отделов конечностей (эритема ладоней и подошв, плотный отек тыльной поверхности кистей и стоп); полиморфная кожная сыпь; шейная лимфаденопатия [2, 3, 9].
Необходимо отметить, что диагноз «полный синдром Кавасаки» устанавливают у ребенка при наличии лихорадки не менее 5 дней и не менее 4 из 5 основных клинических симптомов. Если же при ЭхоКГ выявлено поражение коронарных артерий, то для постановки диагноза будет достаточно трех признаков. Однако при меньшем количестве критериев в случае лихорадки и признаков поражения сердца состояние классифицируют как неполный вариант болезни Кавасаки. Согласно обобщенным данным литературы, распространенность неполного варианта заболевания составляет от 15 до 36,2 % всех пациентов с БК [3, 6].
Проведенное нами исследование выявило, что диагноз болезни Кавасаки был установлен в период острой стадии (на 6–10-е сутки заболевания) только в 57 % случаев (у 4 детей). У 3 детей (43 % случаев) отмечена более поздняя диагностика — в подострую стадию, в конце третьей недели заболевания.
Сложность диагностики болезни Кавасаки у наблюдаемых детей была обусловлена отсутствием полного комплекса типичных клинических признаков. Только у двоих детей старше 5-летнего возраста мы наблюдали наличие всех клинических симптомов: лихорадка более 5 суток, шейная лимфаденопатия, конъюнктивит (инъецированность конъюнктив), эритема и отек кистей и стоп, эритема слизистой полости рта, губ, полиморфная сыпь (табл. 1). Ведущим симптомом была длительная лихорадка, средняя продолжительность которой составила 14 суток. Причем у детей раннего возраста (первых трех лет жизни) продолжительность лихорадки была свыше 3 недель. У одного пациента в возрасте 3 года и 9 месяцев отмечалось четыре патогномоничных признака, за исключением изменений ладоней и стоп. Таким образом, полный вариант болезни Кавасаки был только у 3 детей.
Неполный вариант наблюдался преимущественно у детей первых трех лет жизни и включал такие симптомы, как конъюнктивит, пятнисто-папулезная сыпь и поражение ротовой полости в виде сухости, гиперемии и трещин губ, гиперемии слизистых ротовой полости, отека сосочков языка по типу малинового в различных комбинациях. Данная симптоматика появлялась не всегда в течение первой недели заболевания, что также затрудняло своевременную диагностику болезни Кавасаки. Заболевания у этих детей дифференцировались с различными инфекциями — скарлатиной, аденовирусной инфекцией, вирусной инфекцией Эпштейна — Барр.
Также у детей раннего возраста мы не наблюдали значительного увеличения регионарных лимфоузлов и изменений на стопах и ладонях. У двоих детей в возрасте до 1,5 года вообще не было лимфаденопатии в течение всего периода наблюдения. А эритема ладоней отмечалась только у одного ребенка раннего возраста и возникла уже в конце третьей недели, то есть в подострой стадии заболевания.
Помимо симптомов, являющихся основными диагностическими критериями болезни Кавасаки, мы наблюдали и другую сопутствующую симптоматику. Так, у 4 (57 %) детей отмечался гастроинтестинальный синдром в виде диареи, рвоты, положительного теста на ацетон. У 2 (28,6 %) детей раннего возраста (до 1,5 года) была симптоматика респираторного заболевания — кашель, осиплость голоса. У 1 ребенка наблюдались изменения со стороны мочевыделительной системы, которые были расценены как инфекция мочевыделительных путей. Также 1 ребенок (14,3 %) жаловался на боли в голеностопных суставах. К сожалению, разнообразие клинических данных у этих детей обусловило более позднюю диагностику болезни Кавасаки и, соответственно, более отсроченный старт специфической терапии.
Лабораторная диагностика имеет большое значение в постановке диагноза синдрома Кавасаки, несмотря на то, что сегодня не существует высокоспецифичного биохимического, генетического или иммунологического маркера этого заболевания. Для первых недель заболевания типичны острофазные изменения: нейтрофильный лейкоцитоз более 15 ´ 109/л, нормохромная нормоцитарная анемия легкой и средней степени тяжести, увеличение уровня С-реактивного белка (СРБ) и увеличение скорости оседания эритроцитов (СОЭ), нормализация которой может продолжаться несколько недель. Для течения болезни характерен нарастающий тромбоцитоз (500–1000 ´ 109/л), достигающий пика на третьей неделе заболевания, постепенно нормализующийся к 4–8-й неделе. Помимо тромбоцитоза происходят сдвиги в системе гемостаза, в целом переходящие в гиперкоагуляцию, выраженность которых коррелирует с тяжестью клинической картины [3, 4].
При проведении лабораторного обследования у всех детей были выявлены следующие гематологические изменения: нейтрофильный лейкоцитоз, значительное повышение СОЭ, высокий уровень С-реактивного белка. Однако можно отметить менее выраженный лейкоцитоз у детей раннего возраста. В данной группе с первых дней заболевания превалировала повышенная СОЭ, которая к 2-й неделе заболевания достигала в среднем 54 мм/ч. Для детей раннего возраста было характерно более длительное сохранение высокой СОЭ, в среднем до 28 суток заболевания. Также у детей раннего возраста мы наблюдали гипохромную анемию І–ІІ степени.
Характерным для болезни Кавасаки признаком является увеличение числа тромбоцитов [3, 4]. В исследуемой группе пациентов данный лабораторный симптом мы наблюдали только у 4 детей, причем в 75 % случаев это были дети до 3-летнего возраста. Показатель тромбоцитоза варьировал на уровне от 408 до 1080 Г/л и достигал максимума к концу 3-й — началу 4-й недели болезни.
Помимо повышения острофазовых показателей воспаления, мы наблюдали другие изменения биохимических показателей: гипоальбуминемию — у 3 пациентов (43 % случаев), повышение уровня трансаминаз — у 2 детей (28,6 % случаев).
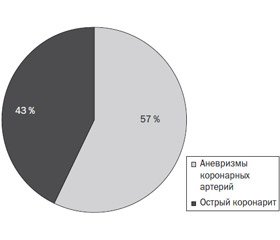
Наличие длительной лихорадки, неэффективность проводимой терапии у пациентов с неполным вариантом синдрома Кавасаки является основанием для проведения ЭхоКГ [2–4]. В группе обследованных детей ЭхоКГ-исследование выявило наличие аневризм коронарных артерий в 57 % случаев (у 4 детей) (рис. 1). Поражение коронарных артерий в виде аневризм было выявлено на 17–22-е сутки от дебюта заболевания, причем в 2 случаях — при повторном ЭхоКГ-исследовании. Предварительное обследование, проводимое на 6-е и 9-е сутки, не выявило выраженных патологических изменений со стороны сердечно-сосудистой системы. У 3 детей аневризмы были мелкие, до 5 мм в диаметре, а у 1 ребенка — более 5 мм.
Преимущественно аневризмы коронарных артерий были выявлены у детей раннего возраста (n = 3) с неполным вариантом болезни Кавасаки, в клинической картине которых, помимо длительной лихорадки, отмечались 2 или 3 специфических признака. Именно отсутствие типичного комплекса клинических симптомов и обусловило позднюю диагностику болезни Кавасаки, в подострой стадии, уже на этапе формирования аневризм коронарных артерий.
Таким образом, поскольку у детей раннего возраста часто имеется неполный набор клинических симптомов и наиболее высок риск кардиальных осложнений, пациентам с лихорадкой длительностью 5–7 дней и более показаны лабораторные исследования, а при наличии признаков системного воспаления — ЭхоКГ даже в отсутствие других клинических признаков синдрома Кавасаки [3, 4].
Во многих случаях несвоевременная диагностика синдрома Кавасаки приводит к необоснованному и малоэффективному применению антибактериальной терапии. Так, в группе нашего исследования всем детям назначались антибиотики, причем 4 детям (57 % случаев) — даже повторные курсы антибиотикотерапии.
Согласно литературным данным, лечение болезни Кавасаки антибиотиками, стероидными гормонами не эффективно. Специфическая терапия направлена на модуляцию иммунного ответа, ингибирование активации тромбоцитов, предотвращение образования коронарных аневризм. Основным методом лечения является сочетание иммуноглобулина для внутривенного введения и ацетилсалициловой кислоты [3, 4, 9].
Всем детям из исследуемой группы после установления диагноза «болезнь Кавасаки» была проведена терапия в соответствии с установленными международными стандартами: ВВИГ в дозе 2 г/кг массы тела и аспирин в дозе 50–80 мг/кг/сут. Доза и длительность курса аспиринотерапии определялись в зависимости от выраженности лихорадки и других клинических симптомов, а также наличия аневризм при ЭхоКГ-исследовании. После нормализации температуры доза аспирина постепенно снижалась.
Двум детям было проведено однократное введение ВВИГ, что привело к нормализации температуры и улучшению общего самочувствия. Остальным пациентам с болезнью Кавасаки потребовалось 2–3 введения ВВИГ, что обосновывалось пролонгацией лихорадки, слизистокожного синдрома, выраженностью интоксикационного синдрома, наличием высокой воспалительной активности (лейкоцитоз с нейтрофильным сдвигом влево, нарастающая в динамике анемия, тромбоцитоз, резко повышенная СОЭ, высокий уровень СРБ), а также сохранением сонографических данных со стороны сердца.
Все дети были выписаны в удовлетворительном состоянии с рекомендациями динамического наблюдения по месту жительства с контролем ЭКГ, ЭхоКГ. Повторное проведение ЭхоКГ-исследования на момент выписки установило значительный регресс аневризм коронарных артерий у всех наблюдаемых детей. Пациентам с выявленными аневризмами коронарных артерий была рекомендована длительная аспиринотерапия в низких дозах под контролем коагулограммы, ревмокомплекса и ЭхоКГ до полного исчезновения аневризм.
Выводы
1. Болезнь Кавасаки является одной из важнейших причин развития приобретенных сердечно-сосудистых заболеваний у детей. Ранняя диагностика синдрома Кавасаки важна именно с позиции предотвращения долгосрочных осложнений этого острого заболевания.
2. Гиподиагностика синдрома Кавасаки связана с низкой информированностью врачей об основных диагностических критериях заболевания и наличием большого количества клинических масок болезни.
3. У детей раннего возраста наиболее часто встречается неполный вариант синдрома Кавасаки, что затрудняет его диагностику.
4. Длительная лихорадка в сочетании даже с 2–3 типичными признаками синдрома Кавасаки должна быть абсолютным показанием к проведению ЭхоКГ с обязательной визуализацией коронарных артерий.
5. Своевременная диагностика синдрома Кавасаки и максимально раннее введение внутривенного иммуноглобулина предупреждает развитие коронарных осложнений.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов при подготовке данной статьи.
1. Шостакович-Корецкая Л.Р. Синдром Кавасаки как причина длительной лихорадки у детей. Актуальная инфектология. 2013. № 1. С. 104-107.
2. Лутфуллин И.Я. Синдром Кавасаки: клинические алгоритмы и проблема гиподиагностики заболевания. Вестник современной клинической медицины. 2016. Т. 9, вып. 2. С. 52-60.
3. Майданник В.Г. Болезнь Кавасаки в детском возрасте. Киев: Логос, 2015. 375 с.
4. Лыскина Г.А., Виноградова О.И., Ширинская О.Г. [и др.]. Клиника, диагностика и лечение синдрома Кавасаки. Клинические рекомендации. Москва, 2011. 57 с. http://www.rodkb.ru/Klinic_rec/5.pdf
5. Park Y.W. Epidemiology of Kawasaki disease in Korea. Korean J. Pediatr. 2008. № 5. Р. 452-456.
6. Лыскина Г.А. Синдром Кавасаки у детей, заболевших в возрасте 5 лет и старше. Обзор литературы, собственное наблюдение. Вестник современной клинической медицины. 2016. Т. 2, вып. 2. С. 52-60.
7. Rowley A.H., Baker S.C., Shulman S.T. et al. Ultrastructural, immunofluorescence, and RNA evidence support the hypothesis of a "new" virus associated with Kawasaki disease. J. Infect. Dis. 2011. Vol. 203. P. 1021-30.
8. Franco A., Shimizu C., Tremoulet A.H. et al. Memory T-cells and characterization of peripheral T-cell clones in acute Kawasaki disease. Autoimmunity. 2010. Vol. 43. P. 317-24.
9. Лыскина Г.А. Клиническая картина, диагностика и лечение синдрома Кавасаки: известные факты и нерешенные проблемы. Вопросы современной педиатрии. 2013. Т. 12, № 1. С. 63-73.
10. Бехтерева М.К. Синдром Кавасаки в практике педиатра и инфекциониста. Клинико-лабораторный консилиум. 2013. № 1. С. 43-49.
11. Sudo D., Monobe Y., Yashiro M. et al. Coronary artery lesions of incomplete Kawasaki disease: a nation wide survey in Japan. Eur. J Pediatr. 2012. Vol. 171(4). P. 651-656.

/20-2.jpg)
/20-1.jpg)