Международный неврологический журнал Том 16, №5, 2020
Вернуться к номеру
Особливості концентрації гомоцистеїну у сироватці крові дітей із вазовагальними синкопе
Авторы: Ковальчук Т.А., Боярчук О.Р.
Тернопільський національний медичний університет імені І.Я. Горбачевського Міністерства охорони здоров’я України, м. Тернопіль, Україна
Рубрики: Неврология
Разделы: Клинические исследования
Версия для печати
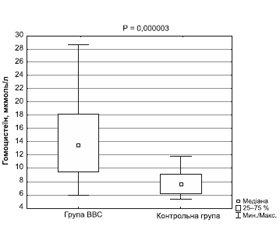
Актуальність. Останніми роками з’являється все більше повідомлень щодо розвитку дефіциту вітаміну B12 серед пацієнтів із вазовагальними синкопе, а отже, рівень гомоцистеїну у цих пацієнтів теж може відрізнятися від показників у здоровій популяції. Мета: вивчити особливості концентрації гомоцистеіїну у сироватці крові дітей із вазовагальними синкопе. Матеріали та методи. Основну групу становили 28 дітей віком 8–17 років із діагнозом вазовагального синкопе, контрольну — 23 практично здорові дитини аналогічного віку, які не мали ознак хронічних захворювань. Рівні вітамінів В6, В12, фолієвої кислоти та гомоцистеїну у сироватці крові визначали за допомогою колориметричного методу імуноферментного аналізу з використанням тест-системи Monobind. Гіпергомоцистеїнемію діагностували у разі, якщо рівень гомоцистеїну в крові був вище 15 мкмоль/л. Результати. У дітей із вазовагальними синкопе виявлено знижені показники вітамінів В6 та В12 при незміненому рівні фолієвої кислоти порівняно зі здоровими респондентами. У групі вазовагальних синкопе реєструвався підвищений рівень гомоцистеїну проти групи контролю (13,86 ± 0,97; 7,81 ± 0,36 мкмоль/л; р = 0,000003). Поширеність гіпергомоцистеїнемії серед дітей із вазовагальними синкопе становила 46,4 %, тоді як у контрольній групі жодного випадку не реєструвалося (χ2 = 14,33; р = 0,0002). Показник гомоцистеїну корелює з модою та середнім значенням інтервалу P-Q, модою інтервалу Q-T, вітаміном В6 (р < 0,05). Зростання концентрації сироваткового гомоцистеїну супроводжується погіршенням окремих показників якості життя за даними опитувальників PedsQLTM (шкала загального благополуччя, багатофакторна шкала втомлюваності, модуль впливу на родину). Висновки. Вазовагальні синкопе у дитячому віці асоціюються з підвищеною концентрацією гомоцистеїну у сироватці крові. Поширеність гіпергомоцистеїнемії серед дітей із вазовагальними синкопе становить 46,4 %.
Актуальность. В последние годы появляется все больше сообщений о развитии дефицита витамина B12 среди пациентов с вазовагальными обмороками, следовательно, уровень гомоцистеина у этих пациентов тоже может отличаться от показателей в здоровой популяции. Цель: изучить особенности концентрации гомоцистеиина в сыворотке крови детей с вазовагальными обмороками. Материалы и методы. Основную группу составили 28 детей в возрасте 8–17 лет с диагнозом вазовагального обморока, контрольную — 23 практически здоровых ребенка аналогичного возраста, не имевших признаков хронических заболеваний. Уровни витаминов В6, В12, фолиевой кислоты и гомоцистеина в сыворотке крови определяли с помощью колориметрического метода иммуноферментного анализа с использованием тест-системы Monobind. Гипергомоцистеинемию диагностировали при уровне гомоцистеина в крови выше 15 мкмоль/л. Результаты. У детей с вазовагальными обмороками были обнаружены сниженные показатели витаминов В6 и В12 при неизменном уровне фолиевой кислоты по сравнению со здоровыми респондентами. В группе вазовагальных обмороков регистрировался повышенный уровень гомоцистеина по сравнению с контролем (13,86 ± 0,97; 7,81 ± 0,36 мкмоль/л; р = 0,000003). Распространенность гипергомоцистеинемии среди детей с вазовагальными синкопе составила 46,4 %, тогда как в контрольной группе не регистрировалась (χ2 = 14,33; р = 0,0002). Показатель гомоцистеина коррелирует с модой и средним значением интервала P-Q, модой интервала Q-T, витамином В6 (р < 0,05). Увеличение концентрации сывороточного гомоцистеина сопровождается ухудшением отдельных показателей качества жизни по данным опросников PedsQLTM (шкала общего благополучия, многофакторная шкала усталости, модуль влияния на семью). Выводы. Вазовагальные синкопе в детском возрасте ассоциируются с повышенной концентрацией гомоцистеина в сыворотке крови. Распространенность гипергомоцистеинемии среди детей с вазовагальным синкопе составляет 46,4 %.
Background. In recent years, there have been increasing reports of vitamin B12 deficiency in patients with vasovagal syncope. Therefore, homocysteine levels in these patients may also differ from those in the healthy population. The purpose of the research was to study the peculiarities of serum homocysteine concentration in children with vasovagal syncope. Materials and methods. The main group consisted of 28 children aged 8–17 years with a diagnosis of vasovagal syncope. The control group included 23 apparently healthy children of the same age who had no signs of chronic diseases. The determination of vitamin B6, B12, folic acid, and homocysteine in the blood serum was performed by means of a colorimetric enzyme-linked immunosorbent assay using the Monobind test system. Hyperhomocysteinemia was diagnosed at the level of serum homocysteine above 15 μmol/l. Results. There were decreased serum levels of vitamins B6 and B12 with unchanged folic acid levels in children with vasovagal syncope compared to healthy respondents. In the vasovagal syncope group, an increased level of homocysteine was observed compared to the controls (13.86 ± 0.97 μmol/l; 7.81 ± 0.36 μmol/l; p = 0.000003). The prevalence of hyperhomocysteinemia among children with vasovagal syncope was 46.4 %, whereas in the control group it was not recorded at all (χ2 = 14.33; p = 0.0002). Homocysteine correlates with P-Q interval (moda and mean), Q-T interval (moda), vitamin B6 (p < 0.05). An increase in serum homocysteine concentration is accompanied by deterioration of some quality of life indicators according to the PedsQLTM (general well-being scale, multifactorial fatigue scale, family impact module). Conclusions. Vasovagal syncope in childhood is associated with increased serum homocysteine. The prevalence of hyperhomocysteinemia among children with vasovagal syncope is 46.4 %.
вазовагальні синкопе; гомоцистеїн; діти
вазовагальные обмороки; гомоцистеин; дети
vasovagal syncope; homocysteine; children
Вступ
Матеріали та методи
Результати
/31.jpg)
Обговорення
Висновки
1. Shevchuk S.V., Postovitenko K.P., Iliuk I.A. et al. The relationship between homocysteine level and vitamins B12, B9 and B6 status in patients with chronic kidney disease. Wiad. Lek. 2019. 72(4). Р. 532-538.
2. Al-Sadeq D.W., Nasrallah G.K. The Spectrum of Mutations of Homocystinuria in the MENA Region. Genes (Basel). 2020. 11(3). E330. doi: 10.3390/genes11030330.
3. Coppedè F., Stoccoro A., Tannorella P., Migliore L. Plasma Homocysteine and Polymorphisms of Genes Involved in Folate Metabolism Correlate with DNMT1 Gene Methylation Levels. Metabolites. 2019. 9(12). E298. doi: 10.3390/metabo9120298.
4. Weber Hoss G.R., Sperb-Ludwig F., Schwartz I.V.D., Blom H.J. Classical homocystinuria: A common inborn error of metabolism? An epidemiological study based on genetic databases. Mol. Genet. Genomic. Med. 2020. 30. E1214. doi: 10.1002/mgg3.1214.
5. Veeranki S., Gandhapudi S.K., Tyagi S.C. Interactions of hyperhomocysteinemia and T cell immunity in causation of hypertension. Can. J. Physiol. Pharmacol. 2017. 95(3). P. 239-246.
6. Morris A.A., Kožich V., Santra S. et al. Guidelines for the diagnosis and management of cystathionine beta-synthase deficiency. J. Inherit. Metab. Dis. 2017. 40(1). P. 49-74.
7. Chen S., Honda T., Ohara T. et al. Serum homocysteine and risk of dementia in Japan. J. Neurol. Neurosurg. Psychiatry. 2020. 0. P. 1-7. doi: 10.1136/jnnp-2019-322366.
8. Zhang T., Jiang Y., Zhang S. et al. The association between homocysteine and ischemic stroke subtypes in Chinese: A meta-analysis. Medicine (Baltimore). 2020. 99(12). E19467. doi: 10.1097/MD.0000000000019467.
9. Yevtushenko S.K., Filimonov D.A. The role of homocysteine in the development of ischemic stroke in young adults (review of the literature and own observation). International Neurological Journal. 2013. 7(61). P. 19-30.
10. Gohlke J.H., Lloyd S.M., Basu S. et al. Methionine-Homocysteine Pathway in African-American Prostate Cancer. JNCI Cancer Spectr. 2019. 3(2). P. 19. doi: 10.1093/jncics/pkz019.
11. Oussalah A., Levy J., Berthezène C. et al. Health outcomes associated with vegetarian diets: An umbrella review of systematic reviews and meta-analyses. Clin. Nutr. 2020. doi: 10.1016/j.clnu.2020.02.037.
12. Fakhrzadeh H., Ghotbi S., Pourebrahim R. et al. Total plasma homocysteine, folate, and vitamin b12 status in healthy Iranian adults: the Tehran homocysteine survey (2003–2004): a cross-sectional population based study. BMC Public Health. 2006. 6(29). https://doi.org/10.1186/1471-2458-6-29.
13. Ghaznain M., Donnelly T.M., Halpenny L. 019 Tilt Table Test Outcome in the Diagnosis and Prevalence of Syncope in Patients with Vitamin D and Vitamin B12 Deficiency. Age and Ageing. 2017. 46(3). P. 13-59.
14. Pektas A., Koken R., Koca H.B. Serum vitamin B-12 in children presenting with vasovagal syncope. Asia Pacific Journal of Clinical Nutrition. 2018. 27. P. 176-181.
15. Ganjehei L., Massumi A., Razavi M., Wilson J.M. Orthostatic hypotension as a manifestation of vitamin B12 deficiency. Texas Heart Institute Journal. 2012. 39(5). P. 722-723.
16. Acar Arslan E., Arslan E., Serin M., Turan O. P2–2736: Vitamin B12 deficiency and neurologic findings: Retrospective analysis of 124 patients European Journal of Paediatric Neurology. 2015. 19(1). S95.
17. Li Y., He B., Li H. et al. Plasma Homocysteine Level in Children with Postural Tachycardia Syndrome. Front Pediatr. 2018. 6. P. 375. doi: 10.3389/fped.2018.00375.
18. Brignole M., Moya A., Lange F.J. et al. ESC Guidelines for the diagnosis and management of syncope. European Heart Journal. 2018. 39(21). P. 1883-1948.
19. Tanaka H., Fujita Y., Takenaka Y. et al. Japanese clinical guidelines for juvenile orthostatic dysregulation version 1. Pediatr. Int. 2009. 51. P. 169-179.
20. Zou R., Wang S., Zhu L. et al. Calgary score and modified Calgary score in the differential diagnosis between neurally mediated syncope and epilepsy in children. Neurol. Sci. 2017. 38(1). P. 143-149.
21. Scaling and scoring of the Pediatric Quality of Life Inventory™ PedsQL. Mapi Research Trust. Version 13. 2013. 2013. 115 P.
22. Mendes R.H., Mostarda C., Candido G.O. et al. Moderate hyperhomocysteinemia provokes dysfunction of cardiovascular autonomic system and liver oxidative stress in rats. Autonomic Neuroscience. 2014. 180. P. 43-47.
23. Gariballa S. Testing homocysteine-induced neurotransmitter deficiency, and depression of mood hypothesis in clinical practice. Age and Ageing. 2011. 40. P. 702-705. doi: 10.1093/ageing/afr086.
24. Jagadish Kumar K., Saldanha K., Sushma K. et al. A prospective study of homocysteine and its relation to body mass index and lipid profile in school children. Indian Pediatr. 2017. 54. P. 935-937. https://doi.org/10.1007/s13312-017-1185-0.
25. Wu H., Wang B., Ban Q. et al. Association of total homocysteine with blood pressure in a general population of Chinese adults: a cross-sectional study in Jiangsu province, China. BMJ Open. 2018. 8. E021103. doi: 10.1136/bmjopen-2017-021103.
26. Lee D.H., Lee K.M., Yoon J.M. et al. P wave dispersion on 12-lead electrocardiography in adolescents with neurocardiogenic syncope. Korean J. Pediatr. 2016. 59(11). P. 451-455. doi: 10.3345/kjp.2016.59.11.451.
27. Meki B., Zübeyde F.D., Fikri D. et al. The Turkish Journal of Pediatrics. 2019. 61(1). P. 85-91. doi: 10.24953/turkjped.2019.01.013.

/31_2.jpg)
/32.jpg)