Несмотря на большое количество психотерапевтических препаратов, разработанных в последние годы, проблема лечения неврологических и психиатрических симптомов, таких как повышенная возбудимость или перенапряжение, связанных с когнитивными расстройствами, остается нерешенной, и это же относится к измененным состояниям личности в младенчестве, связанным с изменениями в эмоциональном развитии, обусловленными факторами окружающей среды или образованием.
Настоящий терапевтический арсенал не обеспечивает необходимыми психотерапевтическими эффектами, поскольку седативные транквилизирующие препараты, даже достигая симптоматического седативного эффекта, имеют небольшую эффективность для контроля всей органической симптоматики, такой как анорексия, гастралгия, цефалгия, диарея, что очень часто наблюдается у пациентов этого типа. С другой стороны, эти препараты демонстрируют серьезный недостаток, заключающийся в том, что их применение влечет за собой значительные побочные эффекты, и они провоцируют снижение умственной деятельности.
Свойства компонентов
Было доказано, что глутамат магния гидробромид (МГБ), синтезированный в исследовательском отделе компании «Феррер» и запатентованный в нескольких странах, обладает седативным эффектом, оказываемым на центральную и вегетативную нервную систему; этот компонент является абсолютно безопасным и не оказывает побочных эффектов. МГБ оказывает лечебное воздействие на личностные изменения посредством церебрального трофического действия, улучшая умственные способности пациентов. МГБ действует как агонист глутаматных рецепторов, препятствуя глутаминовому действию. МГБ обладает седативным эффектом с анксиолитическим действием.
Чтобы улучшить мозговое трофическое действие, МГБ был соединен с витамином B6 и с γ-аминомасляной кислотой (ГАМК) и γ-амино-β-гидроксибутировой кислотой (ГАБОМК) — двумя компонентами, которые, как известно, содержатся в большой пропорции в составе нервной ткани и составляют вместе с глутаматом 80 % небелкового аминного азота, играющего важную роль в физиологии нервной системы в качестве медиаторов в процессах синаптических переносов. Гамалате В6 оказывает седативное действие на повышенную возбудимость нервной системы и содержит аминокислоты, которые очень важны для активации умственной деятельности [1].
Гамма-аминомасляная кислота
ГАМК является основным ингибирующим нейромедиатором в центральной нервной системе (ЦНС), в то время как глутамат является основным возбуждающим нейромедиатором [2]. ГАМК играет роль в регуляции возбудимости нейронов по всей нервной системе и участвует в различных биологических функциях, таких как двигательная система, обучение, репродукция, циркадные ритмы, а также познание, эмоции и сон. Система ГАМК широко используется для лечения тревожных расстройств, бессонницы, эпилепсии, беспокойства и агрессивного поведения. Система ГАМК чувствительна к значительному числу фармакологических агентов (этанол, бензодиазепины, барбитураты и нейростероиды). ГАМКергические механизмы были продемонстрированы в различных периферических тканях и органах. ГАМК — это нейротрансмиттер, который является фундаментальным в гомеостазе нейронов [2].
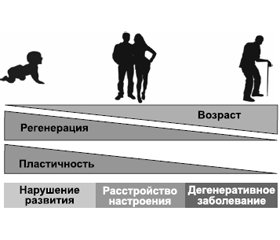
Баланс между возбуждением и торможением является важной характеристикой, которую необходимо поддерживать, чтобы избежать патологических процессов. Баланс торможения и возбуждения контролирует пластичность мозга взрослого человека и лежит в основе патогенеза нарушений развития нервной системы [3]. Ингибирующие интернейроны в целом имеют решающее значение для нормальных когнитивных процессов [4–6]. Нейротрансмиссия кортикального глутамата и ГАМК существенно связана с когнитивным дефицитом [7]. Увеличение передачи ГАМК в префронтальных регионах может быть базовым нейрональным элементом улучшения социальной компетентности [8].
ГАБОМК можно рассматривать как производ-ную ГАМК. ГАБОМК является одним из важнейших факторов ингибирования мозга, так как она в 5–19 раз активнее ГАМК [31]. При использовании в качестве противосудорожного средства это соединение обладает очень интенсивным действием на уровне ЦНС.
Магния глутамат гидробромид
Фармакологически МГБ можно классифицировать как седативное средство мягкого действия, обладающее анксиолитической активностью. Объяснение этому факту необходимо искать в его химической молекуле. Соединение с магнием и бромом в форме хелата дает соединение с жесткой структурой, которое будет действовать только как частичный агонист L-глутамата, тем самым уменьшая стимуляцию и достигая мягкого седативного эффекта. В этом отличие МГБ от других транквилизирующих препаратов, которые вызывают прямое торможение стимуляции, таких как бензодиазепины и барбитураты, но с высокой частотой нежелательных побочных эффектов, которые до этого момента не отмечаются для МГБ [37]. МГБ усиливает действие седативных препаратов. Чтобы проверить его антагонизм по сравнению со стимуляторами ЦНС, кардиазол и стрихнин были выбраны в качестве типичных лекарств. МГБ изменяет аспект судорожного явления, вызванного кардиазолом. Клоническая форма становится короче, а тоническая — менее интенсивной. Остаточная гипервозбудимость исчезает [1]. При равной терапевтической дозе с бромидом калия уровни брома в крови, полученные с помощью МГБ, поддерживались на 60 % ниже, чем с вышеупомянутым неорганическим бромидом [1]. Все это объясняет идеальную переносимость после терапии МГБ и делает ее показанной во всех обычных условиях повышенной возбудимости психосоматического происхождения.
Витамин В6
Это один из витаминных факторов, вызывающих наибольший интерес в связи с важностью его функций. Витамин В6 относится к группе химически сходных соединений, которые могут быть преобразованы в биологических системах. Витамин В6 входит в группу витаминов группы В, необходимых питательных веществ. Его активная форма, пиридоксаль 5'-фосфат, служит коферментом в примерно 100 ферментативных реакциях в метаболизме аминокислот, глюкозы и липидов [38]. Витамин В6 ускоряет превращение глутаминовой кислоты в ГАМК в качестве кофермента GAD (глутаматдекарбоксилаза).
Механизм действия [39]
Прямая поставка ГАМК повышает ее уровень, способствуя ингибирующей нейротрансмиссии (анксиолитическое действие). Витамин B6 помогает ускорить превращение глутаминовой кислоты в ГАМК. ГАБОМК блокирует рецепторы ГАМК A и ГАМК B, останавливая расщепление ГАМК. Приостановление глутаминового действия обусловлено наличием МГБ, обладающего седативным эффектом с анксиолитическим действием.
Клинический опыт
В 1990 году Zamora & Pérez [46] опубликовали свое исследование с использованием Гамалате B6 для лечения тревоги. Это было открытое исследование среди 60 пациентов (14–75 лет) с тревожностью, получавших лечение в течение 60 дней. Авторы обнаружили значительные улучшения через 30 и 60 дней (р < 0,01) симптомов тревоги (рис. 8). Никаких побочных эффектов во время исследования не было обнаружено.
Авторы пришли к выводу, что Гамалате B6 тормозит активность при витальной тревоге, улучшает психомоторную активность пациента и повышает степень эффективности.
Также в 1990 году Núñez & López-Pousa [47] опубликовали исследование, в котором оценивали влияние Гамалате B6 у пациентов с головной болью напряжения. Это было открытое исследование с 36 пациентами (42–71 года) с головной болью напряжения различного происхождения, получавших Гамалате B6 в течение 30 дней. После 30 дней лечения препарат рассматривался в качестве эффективного у 75 % пациентов (табл. 1).
В качестве побочных эффектов 27 и 22 % пациентов назвали увеличение степени спокойствия и сонливости, но пациенты не считали эти эффекты негативными. Было зарегистрировано по одному случаю бессонницы, гастралгии и ночных кошмаров у трех различных пациентов.
В 1992 году Martínez Mendoza опубликовал открытое исследование, проведенное среди 100 пациентов (41 мужчина и 59 женщин) в возрасте от 17 до 70 лет (в среднем 41 год). У всех наблюдался профиль интенсивного или сильного беспокойства, несмотря на то что 48 из них проходили лечение бензодиазепинами в течение более одного месяца.
Основная цель исследования состояла в том, чтобы оценить эффективность Гамалате В6 в отношении общих симптомов тревоги у пациентов и определить эффективность препарата у пациентов, получавших бензодиазепины, и у тех, кто не получал эту терапию. Вторичная цель состояла в том, чтобы определить, будет ли замена бензодиазепинов на Гамалате В6 оказывать положительные или нежелательные эффекты. Оценки основывались на тесте Гамильтона на тревожность. Пациенты были распределены на две группы.
Группа A: пациенты, которые не принимали анксиолитические препараты и имели выраженные или тяжелые симптомы тревоги. В течение 30 дней исследования они принимали Гамалате B6 в дозе 6 таблеток в день (2 таблетки после каждого приема пищи).
Группа B: пациенты, которые получали бензодиазепины более одного месяца и тем не менее имели выраженные симптомы тревоги. В течение первых 15 дней доза бензодиазепина была уменьшена вдвое; применялся Гамалате B6, таблетки, покрытые оболочкой, в дозе 3 таблетки в день (1 таблетка после каждого приема пищи). В течение последующих 15 дней, чтобы завершить 30-дневное исследование, прием всех бензодиазепинов прекращался и пациенты принимали исключительно Гамалате В6 в дозе 6 таблеток в день (по 2 таблетки после каждого приема пищи).
/66.jpg)
Было продемонстрировано, что Гамалате В6 оказался эффективным у 79 % пациентов, которые находились в состоянии тяжелой или довольно тяжелой тревоги (табл. 4). Результаты, полученные с Гамалате B6, были превосходными, так как исчезли психологические и психосоматические симптомы тревожного типа. Замена бензодиазепинов на Гамалате B6 не вызывала беспокойства или любого другого типа расстройства. Затем автор пришел к выводу, что Гамалате B6 является препаратом, который практически не имеет каких-либо побочных эффектов и продемонстрировал отличную переносимость без необходимости какой-либо корректировки дозы в любое время [49].
Последнее клиническое исследование с применением Гамалате B6 было опубликовано в 2002 году Лопес-Поуса и соавт. [51] с оценкой воздействия Гамалате B6 на качество жизни пациентов с фибромиалгией. Фибромиалгия характеризуется генерализованной доброкачественной хронической скелетно-мышечной болью неизвестной этиологии, не локализованной в суставах. Согласно критериям классификации Американского колледжа ревматологии, двумя основными характеристиками для диагностики фибромиалгии являются наличие генерализованной боли продолжительностью более трех месяцев и аномальная чувствительность к давлению пальцами в определенных областях тела. Кроме того, часто присутствуют другие неудобства, такие как ощущение отека и утренней скованности в руках, парестезии и дизестезии в руках, трудности с засыпанием и/или невосстанавливающий сон. Фибромиалгия — очень частая жалоба, которая вызывает высокий уровень невыхода на работу с вытекающими отсюда прямыми и косвенными издержками. Несмотря на распространенность синдрома и связанные с ним психологические и социальные издержки, нет четких результатов относительно его этиологии или фармакологического лечения.
Были испробованы различные подходы, включая антидепрессанты для повышения уровня серотонина и норэпинефрина, нестероидные противовоспалительные препараты, которые ингибируют высвобождение простагландинов при воспалительных процессах, производные опиатов, антагонисты натриевых и кальциевых каналов для стабилизации мембран и препараты ГАМКергических агонистов, которые повышают уровни этого нейромедиатора и снижают возбудимость нервных клеток.
Целью данного проспективного открытого наблюдательного исследования является определение эффективности Гамалате B6 при симптоматическом лечении фибромиалгии в течение 3 месяцев у пациентов, посещающих неврологическую клинику. Выборка состояла из 24 пациентов (92 % женщин), средний возраст 53,33 года (СО = 6,15; диапазон = 40–67), которые посещали невролога и соответствовали критериям ревматической фибромиалгии, установленным Американским колледжем ревматологии: постоянные мышечно-скелетные боли продолжительностью более трех месяцев и наличие по крайней мере одиннадцати специфических болевых точек, выявленных при умеренном надавливании пальцем около 4 кг/см2.
Для оценки эффективности использовался опросник воздействия фибромиалгии (FIQ) — короткий, простой в применении конкретный инструмент, состоящий в общей сложности из 10 пунктов.
Его целью является оценка состояния здоровья на основании физического, психологического, социального и общего проявления пациентов с фибромиалгией. Этот инструмент позволяет отличать пациентов, которые упоминают клинические улучшения, от тех, кто их не упоминает.
После обследования пациенты приступали к фармакологическому лечению Гамалате В6 в дозе 2 таблетки каждые 8 часов наряду с обычным приемом лекарственных средств (табл. 8). Через три месяца пациентов оценивали с использованием того же опросника.
Основной причиной обращения за консультацией была головная боль — 50 % случаев, сопровождаемая ощущением головокружения или нестабильности в 25 % случаев и потерей памяти в оставшихся 25 %.
Среди сопутствующих симптомов выделялись признаки депрессии (83 %), нарушений сна (75 %) и головной боли (67 %) (табл. 9).
Средний балл по FIQ в базальное время составлял 67,70 (СО = 6,96; диапазон = 55–83), тогда как через три месяца он составлял 44,33 (СО = 6,24; диапазон = 32–57), и между обоими показателями существовали значительные различия (Z = –4,28; р = 0,001). Способность выполнять повседневные жизненные действия (DLA), оцененная по пункту 1 опросника FIQ, включающему 10 подпунктов с диапазоном оценок от 0 (всегда) до 3 (никогда), составила 14,7 балла (СО = 5,06) на базальное время. Из оставшихся пунктов FIQ, которые оценивают симптомы, связанные с фибромиалгией, у пациентов с наивысшими показателями в базальное время были усталость, беспокойство, утренняя усталость и скованность, все с оценками выше 7 баллов. Через три месяца балл за пункт по способности выполнять DLA составил 8,95 (СО = 4,76) и наблюдалось снижение в оценках по всем пунктам FIQ. Разница между обеими оценками была значимой для всех пунктов, за исключением дней с хорошим самочувствием в течение последних 7 дней, тревоги и симптомов депрессии (табл. 10).
Согласно BIP-sp, базовые показатели составили 72,79 (СО = 8,30; диапазон = 56–90) и 51,66 (СО = 6,43; диапазон = 39–63) балла через три месяца; разница между обеими оценками была значимой (Z = –4,32; р = 0,001). Самый высокий показатель в базальное время был продемонстрирован влиянием боли на настроение — 8,95 балла (SD = 1,80), затем следовали максимальная выраженность боли и влияние на способность к отвлечению с оценками выше 7 баллов. Через три месяца влияние, вызванное болью во сне, и способность ходить были единственными областями, которые не продемонстрировали значительного улучшения, тогда как во всех других рассматриваемых областях были отмечены значительные изменения по шкале BIP-sp в диапазоне от 1,69 до 2,83 балла (табл. 11).
Ни в одном случае лечение Гамалате B6 не приостанавливалось по причине непереносимости и не было никаких связанных с ним побочных реакций.
В двух случаях отмечалась тошнота и в одном случае беспокойство, которые были связаны с сопутствующим введением других лекарственных средств, так как они уже присутствовали к началу применения Гамалате B6.
Результаты, полученные в этом исследовании, позволяют предположить, что Гамалате B6 может оказывать благоприятное воздействие при симптоматическом лечении фибромиалгии, главным образом в качестве дополнения к обычному лечению. Результаты показывают статистически значимое клиническое улучшение в пределах от 1 до 3 баллов через три месяца во всех шкалах оценивания, используемых для пациентов, у которых не было продемонстрировано явного улучшения при обычном лечении.
Список литературы
1. Bartolomé M. Toxicological and Pharmacological test carried out with the specialty Gamalate B6. Unpublished data.
2. Gamma-aminobutyric acid (GABA). Altern. Med. Rev. 2007. 12 (3). 274-279.
3. Gatto C.L., Broadie K. Genetic controls balancing excitatory and inhibitory synaptogenesis in neurodevelopmental disorder models. Front. Synaptic. Neurosci. 2010. 2. 4.
4. Krook-Magnuson E., Varga C., Lee S.H., Soltesz I. New dimensions of interneuronal specialization unmasked by principal cell heterogeneity. Trends Neurosci. 2012. 35 (3). 175-184.
5. Gonzalez-Burgos G., Fish K.N., Lewis D.A. GABA neuron alterations, cortical circuit dysfunction and cognitive deficits in schizophrenia. Neural. Plast. 2011. 1-24.
6. Lehmann K., Steinecke A., Bolz J. GABA through the ages. regulation of cortical function and plasticity by inhibitory interneurons. Neural. Plast. 2012. 1-11.
7. Scholl J., Kolling N., Nelissen N., Stagg C.J., Harmer C.J. et al. Excitation and inhibition in anterior cingulate predict use of past experiences. 2017. eLife. doi: 10.7554/eLife.20365.
8. Lee J.S., Lee J.D., Park H.J., Oh M.K., Chun J.W. et al. Is the GABA System Related to the Social Competence Improvement Effect of Aripiprazole? An (18) F-Fluoroflumazenil PET Study. Psychiatry Investig. 2013. 10 (1). 75-80.
9. Gibson K.M, Sweetman L., Nyhan W.L., Jakobs C., Rating D. et al. Succinic semialdehyde dehydrogenase deficiency. an inborn error of gamma-aminobutyric acid metabolism. Clin. Chim. Acta. 1983. 133 (1). 33-42.
10. Pizzarelli R., Cherubini E. Alterations of GABAergic signaling in autism spectrumdisorders. Neural. Plast. 2011. 297153.
11. Robertson C.E., Ratai E.M., Kanwisher N. Reduced GABAergic Action in the Autistic Brain. Curr. Biol. 2016. 26 (1). 80-85.
12. Ajram L.A., Horder J., Mendez M.A., Galanopoulos A., Brennan L.P. et al. Shifting brain inhibitory balance and connectivity of the prefrontal cortex of adults with autism spectrum disorder. Transl. Psychiatry. 2017. 7 (5). e1137.
13. Inui T., Kumagaya S., Myowa-Yamakoshi M. Neurodevelopmental Hypothesis about the Etiology of Autism Spectrum Disorders. Front. Hum. Neurosci. 2017. 11. 354.
14. Catts V.S., Fung S.J., Long L.E., Joshi D., Vercammen A. et al. Rethinking schizophrenia in the context of normal neurodevelopment. Front. Cell. Neurosci. 2013. 7. 60.
15. Giacopuzzi E., Gennarelli M., Minelli A., Gardella R., Valsecchi P. et al. Exome sequencing in schizophrenic patients with high levels of homozygosity identifies novel and extremely rare mutations in the GABA/glutamatergic pathways. PLoS One. 2017. 12 (8). e0182778.
16. Wang J., Tang Y., Zhang T., Cui H., Xu L. et al. Reduced γ-Aminobutyric Acid and glutamate + glutamine levels in drug-naïve patients with first-episode schizophrenia but not in those at ultrahigh risk. Neural. Plast. 2016. 3915703.
17. Yee J.Y., Nurjono M., Teo S.R., Lee T.S., Lee J. GAD1 gene expression in blood of patients with first-episode psychosis. PLoS One. 2017. 12 (1). e0170805.
18. Haussleiter I.S., Wandinger K.P., Juckel G. A case of GABAR antibodies in schizophrenia. BMC Psychiatry. 2017. 17 (1). 9.
19. Gilpin N.W. Corticotropin-releasing factor (CRF) and neuropeptide Y (NPY): effects on inhibitory transmission in central amygdala, and anxiety- & alcohol-related behaviors. Alcohol. 2012. 46 (4). 329-337.
20. Zhang Z., Fan Q., Bai Y., Wang Z., Zhang H. et al. Brain Gamma-Aminobutyric Acid (GABA) concentration of the prefrontal lobe in unmedicated patients with obsessive-compulsive disorder: a research of magnetic resonance spectroscopy. Shanghai Arch. Psychiatry. 2016. 28 (5). 263-270.
21. Levar N., van Leeuwen J.M.C., Puts N.A.J., Denys D., van Wingen G.A. GABA concentrations in the anterior cingulate cortex are associated with fear network function and fear recovery in humans. Front. Hum. Neurosci. 2017. 11. 202.
22. Skorzewska A., Wislowska-Stanek A., Lehner M., Turzynska D., Sobolewska A. et al. Corticotropin releasing factor receptor 1 antagonist differentially inhibits freezing behavior and changes gamma-aminobutyric acidergic activity in the amygdala in low- and high-anxiety rats. J. Physiol. Pharmacol. 2017. 68 (1). 35-46.
23. Szczepanska-Sadowska E., Cudnoch-Jedrzejewska A., Ufnal M., Zera T. Brain and cardiovascular diseases. common neurogenic background of cardiovascular, metabolic and inflammatory diseases. J. Physiol. Pharmacol. 2010. 61 (5). 509-521.
24. Campos A.C., Fogaça M.V., Scarante F.F., Joca S.R.L., Sales A.J. et al. Plastic and neuroprotective mechanisms involved in the therapeutic effects of cannabidiol in psychiatric disorders. Front. Pharmacol. 2017. 8. 269.
25. Zhu Z., Wang G., Ma K., Cui S., Wang J.H. GABAergic neurons in nucleus accumbens are correlated to resilience and vulnerability to chronic stress for major depression. Oncotarget. 2017. 38 (22). 35933-35945.
26. Vaiva G., Thomas P., Ducrocq F., Fontaine M., Boss V. et al. Low posttrauma GABA plasma levels as a predictive factor in the development of acute posttraumatic stress disorder. Biol. Psychiatry. 2004. 55 (3). 250-254.
27. Vaiva G., Boss V., Ducrocq F., Fontaine M., Devos P. et al. Relationship between posttrauma GABA plasma levels and PTSD at 1-year follow-up. Am. J. Psychiatr. 2006. 163 (8). 1446-1448.
28. Porges E.C., Woods A.J., Edden R.A., Puts N.A., Harris A.D. et al. Frontal gamma-aminobutyric acid concentrations are associa-ted with cognitive performance in older adults. Biol. Psychiatry Cogn. Neurosci Neuroimaging. 2016. 2 (1). 38-44.
29. Contestabile A., Magara S., Cancedda L. The GABAergic Hypothesis for Cognitive Disabilities in Down Syndrome. Front. Cell. Neurosci. 2017. 11. 54.
30. Kim Y.S., Yoon B.E. Altered GABAergic signaling in brain disease at various stages of life. Exp. Neurobiol. 2017. 26 (3). 122-131.
31. Hayashi T., Nagai K. Complete cure of epilepsy in dogs following intraventricular injection of 4-amino-3-hydroxybutyric acid. Prensa Med. Argent. 1964. 51. 286.
32. Tadokoro Y., Han K., Okada T., Kank, Hirano C. Clinical use of gamma-amino-beta-hydroxybutyric acid in epilepsy, with special reference to its effect on brain waves. Sogo Igaku. 1962. 19. 462-465.
33. Yamamoto S., Haraoka T., Hashimoto Y. On the therapeutic effectiveness of gamma-aminobutyric acid and gamma-amino-beta-hydroxybutyric acid for cerebrovascular disorders and hypertension. Sogo Igaku. 1962. 19. 445-447.
34. Colucci D’Amato F. Therapeutic effect of gabob in a group of patients with character disorders. Osp. Psichiatr. 1968. 36 (3). 478-484.
35. Mille T., Scamoni C., Presazzi A. Clinical and electroencepha-lographic studies of Gabob-Diazepam effects on young children with behavior disorders. Minerva Pediatr. 1973. 25 (13). 593-603.
36. Amore F., Cavazzuti G.B. Clinical and statistical evaluation of GABOB in behavior disorders in young children. Minerva Med. 1971. 62 (29). 1503-1513.
37. Heinze H. Long-term treatment with psychoverlan in children and adolescents with behavior disorders. Fortschr. Med. 1978. 24. 96 (32).
38. Vitamin B6. Micronutrient Information Center, Linus Pauling Institute, Oregon State University, Corvallis, OR, USA, 2017.
39. Technical Information (fact sheet) of Gamalate B6.
40. Espadaler Medina J.M., Pujol J., Balcells M., Jubert-Gruart J. Clinical experience with a new medicamental association GB6 in neurologic practice. MMW (spanished). 1996. 1. 40-57.
41. FolchCamarasa L., Folch L., Folch J. Experiences carried out to determine the influence of Gamalate B6 on the thought automatisms in mental defective patients. Rapports de Psicologia y Psiquiatria Pediátricas. 1968. 10. 1-6.
42. Knobel M. Clinical experience with Gamalate B6 in some infantile mental deficiencies. 1972 (Unpublished data).
43. Vendrell J., Amorós M.C., Vendrell D.P. An approach to the study of evolution of speech disturbances in children, on combining the logotherapeutic treatment with a drug association (GB6). N. Engl. J. Med. (spanished). 1973. 7 (82). 51-61.
44. Espadaler J.M. Our experience in the treatment of minimum cerebral dysfunctions with GB6. Med. Klin. (spanish edition). 1982. 249. 39-44.
45. Foch Soler J. Gamalate B6 in paidopsychiatry. Med. Klin. (spanished). 1983. 254. 29-36.
46. Zamora A., Pérez L.M. Magnesium glutamate hydrobromide and GABA as treatment of anxiety. Phronesis. 1990. 11. 5-8.
47. Núñez Sintas D., López-Pousa S. Tension headaches response to medication with GAMALATE-B6. Phronesis. 1990. 12(6). 1-4.
48. Martínez M., Alvarado M., Tagle I., Orrillo E. Gabaergic precursors and neurological learning disorders comparative study of school children in urban-marginal areas of metropolitan Lima. Revista de Neuro-Psiquiatría. 1991. 54. 113-120.
49. Martínez Mendoza M. Gamalate-B6 (G-B6) in the treatment of anxiety. Phronesis. 1992. 13. 33-38.
50. Novell R., Aguas S., Franco M., Ampudia M., Roig J.M., Gutiérrez J.R. et al. Treatment of behaviour disorders in slight and moderately mentally retarded children. Efficacy and safety of Gamalate B6. Psiquis. 1998. 19 (7). 265-273.
51. López-Pousa S., Lombardia C., Ortega E., Novell R. Efficacy of a GABAergic drug (Gamalate-B6®) on the quality of life of the patients with fibromyalgia. Psiquis. 2002. 23 (1). 27-34.
Печатается в сокращении. Впервые опубликовано в J. Neurol. Neurosurg. 2017. 6 (5). 555696. DOI: 10.19080/OAJNN.2017.06.555696
/64.jpg)
/64_2.jpg)

/66.jpg)
/67.jpg)