Вступ
Синдром хронічної втоми (СХВ) — це поєднання відчуття стійкої стомленості організму пацієнта в цілому і різних соматичних симптомів. Синдром хронічної втоми/міалгічний енцефаломієліт (СХВ/МЕ) можна відрізнити від соматичних та психіатричних порушень при диференціальній діагностиці втоми за такими ознаками: наявність виснажливої втоми тривалістю понад 6 місяців; поєднання когнітивної дисфункції, болю в усьому тілі та сну, який не дає бадьорості та відновлення нормальної функціональності; постнавантажувальна слабкість, коли вплив інших стресорів призводить до загострення симптомів, що розвиваються після такого впливу протягом декількох годин або ввечері. Всесвітня організація охорони здоров’я (ВООЗ) класифікує СХВ/МЕ як неврологічне захворювання. Об’єктивних діагностичних тестів, верифікованих біомаркерів, препаратів або методик, що забезпечують лікування СХВ/МЕ, зараз не існує. Первинними цілями лікування є зняття симптомів та покращення функціональної здатності. Початкове лікування має бути індивідуалізоване та засноване на найбільш виражених скаргах пацієнта [1–3].
Хронічна непередбачувана непрацездатність у пацієнтів із СХВ вимагає істотних змін способу життя: ретельного планування щоденних дій, збереження енергетичних ресурсів для найважливіших завдань, планування періодів відпочинку, щоб запобігти перевтомі і покращити якість сну. За оцінками експертів з різних країн світу, до 30,5 % населення страждає на хронічну втому [4, 5].
СХВ увійшов у номенклатуру Міжнародної класифікації хвороб X перегляду (G93.3), визначено його діагностичні критерії, відомі як критерії Холмса (Holmes). Відповідно до критеріїв Холмса, діагноз цього синдрому встановлюється при поєднанні 2 великих критеріїв і не менше 8 із 11 малих або 6 малих + 2 із 3 фізикальних (об’єктивних) критеріїв. До великих критеріїв СХВ відносять такі:
1. Уперше розвивається стомленість, що триває 6 місяців і супроводжується зниженням фізичної активності більше ніж на 50 відсотків від початкового рівня.
2. Відсутність причин, які могли обумовити стомленість.
До переліку малих критеріїв увійшли наведені далі симптоми, які з’явились одночасно або після появи стомленості і тривають не менше ніж 6 місяців:
1. Лихоманка з температурою тіла 37,5–38,6 °С.
2. Першіння в горлі.
3. Болісні шийні або пахвові лімфовузли.
4. Генералізована м’язова слабкість.
5. Біль у м’язах.
6. Стомленість після фізичного навантаження, яка триває 24 години.
7. Головний біль.
8. Мігруючі артралгії.
9. Психоневрологічні скарги (фотофобія, скороминуща скотома, забудькуватість, велика дратівливість, дезорієнтування, утруднення мислення, труднощі у концентрації уваги або депресія).
10. Погіршення сну.
11. Гострий розвиток симптомів протягом кількох годин або днів.
До фізикальних ознак, які можуть бути констатовані лікарем, але відзначаються не менше ніж 2 рази на місяць, віднесені:
1. Лихоманка 37,5–38,6 °С.
2. Неексудативний фарингіт.
3. Пальпуються шийні або пахвові лімфовузли діаметром до 2 см.
Провідний симптом СХВ — виснажлива стомленість, що триває не менше ніж 6 місяців, при обов’язковому виключенні органічних захворювань, що можуть її спричинювати. Серед цих органічних захворювань необхідно виключити: хронічні запальні захворювання (саркоїдоз, гепатит тощо), злоякісні пухлини, автоімунні захворювання, хронічні інфекції, ендокринні розлади, нервово-м’язові хвороби, хронічні захворювання органів кровообігу, дихання, нирок, шлунково-кишкового тракту, кровотворних органів [6–9].
Ми живемо у нову епоху — в умовах глобальної пандемії коронавірусної інфекції SARS-CoV-2 (COVID-19). COVID-19 — це інфекційне захворювання з тяжким гострим респіраторним синдромом, яке характеризується переважно пневмонією з подальшою тяжкою гіпоксемічною дихальною недостатністю. Лише через кілька місяців від початку пандемії клініцисти звернули увагу на виникнення неврологічних симптомів у пацієнтів з COVID-19. Хоча багато з них були просто симптомами, які зазвичай спостерігаються при гарячкових захворюваннях (головний біль, нездужання, міалгія), у літературі почали з’являтися дані про значні неврологічні розлади, що розвиваються внаслідок COVID-19, включаючи порушення свідомості, імунологічно опосередковані неврологічні захворювання та цереброваскулярні ураження [10]. Коронавірус SARS-CoV-2 має нейротоксичну дію, призводить до пошкодження центральних і периферичних структур нервової системи. Механізм пошкодження нервових клітин реалізується через альтерацію судин та проникнення вірусу через гематоенцефалічний бар’єр і надалі — через вироблення цитокінів, які можуть впливати на функцію нейронів, що призводить до цитокінової хвороби (цитокінового шторму) та енцефалопатії при COVID-19 [11]. Також важливо відмітити, що нейрозапалення та тривала гіпоксія внаслідок запалення легенів можуть сприяти нервово-психічним розладам та когнітивним порушенням. Нейрозапалення завжди було важливою особливістю наростання нейродегенеративних розладів та психічних патологій, таких як гострий психоз, шизофренія, депресивні стани тощо. Встановлено, що COVID-19 найчастіше призводить саме до опосередкованих неврологічних пошкоджень: гіпоксичної травми головного мозку та імунообумовленого ураження ЦНС [12].
У міру розвитку пандемії та отримання результатів клінічних випробувань стало очевидним, що значний тягар захворюваності, спричиненої коронавірусом, походить не від самого збудника інфекції, а від реакції організму пацієнта на інфекційний процес, причому імуномодулюючі втручання показують значну користь для виживання порівняно з помірними ефектами від застосування противірусних засобів [13].SARS-CoV-2, як і інші тригери СХВ (вірусні та невірусні), вважається фізіологічно сильним фактором впливу, який може бути спрямований на ініціацію стресу в мозку — паравентрикулярне ядро гіпоталамуса (PVN). Передбачається, що медіатори запалення, які вивільняються в місці інфікування COVID-19, можуть передаватися як стресові сигнали через гуморальні та нервові шляхи, які переповнюють цей стрес-центр. У генетично сприйнятливих людей спостерігається перевищення внутрішнього порога стресу, що спричиняє тривалу дисфункцію складної неврологічної схеми гіпоталамуса. У цьому скомпрометованому стані PVN може бути гіперчутливим до широкого спектра постійних фізіологічних стресових факторів життя. Це може призвести до зареєстрованих епізодів нездужання після напруження та більш тяжких рецидивів, які продовжують хворобливий стан. Коли перевищено певний рівень стійкості до стресу, PVN може стати епіцентром індукованої мікроглією активації та нейрозапалення, що вражає гіпоталамус та його проксимальну лімбічну систему, що пояснює спектр зареєстрованих симптомів, подібних до СХВ (рис. 1) [14].Отже, коронавірусна інфекція має доведені механізми шкідливого впливу на нервову систему та імунітет, провокує розвиток постковідного синдрому хронічної втоми, тому пацієнтам, які перенесли COVID-19, необхідно призначати нейропротектори та імунокоригуючі засоби. До препаратів-імуномодуляторів, які підтримують захисні сили організму та мають доведені противірусні властивості, належить комплексний засіб Трилумін, який містить комплекс низькомолекулярних органічних біологічно активних сполук, отриманих із Bacillus subtilis [15]. Тому вивчення можливих перспектив застосування Трилуміну при СХВ є науково і клінічно обґрунтованим.
/37.jpg)
Мета роботи: вивчити ефективність додавання імунокоригуючого засобу Трилумін до комплексної терапії пацієнтів, які перенесли коронавірусну хворобу COVID-19 і мають синдром хронічної втоми на тлі вторинного імунодефіциту.
Матеріали та методи
Для оцінки ефективності комплексної терапії постковідного синдрому хронічної втоми на тлі вторинного імунодефіциту брали до уваги результати клінічних та імунологічних тестів, оцінку якості життя пацієнтів та провели статистичний аналіз.
До групи дослідження були включені 30 пацієнтів віком від 29 до 45 років, які звернулися за медичною допомогою з клінічними проявами СХВ після перенесеної інфекції SARS-CоV-2. Пацієнтам цієї групи було призначено комплексне лікування: ноотропний засіб фенібут (усередину по 1 табл. (250 мг) 3 рази на день, курс 20 днів) та вітамін D3 (усередину по 1 капс. (50 мкг (2000 МО)) на добу впродовж 20 днів), а як додатковий імунокоригуючий препарат — натуральний засіб Трилумін (усередину за 30 хвилин до їди по 1 капсулі (350 мг) двічі на добу, курс 20 днів).
Трилумін містить комплекс низькомолекулярних органічних біологічно активних сполук, отриманих із Bacillus subtilis (10 мг). Препарат справляє імуномодулюючу, противірусну, антибактеріальну, протизапальну дію, знижує інтоксикаційне навантаження. Трилумін підвищує резистентність організму до вірусних і бактеріальних інфекцій, скорочує тривалість захворювання, запобігає розвитку ускладнень, знижує ризик виникнення рецидивів та подовжує періоди ремісії. Прискорює відновлення організму після одужання та знижує частоту захворюваності протягом року. Клінічний досвід застосування Трилуміну показав його високу ефективність, добру переносимість, відсутність токсичності та небажаних побічних ефектів. Трилумін сприяє нормалізації активності лімфоцитів, стимулює поділ та активацію макрофагів, зміцнюючи природні захисні сили організму проти вірусів і бактерій [15].
Фенібут має ноотропну дію: покращує пам’ять, підвищує фізичну та розумову працездатність, помітно зменшує прояви астенії та вазовегетативні симптоми, включаючи головний біль, відчуття тяжкості в голові, покращує біоенергетику мозку. Вітамін D має потужну нейропротекторну дію через низку незалежних механізмів, пов’язаних з індукцією нейротрофінів — важливих факторів для росту та диференціації нервових клітин у периферичній і центральній нервовій системі, виживаності нейронів. Відкриття рецепторів до кальцитріолу на багатьох клітинах імунної системи, а також спроможності мононуклеарних фагоцитів до продукції 1,25(ОН)2D3 стало доказом участі вітаміну D у функціонуванні імунної системи. Основним механізмом протиінфекційної дії вітаміну D є його здатність індукувати утворення в імунних клітинах активних антиінфекційних пептидів, які здатні знищувати патогени. Пацієнтам контрольної групи, яка була порівнянною з групою дослідження, було призначено схему лікування без імунотропного засобу Трилумін — фенібут та вітамін D3 за аналогічною схемою.
У точках контролю до початку лікування, на 12-ту та 22-гу добу після початку лікування оцінювали:
1) наявність або відсутність у пацієнтів таких симптомів, як загальна слабкість, розлади сну, посилення втоми після навантаження, біль у м’язах, головний біль, артралгії, температура вище від 37,5 °С, фарингіт, лімфаденопатія, когнітивні розлади, депресивний стан;
2) показники імунограми та імунорегуляторний індекс (ІРІ). ІРІ є одним із основних лабораторних показників задовільного стану імунної системи та відображає співвідношення CD4+/CD8+ Т-лімфоцитів; у здорових людей абсолютна кількість клітин CD4+ зазвичай становить від 800 до 1050 клітин/мкл, а співвідношення CD4+/CD8+ перевищує 1,0; підрахунок клітин CD4+ та CD8+ також важливий при обстеженні пацієнтів з різними видами імунодефіцитів, методика підрахунку зважає на поділ лімфоцитів на підкласи на основі імунної функції (експресії CD4+ та CD8+ антигенів) за допомогою проточної цитометрії;
3) якість життя пацієнтів за анкетою EuroQoL-5D. Опитувальник EuroQoL-5D є загальноприйнятим методом визначення якості життя пацієнтів і складається із двох субшкал: 1 — загальний стан пацієнта та зміни у повсякденній активності, пов’язані із хворобою; 2 — зміна загального стану пацієнта внаслідок лікування; перша підшкала складається із п’яти запитань, які стосуються 5 різних сфер життєдіяльності (пересування, самообслуговування, активність у щоденному житті, больовий синдром, загальний настрій); пацієнт обирає один із трьох варіантів відповідей (бали 0–2), які наведені у кожному із п’яти розділів. Індекс EuroQoL-5D визначається як сума балів у всіх 5 розділах [16, 17]. Статистична обробка даних проводилася із використанням спеціальної програми STATA 12.
Результати та обговорення
Клінічні прояви синдрому хронічної втоми у пацієнтів досліджуваної і контрольної груп були схожими: загальна слабкість, розлади сну, посилення втоми після навантаження, біль у м’язах, головний біль, артралгії, підвищення температури, фарингіт, лімфаденопатія, когнітивні розлади та депресія. В обох групах хворих ми спостерігали стійкий регрес клінічної симптоматики СХВ упродовж усього періоду лікування, однак слід відмітити, що саме у групі дослідження різні симптоми СХВ минали раніше та кількість їх була відносно меншою після закінчення терпії.
Важливо підкреслити, що у групі дослідження найбільш значущий симптом СХВ — загальна слабкість — був зафіксований у 21 (70 %) пацієнта на 12-й день спостереження, а на 22-й день — у 6 хворих (20 %) (табл. 1, 2).
/38.jpg)
Натомість у групі контролю, незважаючи на загальну позитивну динаміку регресу клінічної симптоматики СХВ, загальна слабкість залишалася у 24 (80 %) пацієнтів на 12-й день та у 13 (43,3 %) після закінчення лікування (рис. 2). Це свідчить про те, що за критерієм елімінації головного симптому СХВ кращою виявилася стратегія терапії у групі дослідження. У досліджуваній групі пацієнтів до початку лікування cпостерігалися знижені (відносно нормальних) імунологічні показники, а також відносно низький імунорегуляторний індекс — 0,73 у середньому значенні; аналогічна картина в імунограмі була зафіксована і в контрольній групі. Але слід відмітити, що більш виражена тенденція до відновлення клітинного імунітету спостерігалася у групі дослідження: це нормалізація абсолютної кількості та питомої ваги клітин CD3, CD4, CD8, CD16, CD22. Доцільним буде відмітити, що в обох групах спостереження впродовж курсу комплексної терапії нормалізувалися показники антитіл, зокрема знижувався титр противірусних IgM, та циркулюючих імунних комплексів (ЦІК) (табл. 3, 4).
/39.jpg)
Також слід відзначити, що середнє значення імунорегуляторного індексу на 22-й день після початку лікування було 1,02 у групі дослідження, а в групі порівняння — 0,87 (рис. 3).
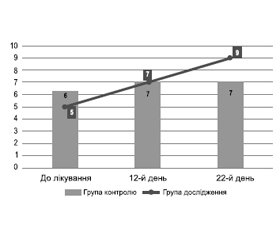
Показовим виявилося порівняння показників якості життя пацієнтів у точках моніторингу. Необхідно відзначити, що оцінка якості життя за опитувальником EuroQoL-5D продемонструвала, що у групі дослідження пацієнти суб’єктивно відмічали відчутне поліпшення свого стану та здатності до щоденної активності, яка була кращою, ніж у групі контролю (рис. 4).
У динаміці спостереження саме у групі дослідження в точках моніторингу на 12-й та 22-й день відзначався більш виражений регрес клінічної симптоматики, спостерігалася тенденція до повноцінної нормалізації показників імунограми, зокрема імунорегуляторного індексу, а також фіксувалися кращі показники якості життя хворих.
Отримані результати ведення постковідного СХВ на тлі вторинного імунодефіциту дозволяють обґрунтовано припустити, що доповнення схеми менеджменту цього захворювання імунокоригуючим компонентом Трилумін реалізує програму комплексної реабілітації пацієнтів: призводить до зменшення інтенсивності клінічних проявів, нормалізації імунологічних показників, відновлення фізичної та розумової активності пацієнтів.
Висновки
1. Коронавірусна інфекція має доведені механізми шкідливого впливу на нервову систему та імунітет, провокує розвиток постковідного синдрому хронічної втоми, тому пацієнтам, які перенесли COVID-19, необхідно призначати засоби нейропротекторної та імунокоригуючої дії.
2. Застосування Трилуміну як додаткового засобу в менеджменті пацієнтів із постковідним синдромом хронічної втоми на тлі вторинного імунодефіциту порівняно з групою контролю призвело до кращої нормалізації імунологічних показників, зокрема імунорегуляторного індексу.
3. Важливо відмітити, що натуральний засіб Трилумін має м’який імунокоригуючий ефект, тобто діє за принципом «patient friendly» (доброзичливо до пацієнта); іншими словами, він не виснажує імунний ресурс організму, не викликає різкого зростання імунної активності клітин, а здатен сприяти поступовій гармонізації імунної відповіді, що є життєво важливим для пацієнтів з постковідним синдромом.
4. У групі пацієнтів, у якій до схеми терапії СХВ як імунокоригуючий засіб був доданий Трилумін, порівняно з референтною групою спостерігалася більш виражена динаміка регресу клінічної симптоматики, а результати опитування за анкетою EuroQoL-5D продемонстрували краще відновлення якості життя пацієнтів.
5. Зважаючи на результати даної роботи, можна обґрунтовано рекомендувати комплексний засіб Трилумін для додавання до схеми менеджменту пацієнтів, які перенесли коронавірусну хворобу COVID-19 і мають постковідний синдром хронічної втоми на тлі вторинного імунодефіциту.
Конфлікт інтересів. Не заявлений.
Отримано/Received 17.01.2022
Рецензовано/Revised 31.01.2022
Прийнято до друку/Accepted 04.02.2022
Список литературы
1. Avellaneda Fernández A., Pérez Martín A., Izquierdo Martínez M., et al. Chronic fatigue syndrome: aetiology, diagnosis and treatment. BMC Psychiatry. 2009. 9 Suppl. 1 (Suppl. 1). S1. Published 2009 Oct 23. doi: 10.1186/1471-244X-9-S1-S1.
2. Castro-Marrero J., Sáez-Francàs N., Santillo D., Alegre J. Treatment and management of chronic fatigue syndrome/myalgic encephalomyelitis: all roads lead to Rome. Br. J. Pharmacol. 2017. 174(5). 345-369. doi: 10.1111/bph.13702.
3. Noor N., Urits I., Degueure A., Rando L., Kata V., Cornett E.M., et al. A Comprehensive Update of the Current Understan-ding of Chronic Fatigue Syndrome. Anesth. Pain Med. 2021 Jun 26. 11(3). e113629. doi: 10.5812/aapm.113629. PMID: 34540633; PMCID: PMC8438707.
4. Sharpe M., Chalder T., White P.D. Evidence-Based Care for People with Chronic Fatigue Syndrome and Myalgic Encephalomyelitis. J. Gen. Intern. Med. 2021 Nov 17. doi: 10.1007/s11606-021-07188-4. Epub ahead of print. PMID: 34791590.
5. Natelson B.H., Haghighi M.H., Ponzio N.M. Evidence for the presence of immune dysfunction in chronic fatigue syndrome. Clin. Diagn. Lab. Immunol. 2002. 9(4). 747-752. doi: 10.1128/cdli.9.4.747-752.2002.
6. Arnett S.V., Alleva L.M., Korossy-Horwood R., Clark I.A. Chronic fatigue syndrome — a neuroimmunological model. Med. Hypotheses. 2011 Jul. 77(1). 77-83. doi: 10.1016/j.mehy.2011.03.030. Epub 2011 Apr 6. PMID: 21474251.
7. Bansal R.A., Tadros S., Bansal A.S. The presence of overlapping quality of life symptoms in primary antibody deficiency (PAD) and chronic fatigue syndrome (CFS). Allergy Asthma Clin. Immunol. 2020. 16. 21. Published 2020 Mar 30. doi: 10.1186/s13223-020-0417-3.
8. Roberts D. Chronic fatigue syndrome and quality of life. Patient Relat. Outcome Meas. 2018. 9. 253-262. Published 2018 Aug 1. doi: 10.2147/PROM.S155642.
9. Mensah F.K.F., Bansal A.S., Ford B., Cambridge G. Chronic fatigue syndrome and the immune system: Where are we now? Neurophysiol. Clin. 2017 Apr;. 47(2). 131-138. doi: 10.1016/j.neucli.2017.02.002. Epub 2017 Apr 12. PMID: 28410877.
10. Wildwing T., Holt N. The neurological symptoms of COVID-19: a systematic overview of systematic reviews, comparison with other neurological conditions and implications for healthcare services. Ther. Adv. Chronic Dis. 2021. 12. 2040622320976979. Published 2021 Jan 28. doi: 10.1177/2040622320976979.
11. Iadecola C., Anrather J., Kamel H. Effects of COVID-19 on the Nervous System. Cell. 2020. 183(1). 16-27.e1. doi: 10.1016/j.cell.2020.08.028.
12. Tu H., Tu S., Gao S., Shao A., Sheng J. The epidemiological and clinical features of COVID-19 and lessons from this global infectious public health event. J. Infect. 2020.
13. Cosentino G., Todisco M., Hota N., Della Porta G., Morbini P., Tassorelli C., Pisani A. Neuropathological findings from COVID-19 patients with neurological symptoms argue against a direct brain invasion of SARS-CoV-2: A critical systematic review. Eur. J. Neurol. 2021 Nov. 28(11). 3856-3865. doi: 10.1111/ene.15045. Epub 2021 Aug 17. PMID: 34339563; PMCID: PMC8444743.
14. Mackay A. A Paradigm for Post-COVID-19 Fatigue Syndrome Analogous to ME/CFS. Front Neurol. 2021. 12. 701419. Published 2021 Aug 2. doi: 10.3389/fneur.2021.701419.
15. Dyudyun A.D. Innovative approaches to treatment of urogenital infections. Medical aspects of women’s health. 2019. 4–5 (125–126). 60-66 (in Ukrainian).
16. Oliveira J.S., Hayes A. Clinimetrics: The EuroQol-5 Dimension (EQ-5D). J. Physiother. 2020 Apr. 66(2). 133. doi: 10.1016/j.jphys.2020.02.012. Epub 2020 Apr 11. PMID: 32291225.
17. Fisk J.D., Ritvo P.G., Ross L., et al. Measuring the functional impact of fatigue: initial validation of the fatigue impact scale. Clinical Infectious Diseases. 1994. 1. 79-83.
/41.jpg)

/37.jpg)
/38.jpg)
/39.jpg)
/40.jpg)