Международный эндокринологический журнал Том 20, №4, 2024
Вернуться к номеру
Ефективність застосування комбінації фіксованих доз метформіну й глімепіриду у хворих на цукровий діабет 2-го типу
Авторы: Паньків В.І.
Український науково-практичний центр ендокринної хірургії, трансплантації ендокринних органів і тканин МОЗ України, м. Київ, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
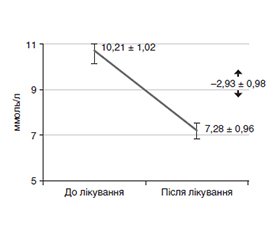
Актуальність. Доведено, що монотерапія цукрового діабету 2-го типу (ЦД2) ефективна лише упродовж обмеженого часу. При цьому важливою складовою успішного менеджменту ЦД2 залишається раціональність комбінацій лікарських засобів. У цьому контексті, з огляду на складний багатофакторний патогенез ЦД2, оптимальним є вплив на різні механізми виникнення гіперглікемії. Використання глімепіриду в терапії ЦД2 порівняно з іншими препаратами сульфонілсечовини значно менше стимулює підшлункову залозу, зберігаючи тим самим її ресурс, і не призводить до гіперінсулінемії, а також забезпечує найбільш високий профіль безпеки при найменшому стимулюючому впливі на секрецію інсуліну. Мета дослідження: визначення ефективності й безпеки комбінації метформіну й глімепіриду в умовах застосування в повсякденній клінічній практиці в пацієнтів з ЦД2 з рівнем глікованого гемоглобіну (HbA1c) 8,0–9,0 %. Матеріали та методи. Під спостереженням перебувало 57 хворих на ЦД2. У дослідження було включено 19 чоловіків (середній вік 51,9 ± 6,9 року) і 38 жінок (середній вік 53,9 ± 6,1 року) з ЦД2. Середня тривалість ЦД2 становила 6,3 ± 2,3 року. Пацієнти мали середній ІМТ 30,8 ± 1,2 кг/м2 на момент включення в дослідження. Хворим було призначено фіксовану комбінацію метформіну і глімепіриду (препарат Дуглимакс® 2/500) упродовж 3 місяців 1 або 2 рази на добу. Аналіз ефективності лікування проводили щомісяця й наприкінці лікування. Результати. Середній рівень HbA1c у 57 хворих на ЦД2 становив 8,42 ± 0,19 %, глюкози плазми натще — 10,21 ± 1,02 ммоль/л. Через 3 місяці після початку комбінованого лікування рівень HbA1c вірогідно знизився до 7,25 ± 0,16 % (p < 0,05). Середнє зниження HbA1c після переведення на додаткову терапію метформіном з глімепіридом становило 1,17 ± 0,14 %. Частка пацієнтів, які досягнули рівня HbA1c < 7,5 %, становила через 3 місяці 56,1 % (p < 0,05). Ефективність призначення фіксованої комбінації метформіну й глімепіриду підтверджується і високою часткою пацієнтів, які досягнули показника HbA1c < 7,0 %, — 24,5 % (p < 0,05). Жодного випадку гіпоглікемії чи інших небажаних явищ упродовж усього періоду дослідження зареєстровано не було. Висновки. Терапія фіксованими дозами метформіну й глімепіриду демонструє високу ефективність та безпеку та підвищує прихильність пацієнтів до лікування. Застосування комбінації фіксованих доз метформіну та глімепіриду (Дуглимакс®) вірогідно поліпшує стан вуглеводного обміну у пацієнтів із цукровим діабетом 2-го типу. Така терапія є безпечною завдяки низькому ризику розвитку гіпоглікемічних станів, відсутності побічних ефектів та негативного впливу на масу тіла.
Background. Monotherapy for type 2 diabetes (T2DM) is effective only for a limited time. At the same time, the rationality of drug combinations remains an important component of successful management of T2DM. In this context, given the complex multifactorial pathogenesis of T2DM, it is optimal to influence various mechanisms of hyperglycemia. Compared to other sulfonylurea drugs, the use of glimepiride in the treatment of T2DM stimulates the pancreas significantly less, thus preserving its resource, does not lead to hyperinsulinemia, and also provides the highest safety profile with the least stimulating effect on insulin secretion. The purpose of the study was to determine the effectiveness and safety of the combination of metformin and glimepiride when using in everyday clinical practice for patients with type 2 diabetes with a level of glycated hemoglobin (HbA1c) of 8.0–9.0 %. Materials and methods. Fifty-seven patients with T2DM were included in the study, 19 men (mean age 51.9 ± 6.9 years) and 38 women (mean age 53.9 ± 6.1 years). The average duration of T2DM was 6.3 ± 2.3 years. Patients had an average body mass index of 30.8 ± 1.2 kg/m2 at the time of inclusion in the study. Participants were prescribed a fixed combination of metformin and glimepiride (Duglimax® 2/500) for three months 1 or 2 times a day. Analysis of treatment effectiveness was performed monthly and at the end of treatment. Results. The average level of HbA1c in 57 patients with T2DM was 8.42 ± 0.19 %, fasting plasma glucose was 10.21 ± 1.02 mmol/l. Three months after the start of combined treatment, the HbA1c level significantly decreased to 7.25 ± 0.16 % (p < 0.05). The average reduction in HbA1c after switching to additional metformin and glimepiride therapy was 1.17 ± 0.14 %. The proportion of patients who achieved the level of HbA1c < 7.5 % was 56.1 % after 3 months (p < 0.05). The effectiveness of prescribing a fixed combination of metformin and glimepiride is also confirmed by the high percentage of patients who achieved HbA1c < 7.0 % (24.5 %; p < 0.05). Not a single case of hypoglycemia or other adverse events was registered during the entire study period. Conclusions. Therapy with fixed doses of metformin and glimepiride demonstrates high efficacy and safety and increases patient adherence to treatment. The use of a fixed-dose combination of metformin and glimepiride (Duglimax®) reliably improves the state of carbohydrate metabolism in patients with type 2 diabetes. Such therapy is safe due to the low risk of developing hypoglycemic conditions, the absence of side effects and a negative impact on body weight.
цукровий діабет 2-го типу; лікування; метформін; глімепірид
type 2 diabetes; treatment; metformin; glimepiride
Вступ
Матеріали та методи
Результати
/64.jpg)
/65.jpg)
Обговорення
Висновки
- Weiss T, Iglay K, Gulati T, Rajpathak S, Yang L, Blonde L. Secondary metformin monotherapy failure in individuals with type 2 diabetes mellitus. BMJ Open Diabetes Res Care. 2021 Jun;9(1):e002127. doi: 10.1136/bmjdrc-2021-002127. PMID: 34167954; PMCID: PMC8230991.
- American Diabetes Association Professional Practice Committee. 9. Pharmacologic Approaches to Glycemic Treatment: Standards of Care in Diabetes-2024. Diabetes Care. 2024 Jan 1;47(Suppl 1):S158-S178. doi: 10.2337/dc24-S009. Erratum in: Diabetes Care. 2024 May 02. PMID: 38078590; PMCID: PMC10725810.
- Yu J, Lee SH, Kim MK. Recent Updates to Clinical Practice Guidelines for Diabetes Mellitus. Endocrinol Metab (Seoul). 2022 Feb;37(1):26-37. doi: 10.3803/EnM.2022.105. Epub 2022 Feb 28. PMID: 35255599; PMCID: PMC8901964.
- Marx N, Federici M, Schütt K, Müller-Wieland D, Ajjan RA, Antunes MJ, et al.; ESC Scientific Document Group. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023 Oct 14;44(39):4043-4140. doi: 10.1093/eurheartj/ehad192. Erratum in: Eur Heart J. 2023 Dec 21;44(48):5060. Erratum in: Eur Heart J. 2024 Feb 16;45(7):518. PMID: 37622663.
- Fernandes G, Sawhney B, Hannachi H, Liu J, Wang T, Fu AZ, et al. Distance to glycemic goal at the time of treatment intensification in patients with type 2 diabetes mellitus failing metformin monotherapy in the United States. Curr Med Res Opin. 2020 May;36(5):741-748. doi: 10.1080/03007995.2020.1722623. Epub 2020 Feb 5. PMID: 31990206.
- Xie X, Wu C, Hao Y, Wang T, Yang Y, Cai P, et al. Benefits and risks of drug combination therapy for diabetes mellitus and its complications: a comprehensive review. Front Endocrinol (Lausanne). 2023 Dec 19;14:1301093. doi: 10.3389/fendo.2023.1301093. PMID: 38179301; PMCID: PMC10766371.
- Karki N, Kandel K, Shah K, Prasad P, Khanal J. Combination Therapy in Diabetes Mellitus Patients Attending Outpatient Department in a Tertiary Care Centre: A Descriptive Cross-sectional Study. JNMA J Nepal Med Assoc. 2022 Dec 1;60(256):1016-1020. doi: 10.31729/jnma.7642. PMID: 36705114; PMCID: PMC9795118.
- Piya MK, Hocking S. Challenges in achieving racial and ethnic health equity in type 2 diabetes: access to newer medications. Lancet Reg Health Am. 2024 May 23;34:100784. doi: 10.1016/j.lana.2024.100784. PMID: 38817955; PMCID: PMC11137501.
- Samson SL, Vellanki P, Blonde L, Christofides EA, Galindo RJ, Hirsch IB, et al. American Association of Clinical Endocrinology Consensus Statement: Comprehensive Type 2 Diabetes Management Algorithm — 2023 Update. Endocr Pract. 2023 May;29(5):305-340. doi: 10.1016/j.eprac.2023.02.001. PMID: 37150579.
- Borse SP, Chhipa AS, Sharma V, Singh DP, Nivsarkar M. Management of Type 2 Diabetes: Current Strategies, Unfocussed Aspects, Challenges, and Alternatives. Med Princ Pract. 2021;30(2):109-121. doi: 10.1159/000511002. Epub 2020 Aug 20. PMID: 32818934; PMCID: PMC8114074.
- Davies MJ, Aroda VR, Collins BS, Gabbay RA, Green J, Maruthur NM, et al. Management of Hyperglycemia in Type 2 Diabetes, 2022. A Consensus Report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022 Nov 1;45(11):2753-2786. doi: 10.2337/dci22-0034. PMID: 36148880; PMCID: PMC10008140.
- Olomu A, Kelly-Blake K, Hart-Davidson W, Gardiner J, Luo Z, Heisler M, et al. Improving diabetic patients' adherence to treatment and prevention of cardiovascular disease (Office Guidelines Applied to Practice-IMPACT Study) — a cluster randomized controlled effectiveness trial. Trials. 2022 Aug 15;23(1):659. doi: 10.1186/s13063-022-06581-6. PMID: 35971135; PMCID: PMC9376908.
- Abdul-Ghani M, DeFronzo RA. Personalized approach for type 2 diabetes pharmacotherapy: where are we and where do we need to be? Expert Opin Pharmacother. 2021 Nov;22(16):2113-2125. doi: 10.1080/14656566.2021.1967319. Epub 2021 Aug 26. PMID: 34435523.
- Cai X, Gao X, Yang W, Han X, Ji L. Efficacy and Safety of Initial Combination Therapy in Treatment-Naïve Type 2 Diabetes Patients: A Systematic Review and Meta-analysis. Diabetes Ther. 2018 Oct;9(5):1995-2014. doi: 10.1007/s13300-018-0493-2. Epub 2018 Aug 28. PMID: 30155646; PMCID: PMC6167297.
- Hwang YC, Kang M, Ahn CW, Park JS, Baik SH, Chung DJ, et al. Efficacy and safety of glimepiride/metformin sustained release once daily vs. glimepiride/metformin twice daily in patients with type 2 diabetes. Int J Clin Pract. 2013 Mar;67(3):236-43. doi: 10.1111/ijcp.12071. Epub 2013 Jan 22. PMID: 23336668.
- Melikian C, White TJ, Vanderplas A, et al. Adherence to oral antidiabetic therapy in a managed care organization: A comparison of monotherapy, combination therapy, and fixed-dose combination therapy. Clinical Therapeutics. 2002;24(3):460-467. https://doi.org/10.1016/S0149-2918(02)85047-0.