Журнал «Здоровье ребенка» 2 (23) 2010
Вернуться к номеру
Подходы к лечению и реабилитации часто и длительно болеющих респираторными заболеваниями детей, проживающих в доме ребенка
Авторы: Юлиш Е.И., Балычевцева И.В., Висягин В.Б., Кривущев Б.И., Гадецкая С.Г., Ярошенко С.Я., Лютова Т.А., Щур Н.В., Донецкий национальный медицинский университет им. М. Горького, Областной дом ребенка «Малютка», г. Донецк
Рубрики: Педиатрия/Неонатология
Версия для печати
Большинство работ, касающихся состояния здоровья воспитанников домов ребенка, освещают подходы к их социально-психологической реабилитации. Однако более 80 % этих детей относятся к группе часто и длительно болеющих респираторными заболеваниями. В данной работе проведен анализ причин высокой заболеваемости ОРВИ у воспитанников домов ребенка, на основании которого определен наиболее рациональный подход к их терапии и реабилитации.
Дом ребенка, часто болеющие дети, ОРВИ, лечение.
Согласно статистике, частота заболеваемости ОРВИ в течение всего периода раннего возраста у воспитанников домов ребенка выше, чем у детей, воспитывающихся в семье (250,0 и 186,1 случая на 100 детей соответственно). При этом среди воспитанников домов ребенка отмечается более высокий показатель числа часто болеющих детей (ЧБД) первого года жизни (22,5 и 8,8 % соответственно).
Большинство воспитанников домов ребенка имеют II группу здоровья; значителен удельный вес детей, имеющих III–V группы здоровья [1]. Общей возрастной закономерностью у воспитанников домов ребенка является увеличение к трем годам числа детей с III группой здоровья и уменьшение числа детей со II группой здоровья, т.е. увеличение с возрастом числа хронических заболеваний, переход функциональных нарушений в хроническую патологию [2].
К эпидемиологическим особенностям острых респираторных инфекций (ОРИ) в домах ребенка относятся быстрое распространение возбудителей и длительная их циркуляция в коллективе. Это, в свою очередь, повышает риск супер- и реинфицирования и ведет к более длительному, затяжному течению ОРИ и, на фоне функциональной напряженности систем адаптации, к более частому возникновению осложнений [3].
Поэтому большинство детей в домах ребенка входят в группу часто болеющих, более склонны к хроническому течению заболеваний; у них чаще, чем в общей популяции, выявляются кожные и респираторные аллергозы, отклонения физического развития [4].
Средняя продолжительность неосложненных форм ОРИ у детей (13,11 ± 4,23 дня) из дома ребенка почти в 3 раза превышает аналогичный показатель у детей из семей (4,97 ± 0,54 дня), а осложнения (отиты, синуситы, бронхиты, пневмонии) развиваются в 2,8 раза чаще — в 56,9 % случаев. Практически у всех часто и длительно болеющих детей из дома ребенка выявляется иммунный дисбаланс (у детей данной категории из семей — не более чем у 20 %), у 36,7 % из них гипер- или гипоплазия тимуса [5–7].
Множественность неблагоприятных факторов, воздействующих на воспитанников домов ребенка, усугубляется инфицированностью их персистирующими агентами (хламидиями, микоплазмами, цитомегаловирусом, вирусом Эпштейна — Барр, вирусами простого герпеса 1-го и 2-го типа и др.), наблюдающейся у 74,6 % детей, причем активное течение инфекций выявляется у более чем 80 % детей этой группы [8–11].
Кроме предрасположенности к частым заболеваниям, свое влияние оказывает тот факт, что у часто болеющих детей повторные инфекции часто вызываются бактериями Haemophilus influenzae (наиболее часто тип b), Streptococcus pneumoniae, S.pyogenes, Staphylococcus aureus, Moraxella catarrhali s; вирусами (преимущественно риновирусами, респираторно-синцитиальным вирусом, вирусами гриппа, парагриппа, аденовирусами); возбудителями семейств Chlamydia и Mycoplasma, особенно Ch.pneumoniae и M.pneumoniae . Многие из этих возбудителей циркулируют в общей популяции круглогодично и вызывают заболевания вне зависимости от сезона [12]. При обследовании ЧБД обнаруживается интенсивная микробная колонизация слизистых оболочек грибами рода Candida, энтеробактериями и даже синегнойной палочкой [13–16]. В носовых пазухах, лакунах небных и глоточных миндалин нередко обнаруживаются анаэробы. Выраженные нарушения микробиоценоза носоглотки снижают резистентность к патогенным возбудителям, поддерживают длительный воспалительный процесс, способствуют нарушению целостности эпителиального барьера и развитию хронической интоксикации.
Вирусологическое исследование смывов из носоглотки обнаруживает значительную инфицированность часто болеющих респираторными заболеваниями детей респираторными вирусами и герпесвирусами [15].
Столь высокая заболеваемость воспитанников домов ребенка, 80 % которых относятся к группе часто и длительно болеющих, диктует необходимость создания специальных методов реабилитации для этой группы детей.
Относясь ко II группе здоровья (с отягощенным биологическим анамнезом, функциональными и морфологическими особенностями), часто болеющие дети имеют повышенный риск хронических заболеваний. Предупреждение хронизации заболеваний определяет необходимость проведения комплекса мероприятий детям этой группы как из семей, так, по возможности, и из домов ребенка по следующим направлениям [3]:
— снижение антигенного воздействия, санация местных очагов хронической (в том числе и персистирующей) инфекции и повышение резистентности организма в целом; проводятся в период клинической ремиссии;
— этиопатогенетическое лечение ОРИ в острый период (противовирусная, противовоспалительная, симптоматическая терапия);
— иммунопрофилактика и иммунореабилитация.
Реализация вышеуказанного комплекса включает:
— грудное вскармливание, индивидуальную диету;
— рациональный режим дня и питания;
— здоровый образ жизни семьи (в том числе полный отказ от курения в присутствии ребенка или в помещении, где он находится);
— закаливание;
— общеукрепляющую и лечебную физкультуру;
— поливитаминные средства;
— терапию антиоксидантами (витамины Е и С);
— санацию очагов хронической инфекции;
— восстановление микробиоценоза кожи, открытых и закрытых слизистых, кишечника;
— лечение сопутствующей патологии (желчевыводящей системы и кишечника, глистных инвазий);
— для детей со склонностью к аллергии–консультации аллерголога и аллергологическое обследование и лечение;
— физиотерапевтические методы: ультрафиолетовое облучение, лазеротерапию, общий и точечный массаж;
— своевременную вакцинацию;
— медикаментозную терапию (иммунокоррекцию);
— адекватную рациональную антибактериальную, противовирусную, противогрибковую терапию в остром периоде инфекций по показаниям.
Повышение общей реактивности организма часто болеющих детей — важный и общепризнанный раздел оздоровительных мероприятий.
Одним из важных мероприятий является рациональный режим дня. В связи с тем что у детей из группы часто и длительно болеющих (ЧДБ) наблюдаются функциональные нарушения со стороны центральной и вегетативной нервной системы [4], необходимо исключить переутомление и перевозбуждение. Целесообразно увеличить продолжительность сна на 1–1,5 часа. Обязательным является дневной сон или отдых. При наличии нарушений сна, других астено-невротических расстройств показаны прогулки на свежем воздухе перед сном, а также прием седативных трав (типа пустырника, валерианы).
Питание часто болеющих детей должно быть разнообразным, содержащим оптимальное количество белков, жиров, углеводов, минеральных солей (Zn, Se, Cu, Co) и витаминов.
Учитывая, что у детей из группы ЧДБ нередко незрелость системы терморегуляции определяет пониженную устойчивость к изменяющимся факторам внешней среды, актуальными являются методы рационального закаливания и физического воспитания. Систематическое контрастное воздушное или водное закаливание сопровождается повышением устойчивости организма к температурным колебаниям окружающей среды и повышением иммунобиологической реактивности организма. Закаливающие процедуры необходимо сочетать с проведением гимнастики и массажа грудной клетки, что повышает функциональную активность дыхательной системы.
В оздоровлении часто болеющих детей важное значение имеет систематическое проведение специальных комплексов лечебной физкультуры, направленных на обеспечение хорошего дренажа бронхов и повышение тонуса дыхательной мускулатуры.
Рациональная витаминотерапия — обязательный компонент программ оздоровления детей, часто и длительно болеющих ОРЗ. При инфекционных заболеваниях потребность организма в витаминах резко повышается, что нередко сопровождается развитием относительной витаминной недостаточности. Последняя, в свою очередь, негативно влияет на функциональный статус иммунной системы, снижает резистентность организма к инфекциям и способствует развитию аллергических состояний [17].
В курс реабилитации ЧДБ детей возможно включение адаптогенов и биогенных стимуляторов — веществ, повышающих общую сопротивляемость организма.
Учитывая нарушение микробиоценоза носа, придаточных пазух и ротоглотки у этих детей, местная терапия направлена на санацию хронических очагов инфекции, восстановление целостности слизистых оболочек, подавление хронического воспаления, что в конечном счете обеспечивает снижение антигенной нагрузки на иммунную систему организма ребенка. Местная терапия включает: орошения слизистых оболочек солевыми растворами (аква марис, хьюмер, физиомер, салин и др.), использование бактерицидных пастилок (стрепсилс, бронхикум, фарингосепт), полоскание зева (у детей старше 4–5 лет) антисептическими растворами (раствор фурацилина, отвары ромашки, зверобоя и т.д.), промывание носовых ходов, физиотерапевтические методы (УФО на миндалины, УВЧ, СВЧ и гелий-неоновое лазерное облучение на регионарные лимфоузлы, ингаляции с морской водой, маслом эвкалипта и т.д.), аспирация содержимого лакун небных миндалин, внутрилакунарное введение антисептических паст, промывание лакун раствором протефлазида. Особое значение имеет проведение местного антибактериального лечения.
Учитывая отклонения в системе иммунитета, которые выявляются у большинства ЧДБ детей, повышение общей реактивности организма является важным и общепризнанным разделом оздоровительных мероприятий. При этом особые надежды возлагаются на методы иммунореабилитации [18, 19]. Иммунокоррекция рассматривается в качестве одного из основных компонентов патогенетической терапии рецидивирующих респираторных инфекций, а также используется для профилактики частых ОРЗ.
В настоящее время для иммунокоррекции предлагается большое количество иммунотропных лекарственных средств. Это бактериальные препараты, природные и рекомбинантные интерфероны, индукторы интерфероногенеза, препараты тимуса, костного мозга и другие. При выборе схемы иммунокорригирующей терапии в каждой конкретной клинической ситуации следует учитывать индивидуальные особенности организма ребенка.
Согласно современным данным, в первую очередь необходимо использовать иммуномодуляторы, действующие на клетки моноцитарно-макрофагальной системы, с целью активизации специфических и неспецифических факторов защиты организма.
Специфическая активная иммунизация против наиболее распространенных возбудителей острых респираторных заболеваний выгодно отличается от неспецифической иммуностимуляции своей целенаправленностью и эффективностью.
К сожалению, возможности наиболее высокоэффективного метода профилактики инфекционных заболеваний — вакцинации — в большинстве случаев респираторных заболеваний ограниченны. Существуют вакцины против пневмококка, гемофильной палочки и др., ежегодно появляются новые вакцины против вируса гриппа, стафилококка. Но против большинства возбудителей вакцин не существует, не говоря уж об отсутствии поливакцин с антигенами основных возбудителей респираторных инфекций. Поэтому большое значение имеют так называемые вакциноподобные препараты, действие которых направлено на создание специфического иммунитета против конкретного возбудителя [3].
Учитывая микробный пейзаж ротоглотки у ЧДБ детей, наиболее оправданно использование бактериальных лизатов с целью увеличения продукции специфических антител, а также стимуляции неспецифических факторов защиты (секреторных IgA, цитокинов, NK-клеток, клеток макрофагально-фагоцитарной системы и др.).
По современным данным, лимфоглоточное кольцо является одним из основных органов, обеспечивающих организм информацией об антигенном составе окружающего мира в постнатальный период жизни человека. Четкий дозозависимый характер иммунного ответа на разнообразные ситуации структурами лимфоглоточного кольца с автономной или генерализированной реакцией позволяет в настоящее время не только обеспечивать надежную местную защиту от возбудителей, но и формировать общий иммунный ответ.
Теснейшее взаимодействие иммунных образований лимфоглоточного кольца с подобными структурами ЖКТ (пейеровы бляшки, аппендикс и т.д.) дает возможность выбирать различные варианты иммунизации — системную (Бронхомунал, рибомунил) или топическую (ИРС19).
Анализируя действие препаратов микробного происхождения, содержащих липополисахариды грамотрицательных бактерий и мембранные фракции, следует отметить, что основной механизм их действия связан с активирующим влиянием на функциональный статус макрофагов. Данные препараты стимулируют фагоцитоз и таким образом могут влиять на иммунокомпетентные клетки.
Бактериальные лизаты (ИРС19, Бронхомунал) инициируют специфический иммунный ответ на бактериальные антигены, присутствующие в препарате. Комбинированный иммунокорректор рибомунил, сочетая в себе антигенные носители бактерий (рибосомы) и активные неантигенные компоненты бактериальной оболочки (протеогликаны), вызывает такой же эффект.
Использование бактериальных лизатов или бактериальных рибосом обусловливает контакт антигенов наиболее значимых возбудителей ОРЗ с макрофагами, находящимися в слизистых респираторного и желудочно-кишечного тракта, с последующей их презентацией лимфоцитам MALT-системы (лимфоидная ткань, ассоциированная со слизистыми). В результате этого появляются коммитированные клоны В-лимфоцитов, продуцирующие специфические антитела к антигенам возбудителей, содержащихся в бактериальных иммунотропных препаратах. Кроме того, миграция коммитированных В-лимфоцитов в другие лимфоидные образования MALT-системы и последующая их дифференциация в плазмоциты приводят к продукции специфического секреторного IgA и развитию эффективной местной иммунной защиты против основных возбудителей острых респираторных заболеваний [3].
Бактериальные иммуномодулирующие препараты предназначены для стимуляции специфической защиты организма от патогенного воздействия тех микробов, антигенные субстраты которых входят в сос тав препарата. Таким образом, прием бактериальных иммунотропных препаратов имеет вакциноподобное действие, сопровождаясь индукцией специфического ответа как местного, так и системного иммунитета [3].
В педиатрической практике наибольшее распространение получили бактериальные лизаты системного действия. Многочисленными исследованиями показано, что применение Бронхомунала у часто болеющих детей ведет к урежению ОРВИ, снижает вероятность бактериальных осложнений. Так, у больных, получавших Бронхомунал, снижалось число обострений в 4,8 раза, суммарная длительность обострений уменьшалась в 6,3 раза, длительность лечения антибиотиками — в 12 раз. Бронхомунал сокращал сроки лечения инфекций дыхательных путей в среднем на 3,8 дня.
Иммунологические исследования показали, что очевидным противоинфекционным эффектом Бронхомунала является, помимо увеличения уровня специфических антител, и нарастание уровней IgA как в сыворотке крови, так и в секрете дыхательных путей.
Бронхомунал также вызывает активацию клеточного иммунитета (клетки CD3+, CD4+, CD3+HLA-DR+, CD3+CD16+, CD3-СD16+), повышение функциональной активности макрофагов и выработку ряда цитокинов (ИЛ-6, ИЛ-8, ИЛ-2, NAF, g -ИФН). Одновременно происходит увеличение уровня a -интерферона, а также снижение уровней IL-4 , ФНО- a . Повышение уровня IgG усиливает межклеточные взаимодействия макрофагов, киллеров. Результатом является гибель бактериальной инфекции и повышение активности иммунной системы [20–22]. Эти сдвиги, особенно выраженные у детей с бронхиальной астмой и дерматореспираторным синдромом, можно интерпретировать как переключение иммунного ответа Th2-типа на Th1-тип. Как показали клинические наблюдения, дети с аллергией при влючении Бронхомунала в комплексную терапию не только реже болели ОРВИ, но и в меньшей степени были подвержены приступам бронхообструкции [23]. Применение Бронхомунала для профилактики рецидивов хронического бронхита снижает частоту и тяжесть рецидивов, уменьшает случаи госпитализации в 1,43 раза и ее продолжительность в 1,8 раза. У детей с хроническим риносинуситом отмечено снижение частоты рецидивов и тяжести симптомов [20, 22, 24]. У ЧДБ детей при назначении Бронхомунала в 2–3 раза снижается частота ОРЗ, хронического фарингита, бронхита [25, 26].
Целесообразность использования очищенных бактериальных лизатов наиболее частых бактериальных возбудителей респираторных инфекций определяется необходимостью активного раннего формирования иммунного ответа, подготавливающего детей к вхождению в детские коллективы. Известно, что до 30 % таких детей имеют селективный дефицит по IgA, IgG и низкий уровень секреторного IgA во внешних секретах уха, синусов, глотки и носоглотки.
Способность очищенных бактериальных лизатов не только повышать специфический иммунный ответ, но и активизировать неспецифическую защиту позволяет успешно применять их в группе ЧБД, у которых нередко вирусно-бактериальный синергизм приводит к затяжному рецидивному течению с чередованием инфекций верхних и нижних дыхательных путей и среднего уха. Ранняя иммунизация против основных патогенов снижает процент внутричерепных осложнений со стороны околоносовых пазух и уха у детей раннего возраста.
Одни специалисты рекомендуют проводить иммунокорригирующую терапию с учетом ведущей причины предрасположенности к инфекции и «точек приложения» иммунных препаратов [27, 28]. Другие считают, что прицельный подбор иммуномодуляторов на основе клинико-иммунологического обследования ЧБД сегодня, как правило, малореалистичен, а иммунологическое обследование в таких случаях малоинформативно [29]. В большинстве случаев выбор препарата осуществляется эмпирически, по клиническим показаниям. Иммунологическое обследование ЧБД следует проводить главным образом для исключения первичной иммунной недостаточности, при которой эмпирическая иммунотерапия может оказаться неэффективной, а «частые ОРЗ» могут маскировать более серьезные клинические проблемы. Однако все сходятся во мнении, что мобилизация иммунной сопротивляемости ЧБД, даже если заболеваемость в значительной мере обусловлена социально-гигиеническими или другими неиммунными причинами, может дать положительный клинический эффект.
Реабилитация и оздоровление ЧБД требуют планомерного проведения комплекса медико-социальных мероприятий. Рациональное использование средств иммунопрофилактики и фармакотерапии в комплексе с оздоровительными мероприятиями и просвещением семьи, реализация экологических программ должны способствовать решению проблемы часто болеющих детей.
Учитывая гетерогенность развития синдрома частых и длительных респираторных заболеваний у детей, мы согласны с мнением профессора Н.Л. Аряева [27, 28] о необходимости определения четких причин и механизмов развития заболеваний и разработки направленной этиопатогенетической терапии.
Наши наблюдения и данные исследований зарубежных и отечественных авторов [30–36] свидетельствуют об этиологической значимости внутриклеточных персистирующих возбудителей в формировании самостоятельного инфекционного заболевания, а также как фактора, определяющего сдвиги в системах адаптации. В.А. Булгаковой, И.И. Балаболкиным [37] установлено, что между интенсивностью персистенции вирусов у ЧДБ детей и частотой возникновения ОРИ существует прямая зависимость: длительная, с частыми обострениями персистенция определяет уровень ОРЗ 6–8 и более раз в течение года.
В качестве этиотропной терапии для подавления размножения герпесвирусов наиболее целесообразным представляется использование препарата флавозид. Он воздействует на все типы герпесвирусов, проявляет свою эффективность не только как препарат острой фазы, но и как противорецидивное средство. Препарат является нетоксичным, нетератогенным, не имеет мутагенного действия, антигенных свойств, не вызывает аллергических реакций, может назначаться детям с рождения. Кроме воздействия на вирус герпеса практически во всех фазах его развития (кроме этапа сборки вирионов), обладает рядом свойств: является индуктором интерферона- a и - g , усиливает фагоцитоз, препятствует накоплению продуктов перекисного окисления (угнетает свободнорадикальные процессы), является модулятором апоптоза, вызывая гибель инфицированных клеток. Флавозид не вызывает развития резистентных штаммов, при длительном применении не приводит к иммуносупрессии, напротив, имеет свойства иммуномодулятора, индуктора интерфероногенеза и фагоцитоза, эффективен в качестве противорецидивного средства при герпетической инфекции, влияет на все типы герпесвирусов.
Флавозид принимают за 20–30 мин до еды, причем использовать его можно и у новорожденных. Схема применения препарата в педиатрической практике приводится в табл. 1.
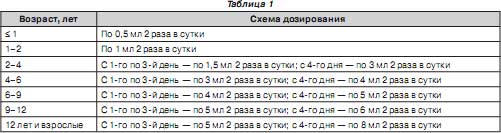
Длительность приема зависит от характера и стадии инфекционного процесса — от 1 до 3–4 месяцев.
С целью повышения функциональной активности системы интерферона, восстановления нарушенных функций иммунной системы, направленных на элиминацию вирусных и бактериальных антигенов, необходимо проведение заместительной и/или модулирующей иммунотерапии, восстанавливающей и модулирующей силу иммунного ответа, что должно обеспечить адекватный иммунный ответ на присутствие инфекционного патогена с последующей его элиминацией. И.В. Нестерова [38] предлагает иммунотропную терапию, в основе восстановления системы интерферонов и иммунной системы которой лежит базисная терапия ИФН альфа-2. Использование его в лечении ЧДБ детей позволяет получать позитивные результаты: количество ОРВИ снижается с 10–18 до 2–3 в году, число бактериальных осложнений сокращается в 4–6 раз, длительность ремиссии увеличивается в 8–10 раз — повышается качество жизни детей. Положительные клинические эффекты сопровождаются позитивной динамикой со стороны системы ИФН и иммунной системы.
Таким образом, реабилитация часто и длительно болеющих острыми респираторными заболеваниями детей требует планомерного проведения комплекса мероприятий, основной целью которых является снижение антигенной нагрузки путем предотвращения персистенции различных возбудителей, формирование адекватного иммунного ответа, позволяющего в последующем эффективно противостоять возбудителям.
Список литературы находится в редакции
