Международный эндокринологический журнал 3 (59) 2014
Вернуться к номеру
Фармакоэкономический анализ применения инсулина гларгин при сахарном диабете 2-го типа в условиях реальной клинической практики в Украине
Авторы: Бездетко Н.В., Кириченко О.Н. - Национальный фармацевтический университет, г. Харьков
Рубрики: Эндокринология
Разделы: Справочник специалиста
Версия для печати
Статья посвящена применению инсулинотерапии у пациентов с сахарным диабетом 2-го типа. Приведены данные исследования клинико-экономической целесообразности перевода пациентов с СД 2-го типа с инсулина НПХ на инсулин гларгин в условиях повседневной клинической практики в Украине.
Стаття присвячена застосуванню інсулінотерапії в пацієнтів із цукровим діабетом 2-го типу. Наведено дані дослідження клініко-економічної доцільності переведення пацієнтів із цукровим діабетом 2-го типу з інсуліну НПХ на інсулін гларгін в умовах повсякденної клінічної практики в Україні.
The article deals with the question of insulin therapy in type 2 diabetic patients. There are demonstrated the results of pragmatic trial of clinical and economic reasonability of transferring of the type 2 diabetic patients from NPH insulin treatment for the therapy with insulin glargin in routine medical practice in Ukraine.
сахарный диабет, инсулин, клинико-экономический анализ.
цукровий діабет, інсулін, клініко-економічний аналіз.
diabetes mellitus, insulin, clinical and economic analysis.
Статья опубликована на с. 77-82
Проблема сахарного диабета (СД) — это общемировая медико-социальная проблема. Несмотря на все усилия медицинской науки и практики, государственных органов здравоохранения и общественных организаций, остановить рост этого заболевания пока не удается. В Украине распространенность и заболеваемость диабетом имеют стойкую тенденцию к увеличению: в 2012 г. общее количество больных СД составило более 1 330 человек, 212 тыс. больных, из которых 8 тыс. — дети, нуждаются в инсулинотерапии [1]. Сахарный диабет занимает лидирующее место среди причин слепоты, увеличивает риск развития ишемической болезни сердца и инфаркта миокарда в 2 раза, патологии почек — в 17 раз, гангрены нижних конечностей — в 20 раз.
Диабет и его осложнения не только медицинская, но и экономическая проблема. Затраты на лечение СД и его осложнений в ЕС составляют около 90 млрд € в год, при этом на одного больного приходится 2000–3000 € [2]. В США в 2007 г. экономическое бремя СД составило 176 миллиардов долларов, а уже в 2012 превысило 245 миллиардов, в том числе 176 миллиардов прямых медицинских затрат и 69 миллиардов потерь за счет снижения трудоспособности пациентов [3, 4]. В нашей стране выделяются значительно более скромные средства на лечение больных диабетом. Так, в бюджете Украины на 2012 г. было предусмотрено примерно 520 млн грн на больных СД, то есть около 4 тыс. грн (примерно 400 евро) на одного пациента. Эти средства были израсходованы преимущественно на обеспечение инсулинами [5].
Растущее медико-социальное и экономическое бремя СД обусловливает настоятельную необходимость осуществления мер, направленных на профилактику возникновения и прогрессирования этого заболевания. Мировая практика убедительно доказала важную роль эффективного и долгосрочного гликемического контроля у больных СД. Такой контроль позволяет отсрочить во времени развитие осложнений СД, уменьшить их частоту, тяжесть, прогрессирование и существенно снизить как личные, так и государственные расходы [6]. В соответствии с современными клиническими рекомендациями, больным СД 2-го типа, у которых не удается достичь нормализации углеводного обмена путем коррекции образа жизни и терапии пероральными сахароснижающими препаратами (ПССП) показана инсулинотерапия [7, 8]. В лечении инсулином по прошествии 10–12 лет с момента развития заболевания, согласно данным Британского проспективного исследования по изучению СД (UKPDS), нуждаются около 80 % пациентов, что обосновывается снижением секреции инсулина бета-клетками приблизительно на 4 % в год [6, 9].
Существующие методики предполагают коррекцию базальной гликемии либо инсулинами средней продолжительности действия (НПХ-инсулин), либо длительно действующими аналогами человеческого инсулина (инсулин гларгин и инсулин детемир). В многочисленных клинических исследованиях доказано, что аналоги инсулина длительного действия позволяют достичь максимальной имитации физиологической секреции инсулина (беспиковый профиль, действие в течение полных суток), минимальных суточных колебаний уровня глюкозы в крови и, следовательно, наименьшего риска развития осложнений СД [10–12]. По сравнению с НПХ-инсулином инсулин гларгин и инсулин детемир обеспечивают более выраженный гликемический контроль, более низкую частоту развития гипогликемических состояний, относительно свободный образ жизни и, следовательно, более высокое качество жизни [13–16]. В экономически развитых странах за последнее десятилетие отмечается четкое увеличение доли аналогов инсулина в общей структуре потребления препаратов инсулина [17]. Основанием для широкого применения этих инсулинов наряду с доказательствами высокой эффективности и безопасности являются результаты фармакоэкономического анализа, подтверждающего их экономическую целесообразность [18, 19]. В нашей стране назначение аналогов инсулина сдерживается их более высокой по сравнению с НПХ-инсулинами стоимостью. В соответствии с национальным протоколом по ведению СД 2-го типа (2012) инсулинотерапию необходимо начинать с введения базального инсулина перед сном или 2 раза в день при необходимости. Рассмотреть как альтернативу аналог инсулина пролонгированного действия, если:
— требуется помощь опекуна или врача для введения инсулина, а использование аналога могло бы сократить частоту инъекций с двух до одного раза в день;
— стиль жизни пациента ограничивают регулярные эпизоды симптоматических гипогликемий;
— пациенту будет необходимо два раза в день получать инъекции инсулина НПХ в комбинации с пероральными сахароснижающими лекарственными средствами;
— пациент не может использовать устройство для введения инсулина НПХ [20].
Помимо цены, сдерживающим моментом более широкого применения аналогов инсулина в Украине является отсутствие фармакоэкономических исследований, основанных на отечественном опыте их применения в реальной клинической практике у больных СД 2-го типа. Это и определило цель данного исследования — оценить клинико-экономическую целесообразность перевода пациентов с СД 2-го типа с инсулина НПХ на инсулин гларгин в условиях повседневной клинической практики в Украине.
Материал и методы исследования
Объектом сравнительной клинико-экономической оценки применения в повседневной клинической практике у пациентов с СД 2-го типа двух различных схем инсулинотерапии явились материалы ретроспективного наблюдательного исследования IDEAL. Это исследование проводилось с 01.08.2011 по 06.12.2011 г. в 30 украинских клинических центрах. В анализ были включены данные 349 больных СД 2-го типа, которые в течение 4–6 месяцев получали инсулин НПХ. Первую (активную) группу составили 216 пациентов, переведенные на инсулин гларгин (Лантус®), вторую — 133 пациента, продолжившие лечение НПХ-инсулином (контрольная группа). Клинико-демографическая характеристика пациентов сравниваемых групп приведена в табл. 1.
Больные обеих групп продолжали принимать ПССП, дозы которых оставались стабильными в течение всего периода наблюдения. Результаты лечения оценивались через 6 мес. Клиническая эффективность различных вариантов инсулинотерапии оценивалась по динамике уровня HbA1c (первичный критерий эффективности). Вторичными критериями эффективности лечения служили данные о динамике уровня глюкозы крови натощак (ГКН), дозе инсулинов, количестве эпизодов гипогликемий и числе дней нетрудоспособности.
Фармакоэкономический анализ применения двух схем терапии проводился методом «затраты/эффективность» (cost-effectiveness analysis, СЕA), который позволяет одновременно оценивать как стоимость альтернативных методов лечения, так и их эффективность [21, 22]. Перед началом анализа по этому методу с учетом особенностей каждого конкретного заболевания выбирается клинически значимый критерий эффективности лечения. Им может быть число выздоровевших больных, или число больных, у которых удалось избежать развития осложнений, или число предупрежденных рецидивов и др. Далее для каждой из сравниваемых схем лечения рассчитывается коэффициент эффективности затрат (cost-effectiveness ratio, СЕR). Он показывает стоимость выбранной единицы эффективности — величину затрат, необходимых для того, чтоб вылечить одного больного (или предупредить развитие осложнений у одного больного, или предупредить один рецидив заболевания — в зависимости от выбранного критерия эффективности). Чем меньше коэффициент СЕR, тем меньше затраты на достижение желаемого клинического результата, а следовательно, метод лечения более выгоден с экономической точки зрения.
Расчеты СЕR проводят по формуле:
/79/79.jpg)
где CER — коэффициент эффективности затрат; DC — затраты, связанные с лечением больного; Ef — эффективность лечения, выраженная в единицах, которые соответствуют выбранным критериям терапии.
В данном исследовании в качестве основного критерия эффективности рассматривали количество больных, у которых в результате лечения удалось достичь целевого уровня HbA1c (6,5–7,5 %). Соответственно, коэффициент CER — это стоимость достижения целевого уровня HbA1c у одного больного.
Также рассчитывались следующие фармакоэкономические показатели.
Число больных, которых необходимо лечить (ЧБНЛ), показывает количество пациентов, которых необходимо пролечить, чтобы достичь одного благоприятного исхода (в данном исследовании — достичь целевого уровня HbA1c). ЧБНЛ определяется как отношение: 1/разница абсолютного риска получения результата. Чем выше ЧБНЛ, тем менее эффективно лечение [23].
Прогнозная стоимость достижения компенсации (целевого уровня HbA1c у одного пациента) рассчитывается как произведение стоимости лечения одного больного и ЧБНЛ.
Коэффициент эффективности вложений — отношение затрат на лечение пациентов, у которых удалось достичь желаемых результатов, к затратам на лечение тех больных, у которых желаемого результата достичь не удалось [24].
Источники данных для моделирования затрат на лечение. При проведении фармакоэкономических расчетов учитывали затраты на инсулин, иглы, шприцы, скарификаторы, тест-полоски, стоимость которых определялась как оптовая (без учета розничной торговой надбавки) цена дистрибьютора «БаДМ», по данным еженедельника «Аптека» по состоянию на 01.02. 2014 г. [25]. Стоимость НПХ-инсулина рассчитывалась как средняя цена всех представленных в Украине препаратов с учетом частоты применения каждого из них.
Потери государством ВВП вследствие временной утраты трудоспособности больных СД за период исследования и средние выплаты государства по листу нетрудоспособности были рассчитаны исходя из величины средней заработной платы и данных о производительности труда за один рабочий день в Украине за 2012 год [26].
Статистический анализ проведен с помощью методов описательной статистики (параметрические и непараметрические методы) с уровнем значимости не менее 95 %.
Результаты и обсуждение
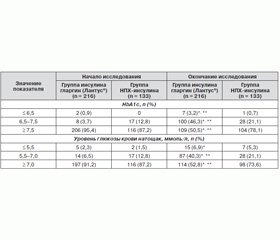
Клиническая оценка. Анализ данных наблюдательной программы по основному критерию эффективности (динамике HbA1c) и уровню ГКН показал преимущества инсулина гларгин перед НПХ-инсулином по влиянию на углеводный обмен. Так, исходный уровень HbA1c превышал 7,5 % у 95,4 % пациентов группы инсулина гларгин и у 87,2 % группы НПХ-инсулина. По окончании исследования уровня HbA1c в диапазоне значений 6,5–7,5 % достигли 46,3 % пациентов активной группы и только 21,1 % пациентов контрольной группы. Также в группе инсулина гларгин у статистически значимо большего количества пациентов было достигнуто снижение уровня глюкозы крови натощак (до значений 5,5–7,5 ммоль/л), чем у пациентов, получавших НПХ-инсулин (табл. 2).
Анализ дозировки инсулина в конце исследования продемонстрировал, что средняя доза гларгина составила 28,44 ± 0,71 МЕ, а НПХ-инсулина — 35,65 ± 1,37 МЕ (p < 0,05).
Общее количество всех случаев симптоматической гипогликемии, отмеченных среди 349 пациентов в течение последнего месяца ретроспективного исследования, составило 361, включая 90 случаев документированной гипогликемии, 90 — ночной гипогликемии, 9 — тяжелой гипогликемии (табл. 3). Явления гипогликемии отсутствовали у 156 (71,22 %) пациентов в группе инсулина гларгин и у 55 (41,35 %) пациентов в группе НПХ-инсулина (p < 0,05).
Перевод на терапию инсулином гларгин привел к уменьшению числа дней нетрудоспособности: 0,19 дня на пациента в месяц в активной группе и 0,35 дня — в контрольной группе (p < 0,05). Анализ внутри групп показал, что по количеству дней нетрудоспособности в группе инсулина гларгин 87,87 % пациентов были нетрудоспособны в течение 1–14 дней, а 12,12 % — в течение 15–29 дней (p < 0,05). Для группы НПХ-инсулина нетрудоспособность в течение 1–14 дней отмечена у 60,71 % пациентов, а у 39,28 % пациентов она составила 15–29 дней.
В течение всего периода наблюдения были госпитализированы 17 пациентов (7,87 %) из числа получавших инсулин гларгин и 14 (10,53 %) получавших НПХ-инсулин (p > 0,05). Средняя продолжительность госпитализации в группе инсулина гларгин составила 12,18 ± 2,16 дня, в группе НПХ-инсулина — 14,36 ± 3,77 дня (p > 0,05).
Таким образом, анализ данных наблюдательного исследования показал, что применение инсулина гларгин в течение 6 месяцев демонстрирует лучшую компенсацию у пациентов с СД 2-го типа (на основе полученных показателей уровней HbA1с, HbA1с и ГКН) в сравнении с инсулином НПХ. Достижение компенсации СД 2-го типа после приема инсулина гларгин требовало у пациентов меньшего количества дневных доз инсулина, реже вызывало гипогликемические состояния и уменьшало число дней нетрудоспособности.
Экономическая оценка. Утилитарная стоимость инсулина гларгин (стоимость эквивалентного количества МЕ и 1 МЕ) выше, чем инсулина НПХ, в 3,8 раза (табл. 4).
С учетом данных наблюдательного исследования о величине средней суточной дозы инсулинов, количестве используемых игл, шприцев, скарификаторов, тест-полосок разница между суммарными затратами на терапию инсулином гларгин и инсулином НПХ оказалась меньше, чем разница утилитарной стоимости препаратов, и составила 1,8 раза.
Основой фармакоэкономического анализа является положение о том, что стоимость альтернативных схем лечения необходимо рассматривать в комплексе с их эффективностью. Установленная в наблюдательном исследовании значительная разница в эффективности двух схем инсулинотерапии проявилась существенными различиями показателя «затраты/эффективность». В группе инсулина гларгин данный показатель составил 10 698,59 грн/1 ед. эффективности (на одного больного, у которого был достигнут целевой уровень HbA1c в диапазоне значений 6,5–7,5 %), а в группе НПХ-инсулина — 29 862,65 грн/1 ед. эффективности, т.е. в 2,8 раза больше (р < 0,001). Таким образом, показатель «затраты/эффективность», который является ключевым фармакоэкономическим показателем, убедительно свидетельствует о большей экономичности инсулина гларгин по сравнению с НПХ-инсулином в данном исследовании.
Экономические преимущества инсулина гларгин перед НПХ-инсулином по показателю «затраты/эффективность» подтверждаются показателями ЧБНЛ, прогнозной стоимостью 1 компенсации, коэффициентом эффективности вложений.
Показатель ЧБНЛ, отражающий число больных, которых необходимо пролечить в течение периода наблюдения, чтобы достичь компенсации у одного пациента, для инсулина гларгин составил 2,35 (1/0,426 = 2,35), а для НПХ-инсулина — 12,05 (1/0,083 = 12,05). Соответственно, прогнозная стоимость достижения компенсации уровня HbA1c у 1 пациента за период наблюдения (6 мес.) составляет при использовании инсулина гларгин 10 710,36 грн, а инсулина НПХ — 29 867,13 грн, т.е. в 2,8 раза больше.
Коэффициент эффективности вложений при терапии инсулином гларгин почти на порядок выше, чем инсулином НПХ, и составил 0,74. Это значит, что на каждую гривну, вложенную в терапию, имеется отдача 74 коп. Соответственно для НПХ-инсулина отдача на каждую гривну составляет всего 9 коп.
Экономические потери государства (потери ВВП) за период исследования вследствие временной утраты трудоспособности больными СД 2-го типа в группе инсулина гларгин были в 1,85 раза меньше, чем в группе инсулина НПХ, и составили соответственно 140,59 и 258,97 грн.
Затраты государства на оплату листов нетрудоспособности из расчета на 1 человека в группе инсулина гларгин были в 1,8 раза меньше, чем в группе НПХ-инсулина, и составили соответственно 164,22 и 302,51 грн.
Полученные результаты клинико-экономического анализа экономической целесообразности перехода на инсулин гларгин в условиях реальной клинической практики в Украине подтверждаются данными исследований, проведенных в других странах [24, 27–31].
Выводы
Таким образом, проведенный клинико-экономический анализ применения инсулина гларгин (Лантус®) в сравнении с инсулином НПХ показал как клинические преимущества, так и экономическую целесообразность применения инсулина гларгин у пациентов с СД 2-го типа.
Несмотря на более высокую утилитарную стоимость инсулина гларгин по сравнению с НПХ-инсулином, он имеет экономические преимущества перед последним по следующим параметрам:
— в 2,8 раза ниже коэффициент «затраты/эффективность»;
— в 2,8 раза ниже прогнозная стоимость достижения компенсации в течение 6 мес.;
— в 8 раз выше коэффициент эффективности вложений.
Применение инсулина гларгин в терапии пациентов с СД 2-го типа также позволяет в 1,8 снизить потери государства вследствие временной утраты трудоспособности больными СД 2-го типа и оплаты им листов нетрудоспособности.
Полученные результаты полностью соответствуют опыту ведущих европейских стран, США и Канады и подтверждают, что в условиях ограниченных ресурсов здравоохранения принятие решения о внедрении и распространении того или иного альтернативного варианта терапии любого заболевания, в особенности такого, как СД, кроме клинических данных должно основываться на результатах фармакоэкономического анализа.
1. Новости УНИАН 14.11.2013 [Электронный ресурс]. Режим доступа: http: // health.unian.ua/country/851984-v-ukrajini-zrostae-kilkist-hvorih-na-tsukroviy-diabet.html
2. Health: the high cost of diabetes [Электронный ресурс]. Режим доступа: http: // www.oecd.org/eu/healththehighcostofdiabetes.htm
3. American Diabetes Association. Economic costs of diabetes in the U.S. in 2007 // Diabetes Care. — 2008. — Vol. 31. — P. 596–615.
4. American Diabetes Association. Economic costs of diabetes in the U.S. in 2012 // Diabetes Care. — 2013. — Vol. 36. — P. 1033–1046.
5. Новые технологии в диагностике, профилактике и лечении наиболее распространенных эндокринных заболеваний // Здоровье Украины — 2012. — № 4 (20). — С. 12–13.
6. UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33) // Lancet. — 1998. — Vol. 352. — Р. 837–853.
7. Inzucchi S.E. et al. Management of hyperglycaemia in type 2 diabetes: a patient-centered approach. Position statement of ADA and EASD // Diabetologia. — DOI 10.1007/s 00125-012-2534-0
8. Herman W. The Economic Costs of Diabetes: Is It Time for a New Treatment Paradigm? // Diabetes Care. — 2013. — Vol. 36, № 4. — P. 775–776.
9. Маньковский Б.Н., Жердева Н.Н. Инсулинотерапия. Что нового? // Международный эндокринологический журнал. — 2013. — № 3 (51).
10. Vaag A., Lund S.S. Insulin initiation in patients with type 2 diabetes mellitus: treatment guidelines, clinical evidence and patterns of use of basal vs premixed insulin analogues // Eur. J. Endocrinol. — 2012. — Vol. 166, 32. — P. 159–170.
11. A 52-week, multinational, open-label, parallel-group, noninferiority, treat-to-target trial comparing insulin detemir with insulin glargine in a basal-bolus regimen with mealtime insulin aspart in patients with type 2 diabetes / P. Hollander, J. Cooper, J. Bregnhoj et al. // Clin. Ther. — 2008. — Vol. 30. — P. 1976–1987.
12. Basal insulin therapy in type 2 diabetes: 28-week comparison of insulin glargin (HOE 901) and NPH insulin / J. Rosenstock, S. Schwarts, C. Clark et al. // Diabetes Care. — 2001. — Vol. 24. — P. 631–636.
13. Comparison of Insulin Glargine Versus NPH Insulin in People with Type 2 Diabetes Mellitus Under Outpatient-Clinic Conditions for 18 Months Using a Basal-Bolus Regimen with a Rapid-Acting Insulin Analogue as Mealtime Insulin / S. Siegmund, S. Weber, H. Blankenfeld et al. // Exp. Clin. Endocrinol. Diabetes. — 2007. — Vol. 115, № 6. — P. 349–353.
14. Reduced hypoglycemia risk with insulin glargine: a meta-analysis comparing insulin glargine with human NPH insulin in type 2 diabetes / J. Rosenstock, G. Dailey, M. Massi-Benedetti et al. // Diabetes Care. — 2005. — Vol. 28. — Р. 950–955.
15. Schreiber S.A., Russmann A. The effects of insulin glargine treatment and an educational program on glycaemic control in type 2 diabetes patients in clinical practice // Curr. Med. Res. Opin. — 2006. — Vol. 22, № 2. — Р. 335–341.
16. The impact of insulin glargine on clinical and humanistic outcomes in patients uncontrolled on other insulin and oral agents: an office-based naturalistic study / J.S. Fischer, T. McLaughlin, L. Loza et al. // Curr. Med. Res. Opin. — 2004. — Vol. 20, № 11. — Р. 1703–1710.
17. Use of Antidiabetic Drugs in the U.S., 2003–2012 / C. Hampp, V. Borders-Hemphill, D. Moeny et al. // Diabetes Care. — 2014. — Vol. 37. — P. 1367–1374.
18. Levin P. The cost-effectiveness of insulin glargine vs. neutral protamine Hagedorn insulin in type 2 diabetes: a focus on health economics // Diabetes, Obesity and Metabolism. — 2008. — Vol. 10 (Suppl. 2). — P. 66–75.
19. Systematic review and economic evaluation of a long-acting insulin analogue, insulin glargine / E. Warren, E. Weatherley-Jones, J. Chilcott et al. // Health Technol. Assess. — 2004. — Vol. 8 (45). — P. 1–57.
20. Наказ МОЗ України від 21.12.2012 № 1118 «Уніфікований клінічний протокол первинної та спеціалізованої медичної допомоги. Цукровий діабет 2-го типу».
21. Фармакоекономіка / Л.В. Яковлєва, Н.В. Бездітко, О.О. Герасимова та ін. — Вінниця: Нова книга, 2009. — 208 с.
22. Levin H.M. Cost-Effectiveness Analysis: Methods and Applications. — SAGE Publications, 2001. — 308 p.
23. Hutton J. Misleading Statistics: The Problems Surrounding Number Needed to Treat and Number Needed to Harm // Pharm. Med. — 2010. — Vol. 24, № 3. — P. 145–149.
24. Аметов А.С., Белоусов Д.Ю. Фармакоэкономика инсулина гларгин при оптимизации инсулинотерапии сахарного диабета 2-го типа // Качественная клиническая практика. — 2012. — № 2. — С. 13–21.
25. Аптека on line. — [Электронный ресурс]. — Режим доступа к сайту http: // www.pharmbase.com.ua. — Название с экрана.
26. Государственный комитет статистики Украины. [Электронный ресурс]. — Режим доступа к сайту http: // www.ukrstat.gov.ua
27. Белоусов Д.Ю. Фармакоэкономика инсулина гларгина (Лантус) в зеркале зарубежных доказательных исследований: обзор литературы // Клиническая фармакология и терапия. — 2008. — № 17 (2). — С. 84–88.
28. Grima D.T., Thompson M.F., Sauriol L. Modelling Cost Effectiveness of Insulin Glargine for the Treatment of Type 1 and 2 Diabetes in Canada // Pharmacoeconomics. — 2007. — Vol. 25, № 3. — P. 253–266.
29. Brandle M., Azoulay M., Greiner R.. Cost-effectiveness and cost-utility of insulin glargine compared with NPH insulin based on a 10-year simulation of long-term complications with the Diabetes Mellitus Model in patients with type 2 diabetes in Switzerland // International Journal of Clinical Pharmacology and Therapeutics. — 2007. — Vol. 45, № 4. — Р. 203–220.
30. Evaluation of the costeffectiveness of insulin glargine versus NPH insulin for the treatment of type 1 diabetes in the UK / P. McEwan, C. Poole, T. Tetlow et al. // Curr. Med. Res. Opin. — 2007. — Vol. 23, Suppl. 1. — Р. 7–19.
31. Clissold R., Clissold S. Insulin glargine in the management of diabetes mellitus: an evidence-based assessment of its clinical efficacy and economic value // Core Evidence. — 2007. — Vol. 2. — P. 89–110.

/78/78.jpg)
/80/80.jpg)
/81/81.jpg)