Статья опубликована на с. 37-41
Главнейшие и существенные задачи практической медицины — предупреждение болезни, лечение болезни развившейся и, наконец, облегчение страданий больного человека.
С.П. Боткин
В связи с неуклонным ростом у детей частоты хронических заболеваний печени, характеризующихся прогрессирующим течением и неблагоприятным медико-социальным прогнозом, велика актуальность вопросов оптимизации базисной фармакотерапии данных заболеваний. В основе терапии хронических заболеваний печени у детей лежит нозологический принцип, то есть выделение отдельных нозологических форм болезней на основе общности этиологии, патогенеза, клинических проявлений и исходов и, соответственно, устранение или коррекция этиологических факторов, вызвавших заболевание. Однако в клинической практике мы часто сталкиваемся с ситуациями, когда проведение этиотропного лечения невозможно, но необходимо уменьшить активность воспалительного и холестатического процессов, замедлить процесс фиброгенеза. Традиционно для этой цели используются гепатопротекторы, оказывающие влияние на патогенетические механизмы, лежащие в основе заболеваний печени и характеризующиеся независимо от этиологии заболевания клеточным повреждением, сопровождающимся воспалительной реакцией, цитолизом, гепатоцеллюлярным (интралобулярным) холестазом, развитием и прогрессированием печеночно-клеточной недостаточности и фиброза печени.
Среди множества гепатопротекторов выделяется урсодезоксихолевая кислота (УДХК) — физиологическая субстанция, составляющая примерно 1 % человеческой желчи. Применение УДХК для лечения заболеваний печени и билиарного тракта имеет древнюю историю. Более 2000 лет назад врачи Древнего Китая назначали «печеночным» больным сухую медвежью желчь, содержащую в высокой концентрации УДХК; в 1954 году был описан метод синтеза УДХК, а в 1975 году — действие УДХК на желчь (десатурация желчи, растворение мелких холестериновых камней). С этого времени препарат стали применять для лечения желчнокаменной болезни, в процессе лечения было отмечено улучшение печеночных биохимических показателей, что и явилось основанием для расширения терапевтических возможностей УДХК и ее назначения при других заболеваниях печени.
Урсодезоксихолевая кислота представляет собой нетоксичную третичную желчную кислоту (ЖК), образующуюся в кишечнике и печени; в норме содержится в желчи человека в небольших количествах — не более 5 % от общего пула желчных кислот. Она является более полярной и гидрофильной по сравнению с другими ЖК, что обусловливает практически полное отсутствие ее токсичности.
На сегодняшний день хорошо известны и апробированы многочисленные специфические эффекты УДХК: антихолестатический, холеретический, цито-/гепатопротективный, антиапоптотический, иммуномодулирующий, гипохолестеринемический, литолитический, антифибротический, антиоксидантный, антинеопластический. Прием УДХК обусловливает повышение бактерицидности желчи и кишечного содержимого, угнетение бактериального роста в кишечнике, купирование бродильной и гнилостной диспепсии, оказывает метаболический эффект, способствуя снижению сывороточного уровня глюкозы, инсулина и индекса НОМА, регулирует метаболизм липидов, гомеостаз желчных кислот, а также пролиферацию и дифференциацию холангиоцитов. Таким образом, УДХК выполняет важные функции и за рамками кишечно-печеночной оси и действует как системный метаболический интегратор.
Круг патологических состояний печени очень велик, и большинство этих изменений могут сопровождаться нарушением любой из перечисленных функций печени или многих с тем или иным преобладанием. Именно УДХК является оптимальным препаратом для патогенетической терапии широкого спектра заболеваний печени и желчевыводящих путей с воздействием на максимальное число звеньев патогенеза. С учетом физиологической роли УДХК ее введение извне является предпочтительным терапевтическим решением уже с первых дней заболевания, возможно, и на этапе диагностического поиска.
Важно учитывать, что при заболеваниях печени за счет выраженного нарушения ее функций может значительно нарушаться метаболизм фармакологических препаратов с последующими неконтролируемыми побочными эффектами. В связи с этим у таких больных возможно применение лишь абсолютно показанных и достоверно безопасных лекарственных средств.
Наибольший положительный опыт применения УДХК накоплен нами при использовании препарата Урсофальк®, Dr. Falk Pharma GmbH, Фрайбург (с 1987 года). В настоящее время около 75 % детей с заболеваниями печени получают Урсофальк в рекомендованных дозировках, при этом около 10 % — более 10 лет. С 1987 г. нами не было зарегистрировано ни одного случая непереносимости Урсофалька, потребовавшего его отмены.
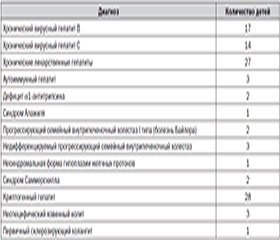
Распределение детей, получавших терапию Урсофальком, представлено в табл. 1.
Следует отметить, что наблюдаемые нами дети с хроническими вирусными гепатитами В и С (31 ребенок) не получали специфической противовирусной терапии по различным причинам: наличие противопоказаний, ранний возраст (до 3 лет), большое количество побочных эффектов противовирусной терапии, отказ родителей, отсутствие разрешения для назначения пегилированных интерферонов детям с массой тела менее 35 кг и др. Терапия таких детей включала диету, охранительный режим и, с учетом многофакторности заболевания, Урсофальк в дозе 10–15 мг/кг массы тела в сутки курсами по три месяца один-два раза в год в течение всего срока наблюдения.
Дети с хроническими лекарственно-токсическими гепатитами получали терапию Урсофальком дважды в год курсами по три месяца в дозе 10–15 мг/кг
массы тела длительно — соответственно длительности назначаемых гепатотоксичных препаратов.
Три девочки с аутоиммунным гепатитом получали иммуносупрессивную терапию преднизолоном: на этом фоне одна девочка получает Урсофальк в течение 13 месяцев в дозе 15 мг/кг массы тела, вторая девочка — курсами дважды в год по три месяца длительно на фоне поддерживающей дозы преднизолона в дозе 15 мг/кг массы тела, третья — продолжила курсы Урсофалька дважды в год длительностью три месяца в состоянии стойкой ремиссии после отмены преднизолона в течение 2 лет в дозе 10 мг/кг массы тела.
Дети с дефицитом a1-антитрипсина и ребенок с синдромом Алажиля в составе комплексной терапии получали длительно курсами по три месяца Урсофальк в дозе 10–15 мг/кг массы тела.
Все наблюдаемые нами дети с врожденными синдромами внутрипеченочного холестаза (болезнь Байлера, недифференцируемый прогрессирующий семейный внутрипеченочный холестаз, несиндромальная форма гипоплазии желчных протоков) родились доношенными с антропометрическими показателями, соответствующими физиологической норме. Желтуха появилась на 2-е — 3-и — 5-е сутки жизни. Примерно у двух третей больных отмечалось наличие «светлого промежутка» — уменьшение интенсивности желтухи к концу 1–2-й недели жизни с последующим постепенным ее нарастанием и появлением зеленоватого оттенка желтухи к концу 1-го месяца; характерным являлся непостоянный характер ахолии стула и отсутствие гепатомегалии при рождении с последующим увеличением размеров печени и изменением ее консистенции от эластичной до плотной в течение первых 2 месяцев жизни. К возрасту 1–3 месяцев жизни развивался геморрагический синдром (кровотечение со слизистых пищеварительной системы, из пупочной ранки, внутричерепное кровоизлияние), обусловленный дефицитом витамин-К-зависимых факторов свертываемости крови в результате нарушения процессов всасывания витамина К в кишечнике. К возрасту 1–2–4 месяцев жизни у всех наблюдаемых детей был сформирован дефицит веса, степень выраженности которого зависела от вида вскармливания ребенка.
Наиболее ранний лабораторный признак болезни — повышение билирубина за счет прямой фракции в сыворотке крови, составляющей более 20 % от уровня общего билирубина, характерно повышение других биохимических маркеров холестаза (β-липопротеиды, холестерин, щелочная фосфатаза, желчные кислоты и др.), степень выраженности которых в динамике нарастает от минимального повышения в течение первых 2–3 недель жизни до значительного повышения к 2–3 месяцам. Ферменты цитолиза (аланин- и аспартатаминотрансфераза — АЛТ, АСТ) повышались умеренно и, как правило, отсроченно. В большинстве случаев в течение первых 2–3 недель после рождения эти показатели оставались в пределах нормы и затем постепенно повышались. Показатели, отражающие белково-синтетическую функцию печени (альбумин, фибриноген, протромбиновый индекс и др.), на ранних сроках болезни не изменялись.
Из двух детей из одной семьи с прогрессирующим семейным внутрипеченочным холестазом I типа (болезнью Byler), находящихся под нашим наблюдением, у одного мальчика с выраженным кожным зудом, ксантомами к 6 месяцам жизни появились признаки портальной гипертензии, спленомегалия, что свидетельствовало о формировании билиарного цирроза печени, проявления которого в дальнейшем прогрессивно наросли и от которых в возрасте 1,5 года ребенок погиб.
Второй ребенок — девочка 10 месяцев на данный момент находится на поддерживающей терапии секвестрантами желчных кислот и Урсофальком в дозе 25 мг/кг массы тела и готовится к проведению трансплантации печени.
Три ребенка с недифференцируемым прогрессирующим семейным внутрипеченочным холестазом (находятся на этапе диагностического поиска) и ребенок с несиндромальной формой гипоплазии желчных протоков получают поддерживающую терапию Урсофальком в дозе 20–25 мг/кг массы тела постоянно.
У двух девочек из одной семьи заболевание начиналось с первых недель жизни интенсивной желтухой с высоким уровнем прямого билирубина и признаками дефицита жирорастворимых витаминов (кровотечениями вследствие дефицита витамина К), в процессе наблюдения отмечалось волнообразное течение желтухи, наличие «светлых промежутков», с каждым разом все более длительных, с последующим постепенным нарастанием желтухи, с величинами билирубина каждый раз более низкими, чем предыдущие. Особенности клинической картины заболевания и результаты дообследования позволили диагностировать у девочек доброкачественный семейный внутрипеченочный холестаз, обусловленный гипоплазией лимфатических сосудов печени, — синдром Саммерскилла.
Все дети с криптогенным гепатитом получали Урсофальк от 3 до 6 месяцев под контролем биохимических проб печени длительностью от 1 года до 11 лет.
У двух мальчиков с неспецифическим язвенным колитом, подтвержденным результатами гистологического исследования, в клинической картине заболевания (с первых дней наблюдения) преобладали внекишечные поражения — имели место выраженные синдромы цитолиза и холестаза. Оба ребенка первоначально получили курс Урсофалька в дозе 20 мг/кг массы тела в течение 3 месяцев, а затем на протяжении ряда лет — в поддерживающей дозе 10 мг/кг по три месяца дважды в год. При попытке не проводить поддерживающую терапию отмечалось повышение уровня трансаминаз в 2–3 раза. У одного мальчика с неспецифическим язвенным колитом через два года от начала заболевания появился синдром цитолиза, что потребовало назначения Урсофалька в дозе 12 мг/кг массы тела на три месяца.
По показаниям детям с синдромом холестаза назначалась сопутствующая терапия, проводилась коррекция митохондриальных нарушений витаминами В6 и Е, коррекция и профилактика остеопороза препаратами кальция и витамином D3, коррекция дефицита жирорастворимых витаминов А, Е, К.
Очень интересное наблюдение — единственный в нашей многолетней практике случай редко встречающегося у детей заболевания — первичного склерозирующего холангита (ПСХ). Этиологию данного заболевания до сих пор установить не удалось. Определенное значение в развитии ПСХ могут иметь токсичные (гидрофобные и липофильные) желчные кислоты — литохолевая и дезоксихолевая, поступающие в печень по воротной вене из кишечника и способные вызывать деструкцию протокового эпителия желчных путей с накоплением свободных радикалов кислорода — продуктов перекисного окисления липидов, которые запускают процесс активации каспаз и нарастание процесса апоптоза клеток эпителия желчных протоков. Большинство авторов, изучающих ПСХ, рассматривают его как аутоиммунное заболевание.
Под нашим наблюдением находится мальчик с первичным склерозирующим холангитом. На сего–дняшний день мальчику исполнилось 15 лет, болен с 13 лет, заболевание дебютировало с субфебрилитета, зуда кожи, нарастающей общей слабости. Мальчик был госпитализирован в стационар, где при обследовании на фоне гепатолиенального синдрома были выявлены анемия, диспротеинемия, синдром цитолиза, диффузные изменения ткани печени при ультразвуковом исследовании. Наследственный анамнез отягощен — у отца бронхиальная астма; аллергологический анамнез не отягощен, указаний на оперативные вмешательства, гемотрансфузии, донорство крови и наличие сопутствующих заболеваний в прошлом нет. В ходе обследования у ребенка были исключены: болезнь Вильсона — Коновалова, дефицит α1-антитрипсина, болезни накопления, наследственные нарушения обмена аминокислот, аутоиммунный гепатит. По результатам компьютерной томографии с внутривенным контрастированием выявлены гепатоспленомегалия и очаговые изменения печени неуточненного генеза (неопластический, воспалительный процесс?); при гистологическом исследовании биоптатов печени имеет место морфологическая картина, характерная для хронического склерозирующего холангита, — описан vanishing bile duct syndrome с перипортальным фиброзом и начальными морфологическими признаками цирротических изменений. Проведенные исследования позволили диагностировать первичный склерозирующий холангит и начать лечение метипредом 16 мг в сутки и Урсофальком 250 мг в сутки, что позволило добиться биохимической ремиссии. Через восемь месяцев от начала лечения на фоне снижения дозы глюкокортикоидного препарата у мальчика появился жидкий стул до пяти раз в сутки с примесью крови, при эндоскопическом обследовании были выявлены эрозии слизистой оболочки сигмовидной кишки, после назначения Салофалька и коррекции дозы глюкокортикостероидного препарата (возвращение к первичной дозе) состояние мальчика улучшилось. Через десять месяцев от начала заболевания имело место повышение уровня трансаминаз, что продиктовало необходимость увеличения дозы Урсофалька до 25 мг/кг
массы тела. В данном случае назначение УДХК имело целью не только патогенетическое воздействие на патологический процесс в печени, но и, с учетом данных о влиянии УДХК на снижение риска развития колоректальной дисплазии у пациентов с язвенным колитом и первичным склерозирующим холангитом, предназначалось для решения вопроса канцерпревенции. Через месяц от начала терапии высокой дозой УДХК у мальчика уменьшился процесс цитолиза в печени — снизился уровень АЛТ и АСТ. Проведено контрольное ректороманоскопическое исследование — умеренно выраженные явления катарального проктосигмоидита, при гистологическом исследовании биоптата — проявления хронического колита с лимфофолликулярной гиперплазией и частично атрофическими изменениями, что позволило выставить мальчику сопутствующий диагноз — «хронический неспецифический неязвенный колит (атрофический), период неполной клинической ремиссии». На сегодняшний день при массе тела 63 кг мальчик продолжает получать метипред 16 мг в сутки и Урсофальк 600 мг в сутки, находится в состоянии биохимической ремиссии. Вместе с тем, по данным литературы, лечение больных ПСХ препаратами УДХК не влияет на прогрессирование фиброза и воспалительный процесс в печени, которые обусловливают деструкцию желчных протоков с появлением стеноза и прогрессирующую обструкцию протоковой системы, а также не оказывает влияния на продолжительность жизни больных.
Динамическое наблюдение за детьми, получающими УДХК, позволило отметить практически у всех клиническое и биохимическое улучшение. Эффект лечения больных препаратом УДХК подтверждается следующими данными.
— Уменьшается внутри- и внепеченочный холестаз, о чем свидетельствует снижение уровня ферментов холестаза (щелочной фосфатазы, гамма-глутамилтранспептидазы, лейцинаминопептидазы).
— Нормализуется уровень желчных кислот крови.
— Уменьшается процесс цитолиза в печени, что подтверждается снижением уровня ферментов цитолиза (АЛТ и АСТ).
— Уменьшается выраженность желтухи за счет снижения уровня общего и конъюгированного билирубина.
— Снижается уровень холестерина в желчи, способствуя растворению холестериновых желчных камней и предупреждая их образование.
— Уменьшается интенсивность кожного зуда.
— Снижается гипериммуноглобулинемия, в том числе уровень IgM.
— Длительный прием УДХК улучшает гистологическую картину печени (по результатам фибротеста) и, как полагают, замедляет прогрессирование портальной гипертензии.
Для своевременного определения стадии фиброза и контроля за его развитием на фоне терапии, а также для оценки некровоспалительного процесса в печеночной ткани ряду детей был проведен фибротест. Тест отображает стадии фиброза (F0, Fl, F2, F3, F4) и степень некровоспалительного процесса (А0, Al, A2, A3) по международной общепринятой системе METAVIR, позволяет осуществлять универсальную интерпретацию результатов исследования. У всех обследованных детей было определено достоверное уменьшение некровоспалительного процесса и, что представляется нам важным, уменьшение прогрессирования фиброза — снижение стадии фиброза. Например, снижение с F3 до Fl у мальчика с криптогенным гепатитом, получавшего Урсофальк в дозе 15 мг/кг массы тела дважды в год по три месяца в течение 2 лет; снижение с F2 до F0 у мальчика с хроническим вирусным гепатитом С с умеренной степенью активности и высокой вирусной нагрузкой, получавшего Урсофальк в дозе 15 мг/кг массы тела дважды в год по три месяца в течение 4 лет.
Таким образом, проведенные исследования показали положительное влияние Урсофалька на состояние детей с заболеваниями печени; для преду–преждения развития необратимых изменений в печени лечение больных необходимо и возможно начинать как можно раньше.
Список литературы
1. Cheng K., Ashby D., Smyth R. Ursodeoxycholic acid for Cystic Fibrosis-related liver disease (Cochrane Review) // The Cochrane Library, Cochrane Database Syst. Rev. — 2014 Dec 15. — 12. — CD000222. — Doi: 10.1002/14651858.CD000222.pub3.
2. Ghany et al. An update on treatment of genotype 1 chronic hepatitis C virus infection: 2011 practice guideline by the American Association for the Study of Liver Diseases // Hepatology. — 2011 Oct. — № 54(4). — Р. 1433–44. — Doi: 10.1002/hep.24641.
3. Nunnari G., Pinzone M.R., Cacopardo B. Lack of clinical and histological progression of chronic hepatitis C in individuals with true persistently normal ALT: the result of a 17-year follow-up // J. Viral. Hepat. — 2013, Apr. — № 20(4). — e131-7. — Doi: 10.1111/jvh.12029.
4. Okada K., Shoda J., Taguchi K. Ursodeoxycholic acid stimulates Nrf2_mediated hepatocellular transport, detoxification, and antioxidative stress systems in mice //Am. J. Physiol. Gastrointest. Liver Physiol. — August 7, 2008. — Doi:10.1152/ajpgi.90321.2008.
5. Pinheiro N.C. et al. Refractory pruritus in primary biliary cirrhosis // BMJ Case Rep. — 2013 Nov. — № 14. — Pii: bcr2013200634. doi: 10.1136/bcr-2013-200634.
6. Silverio A.O. et al. Are the spider angiomas skin mar–kers of hepatopulmonary syndrome? // Arq. Gastroenterol. — 2013 Jul — Sep. — Vol. 50(3). — Р. 175-179. — Doi: 10.1590/S0004-28032013000200031.
7. Guarino M.P., Cocca S., Altomare A. et al. UDCA in the treatment of diseases of the gallbladder: unfinished the story // World J. Gastroenterol. — 2013 Aug 21. — № 19(31). — Doi: 10.3748/wjg.v19.i31.5029.
8. Uto H., Mawatari S., Kumagai K. et al. Clinical features of hepatitis C virus carriers with persistently normal alanine aminotransferase levels // Hepat. Mon. — 2012, Feb. — № 12(2). — Р. 77-84. — Doi: 10.5812/hepatmon.829.
9. Wunsch E., Trottier J., Milkiewicz M., Raszeja-Wyszomirska J. et al. The consequences of the abolition of UDCA in patients with primary sclerosing cholangitis // Hepatology. — 2014 Feb 12. — Doi: 10.1002/hep.27074.
10. Герок В., Блюм Х.Е. Заболевания печения и желчевыделительной системы: Пер. с нем. — М., 2009.
11. Дитяча гастроентерологія. Підручник / Бєлоусов Ю.В., Бєлоусова О.Ю., Бабаджанян О.М., Волошина Л.Г. та ін. — Харкі‑в, 2013. — 520 с.
12. Эль-Райфе Н., Готтранд Ф. Роль урсодезоксихолевой кислоты в лечении холестаза у детей // Consilium medicum Ukraina. — 2008. — № 10.
13. Циммерман С. Первичный склерозирующий холангит: современные представления // Клиническая медицина. — 2014. — № 1. — С. 5–10.

/38.jpg)