Статья опубликована на с. 93-98
Много еще нам нужно узнать, а узнав, удивиться многообразию нашего мира и нашей жизни.
Альберт Эйнштейн
Одной из серьезных проблем современности являются нарушения взаимоотношений микро- и макроорганизмов, что во многом определяется состоянием окружающей среды, а также произошедшими изменениями эндоэкологического равновесия в пользу вирусного микроокружения. Вследствие этого персистирующие вирусные инфекции у человека рассматриваются не только как инфекционный процесс, но и как проявление глубоких, в том числе генетических нарушений внутренней среды человека, ведущих к необратимым для него как биологического вида последствиям. Существует мнение о том, что в развитии многих патологических состояний ведущая роль принадлежит вирусам, однако продолжается поиск доказательств характера их участия — либо в роли этиологического фактора, либо триггера.
Снижение иммунной защиты макроорганизма стимулирует реактивацию многих патогенных организмов, которые раньше, до наступления иммунодефицита, находились у человека в скрытом состоянии и внешне никак себя не проявляли. Такие инфекции называются условно-патогенными или оппортунистическими (от англ. opportunity — возможность), и во многих случаях они вызываются внутриклеточными паразитами. По общепринятому определению это инфекции, заражение которыми у здорового (иммунокомпетентного) субъекта не сопровождается патологическими явлениями, но при недостаточности функционирования иммунной системы вызывают заболевания [1].
В начале ХХ века при существующих в то время методах диагностики ведущая роль в заболеваемости принадлежала инфекциям бактериальной природы (скарлатина, дифтерия, коклюш, дизентерия и т.д.). Со второй половины ХХ и начала ХХI веков в этиологии инфекционных заболеваний доминируют вирусы — грипп, ОРВИ, энтеровирусные, ротавирусная, герпетическая инфекции и др. В последние годы в инфекционной патологии все большее значение приобретают герпесвирусы (от греч. herpes — ползти, красться), что связано с их значимой распространенностью в человеческой популяции. Сегодня инфицированность и заболеваемость герпесвирусными инфекциями в общей популяции опережают скорость прироста населения Земли. Более того, среди основных причин неонатальной заболеваемости и смертности ведущее место принадлежит именно герпесвирусным инфекциям [2]. Так, на Национальной конференции по профилактике инфекций, передающихся половым путем, прошедшей в марте 2012 г. в г. Миннеаполисе, США, опубликованы тревожные данные. Летальность при герпесвирусных инфекциях у новорожденных достигает 30 %, а у 20 % выживших детей отмечаются поражения нервной системы. Роль внутриутробных инфекций, среди которых герпесвирусные занимают одно из первых мест, является ведущей в формировании пороков развития. В резолюции конференции отмечено о «…необходимости определения тактики медицинского наблюдения за женщинами с генитальным герпесом во время беременности, что позволит идентифицировать возможные проблемы и направить образовательные усилия в действительно нужное русло» [3].
Более того, по данным ВОЗ, и в будущем среди инфекционной патологии определяющее место будет занимать герпесвирусная инфекция. Это связано с многообразием клинических проявлений, особенностями возбудителей и возможностью их распространения практически всеми известными путями. Герпесвирусы входят в число плохо контролируемых инфекций человека. Они могут циркулировать у человека с нормальной иммунной системой практически бессимптомно, но у людей с иммуносупрессией — активироваться и вызывать тяжелые заболевания со смертельным исходом. Так, мы наблюдаем проявления герпесвирусных инфекций, чаще в виде лабиальных высыпаний, при интеркуррентных респираторных инфекциях.
Герпесвирусная инфекция может существовать у человека в различных формах: пожизненная латентная персистенция, рецидивирующее течение, формирование иммунодефицитов, соматической иммунозависимой патологии, хронического воспаления, опухолевых процессов — и даже встраиваться в генный аппарат. Особенностью течения герпесвирусных инфекций является возможность вовлечения в инфекционный процесс многих органов и систем, чем и обусловлено многообразие вызываемых герпесвирусами заболеваний, варьирующих от простых кожно-слизистых до угрожающих жизни генерализованных инфекций.
Важное свойство герпесвирусов — способность после первичного инфицирования человека в детском возрасте пожизненно персистировать и реактивироваться под влиянием различных экзо- и эндогенных провоцирующих факторов. Герпесвирусная инфекция лучше всего характеризуется одним образным выражением: «Однажды инфицирован — инфицирован на всю жизнь». Появляющиеся в ответ на внедрение вирусов герпеса специфические антитела зачастую не обеспечивают санацию от вирусов и часто не предупреждают рецидива заболевания. В связи с этим перед практикующими врачами — акушерами, педиатрами, терапевтами в первую очередь стоят задачи своевременной диагностики инфекции и определения активности ее течения. Правильная оценка и интерпретация полученных результатов клинического, специфического лабораторного и инструментального исследования позволяют разработать адекватные и наиболее безопасные лечебные и реабилитационные мероприятия для инфицированных и больных — беременной женщины, плода, ребенка, взрослого пациента.
При герпесе, как и при других хронических заболеваниях с вирусной персистенцией, нередко развивается неполноценность иммунных реакций, обусловленная недостаточностью различных звеньев иммунной системы и ее неспособностью элиминировать вирус. Сохраняющиеся в течение всей жизни, иногда в довольно высоких титрах, вируснейтрализующие антитела хотя и препятствуют распространению вирусов, но не предупреждают возникновения рецидивов. Длительное нахождение герпесвирусов у человека становится возможным благодаря сложной стратегии противоборства и «ускользания» от иммунной системы хозяина. В достижении этого состояния можно выделить три пути стратегии возбудителя:
— «тайное присутствие», позволяющее длительно находиться не распознанным иммунной системой, локализуясь в латентном состоянии в нейронах (вирус простого герпеса — ВПГ), лимфоидных (вирус Эпштейна — Барр — ВЭБ) и гемопоэтических клетках (цитомегаловирус — ЦМВ);
— «эксплуатация» — использование иммунных реакций в собственных интересах;
— «саботаж» — повреждение механизмов иммунной защиты.
Именно стратегия «саботажа», как считают, лежит в основе индуцированной вирусом иммуносупрессии, препятствующей полному удалению патогена и, как следствие, поддерживающей хроническое течение инфекции [4].
В настоящее время герпесвирусы четко классифицированы и объединены в обширное семейство Herpesviridae. Семейство Herpesviridae включает в себя более 100 представителей, 8 из которых для человека наиболее патогенны (human herpes virus — HHV). Внешне сходство герпесвирусов настолько велико, что под электронным микроскопом их практически невозможно различить. Индивидуальность «родственников» начинает проявляться только тогда, когда дело доходит до антигенных свойств вирионных белков и степени гомологии ДНК. Герпесвирусы — филогенетически древнее семейство крупных ДНК-вирусов и, в зависимости от типа клеток, в которых протекает инфекционный процесс, характера репродукции вируса, структуры генома, молекулярно-биологических и иммунологических особенностей, подразделяются на 3 подсемейства [5]: a, b и g (табл. 1).
/95.jpg)
Подсемейство Alpha-herpesvirinae (a-герпес–вирусы) включает ВПГ-1, -2 и -3 (Varicella Zoster virus), которые характеризуются быстрой репликацией вируса и цитопатическим действием на культуры инфицированных клеток. Репродукция α-герпесвирусов протекает в различных типах клеток, особенно в эпителиальных, оказывая цитолитическое действие. В нейронах они вызывают латентную персистирующую инфекцию.
Подсемейство Beta-herpesvirinae (b-герпес–вирусы) видоспецифично, поражает различные виды клеток, которые при этом увеличиваются в размерах (цитомегалия), могут вызывать иммуносупрессивные состояния. Инфекция может принимать генерализованную или латентную форму, в культуре клеток легко возникает персистирование инфекции. Вирусы этой группы характеризуются медленным ростом в эпителиальных клетках, оказывая «цитомегалическое» и лимфопролиферативное действие. Вирусы могут поддерживаться в латенции в клетках эпителия слюнных желез, миндалин, почек, лимфоцитах, секреторных железах, почках и других тканях. К этой группе относятся ЦМВ, ВПГ-6, ВПГ-7.
Подсемейство Gamma-herpesvirinae (g-герпес–вирусы) характеризуется тропностью к лимфоидным клеткам (Т- и В-лимфоциты), в которых они длительно персистируют с возможностью трансформироваться, вызывая лимфомы, саркомы. Инфекционный процесс часто останавливается на прелитической стадии, т.е. отсутствует образование вирусных частиц. Латентное потомство обнаруживается в лимфоидной ткани. В эту группу входят вирус Эпштейна — Барр и герпесвирус человека 8-го типа, ассоциированный с саркомой Капоши (KSHV).
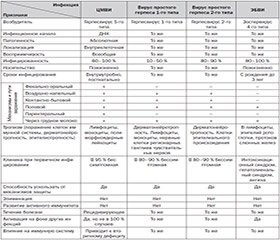
Заболевания, вызываемые ВПГ 1-го и 2-го типа, принято называть герпетической или ВПГ-инфекцией, прочие представители семейства Herpesviridae — герпесвирусными. Представители Herpesviridae, несмотря на многие общие свойства, характерные для всего семейства, имеют и значимые различия (табл. 2).
Сравнивая характеристики герпесвирусов, наиболее часто вызывающих заболевания у человека, обнаруживают большее число однотипных признаков, нежели различий. Так, имеют место одинаковая абсолютная патогенность, одинаковые пути заражения, восприимчивость, склонность к рецидивирующему течению с активацией на фоне интеркуррентных, в т.ч. инфекционных заболеваний, пожизненная персистенция в организме человека и невозможность их полной элиминации, способность «ускользать» от факторов иммунной защиты, в то же время способность подавления защитных функций человека. Вместе с тем имеются и различия: в первую очередь тропизм поражения и клинические характеристики (табл. 2).
Согласно современным воззрениям инфектологии, человек, ввиду своей относительной эволюционной молодости, еще не успел образовать ни с одним из герпесвирусов равновесной системы, что делает их в разной степени патогенными. Однажды заразившись, человек фактически никогда с ними не расстается и всю жизнь как бы носит в себе «неразорвавшуюся бомбу». Разрыв «бомбы» (реактивация «спящего» паразита) может произойти при неблагоприятных ситуациях (стресс, вторичная инфекция, переохлаждение, травма, обострение хронического заболевания и т.д.) даже спустя многие годы, что и наблюдается при латентном течении герпетической и цитомегаловирусной инфекций, хламидиозе, токсоплазмозе, ВИЧ-инфекции и т.д.
Сегодня во многом определена значимость герпесвирусных инфекций в формировании соматических, казалось бы, неинфекционных заболеваний. Нередко при клинически выявленном медленном течении инфекционного процесса, развившемся вследствие герпесвирусной инфекции во внутриутробном периоде, манифестация его проявлений наблюдается не в периоде новорожденности, а в более старшем возрасте. Выявлено, что у большинства детей, умерших в возрасте до 14 лет от различных причин, фоновым заболеванием были именно внутриутробная инфекция и связанное с ней иммунодефицитное состояние. И это диагностировалось только тогда, когда наступил летальный исход. Следовательно, выявление и изучение латентно текущей инфекции, уходящей корнями во внутриутробный период, — актуальная задача не только педиатрии, но и всего здравоохранения. Данный раздел остается самым трудным и практически неизученным [6].
В настоящее время имеется множество свидетельств того, что персистирующие герпесвирусные инфекции являются этиологическим и патогенетическим факторами в развитии хронических соматических заболеваний — кардитов, аритмий сердца, бронхиальной астмы, аутоиммунных процессов, хронических и рецидивирующих обструктивных заболеваний легких, язвенной болезни желудка и двенадцатиперстной кишки, рефрактерных форм хронического гломерулонефрита, сахарного диабета, синдрома хронической усталости, атеросклероза с поражением органов кровообращения, шизо–френии и даже преждевременного старения [7–12]. Многие из этих заболеваний даже в крупных руководствах по-прежнему описываются как идиопатические, неизвестной этиологии.
Появляется все больше данных о роли герпесвирусов в формировании онкологических заболеваний. Еще в 1910 году великий провидец И.И. Мечников печатает в газете «Русское слово» статью, в которой пишет буквально следующее: «Одна причина рака, безусловно, находится в самом организме, но другая попадает в него в виде экзогенного начала, скорее всего — вируса…» В 1911 г. американский ученый Пейтон Раус (1879–1970) обнаружил, что куриная саркома (саркома Рауса) может перевиваться не только клетками, но и субмикроскопическими агентами, экстрагируемыми из клеток, т.е. вызываться вирусами.
В 1933 г. Шоуп открыл вирус папилломы, поражающий кроликов в Северной Америке, в 1936 г. Дж. Биттнер доказал вирусное происхождение рака молочной железы у мышей, в 1951 г. Л. Гроссом открыл вирус лейкоза мышей, в 1964 г. В. Ярретом — вирус лейкоза домашних кошек, а затем и вирус лейкоза обезьян. В 1946 г. советский вирусолог Л.А. Зильбер предложил вирусогенетическую теорию рака [13]. Согласно этой теории, при онкогенезе ДНК вирусного происхождения внедряется (интегрируется) как фрагмент в ДНК клетки и становится составной частью клеточного генома. Эта интеграция — начальное звено в цепи процессов дальнейшего превращения нормальной клетки в раковую. «Каким бы путем опухолеродный вирус ни проник в организм человека, долгое время он ничем не проявляет своего присутствия. В этом нет ничего удивительного. Он мало болезнетворен. Ему нужны особые условия, чтобы проявить болезнетворность, и пока этих условий нет, вирус вполне безобиден» (Л.А. Зильбер). Л.А. Зильбер писал:
«...можно считать доказанным, что механизм действия ДНК или РНК вирусов на клетку заключается в основном в интеграции их нуклеиновой кислоты с геномом клетки, благодаря чему в клетке возникают наследственные изменения, выводящие клетку из соподчинения системам, регулирующим клеточный рост» [13].
В настоящее время установлено, что к вирусам, причастным к раковым заболеваниям человека, относятся ДНК-содержащие вирусы, в частности вирусы Эпштейна — Барр и другие герпесвирусы. Вирус Эпштейна — Барр присутствует в клетках 10–20 % от всех раковых опухолей желудка. Маркеры вирусов простого герпеса 1-го и 2-го типов, цитомегаловируса, вируса Эпштейна — Барр и вируса герпеса человека 6-го типа обнаружены в крови и костном мозге большинства больных острыми лейкозами в период индукционной полихимиотерапии [14].
В ходе масштабного исследования возбудителей инфекционных заболеваний, отнесенных Международным агентством по изучению рака (International Agency for Research on Cancer, Лион, Франция) к разряду канцерогенных для человека, выявлено, что из 12,7 млн впервые выявленных случаев злокачественных опухолей, имевших место в 2008 г., доля инфекционно-обусловленных случаев составила 16,1 %, т.е. около 2 млн. У женщин рак шейки матки составил около половины случаев инфекционно-обусловленных вспышек раковых заболеваний, у мужчин рак желудка и печени составил более 80 %. С герпесвирусами (ВЭБ) были связаны злокачественные новообразования носоглотки, неходжкинская лимфома, саркома Капоши [15].
Многообразие патологических процессов и различных заболеваний, связанных с персистирующими внутриклеточными патогенами, в том числе и с герпесвирусами, явилось основанием того, что в 2003 году Европейское региональное бюро ВОЗ отнесло группу персистирующих внутриклеточных инфекций к числу болезней, определяющих будущее как инфекционной, так и соматической патологии человеческой популяции.
Еще несколько десятков лет назад ведущими среди причин детской заболеваемости и смертности были острые инфекции. Грипп, кишечные, менингококковые инфекции, сепсис, пневмонии, инфекции мочевыводящих путей и связанные с ними заболевания были основной патологией, определяющей продолжительность жизни как детского, так и взрослого населения. Прошло совсем немного времени, и человечество вооружилось мощнейшими противоинфекционными средствами, среди которых основными стали антибиотики и вакцины. И теперь диагнозы «холера», «чума», «сепсис», «менингит», «пневмония» уже не являются смертным приговором для больного. Сегодня в большинстве случаев возможно не только излечение, более того, можно предотвратить само заболевание, вызванное этими инфекциями. Человечество начало смотреть в будущее с надеждой на избавление от инфекционных заболеваний. Наша самоуверенность дошла до того, что в 60–70-х годах прошлого века, т.е. 40–50 лет тому назад, известные ученые публично заявляли о конце века инфекций: «…книгу инфекций можно закопать глубоко в землю, они теперь не страшны…» Ведь практически побеждена страшная «испанка» начала ХХ века, унесшая больше жизней, чем Первая мировая война, уходят как страшный сон обездвиженность полиомиелита, малярийные ознобы, столбняк и многие страшные проявления инфекций.
Но полыхнула «стафилококковая чума», пришли «забытые» полиомиелит, дифтерия; грянули ВИЧ и СПИД, лихорадка Эбола, птичий и свиной грипп и т.д. А сегодня это герпесвирусные инфекции, и их роль во влиянии на здоровье человека еще предстоит узнать. Ведь знаем мы об этих весьма распространенных инфекциях еще крайне мало, да и к науке об окружающем нас микро- и макромире лишь прикоснулись, причем только к ее самому близкому краю. Сегодня мы не имеем общепринятых подходов к диагностике заболеваний, связанных с герпесвирусными инфекциями, не разработаны достоверные критерии, показания и характер проведения рациональной и адекватной терапии, а также отсутствуют достаточно эффективные лекарственные средства, проникающие внутрь клетки и способные к нейтрализации данной группы патогенов. Надеемся в цикле статей по проблемам герпесвирусных инфекций в какой-то мере ответить на некоторые, наиболее часто задаваемые вопросы.
Список литературы
1. Редфилд Р.Р., Берке Д.С. // В мире науки. — 1988. — № 12. — С. 60-69.
2. Кравченко Л.В. Состояние иммунной системы у детей первых месяцев жизни с герпесвирусной инфекцией // Педиатрия. — 2008. — Т. 87, № 1. — С. 52-58.
3. National STD Prevention Conference: Abstract C1.1. Presented March 14, 2012.
4. Лындин А.А. Герпесвирусная инфекция и ее роль в поражении почек // Рос. вест. перинат. и педиатрии. — 2010. — № 6. — С. 69-75.
5. Кускова Т.К., Белова Е.Г. Семейство герпесвирусов на современном этапе // Оппортунистические инфекции: проблемы и перспективы / Под общ. ред. проф. Ю.В. Редькина. — Омск: Омская медицинская академия, 2005. — 100 с.
6. Учайкин В.Ф. Решенные и нерешенные проблемы инфекционной патологии у детей // Педиатрия. — 2004. — № 4. — С. 7-11.
7. Смелянская М.В., Перемот С.Д., Мартынов А.В. Персистирующие герпесвирусные инфекции как потенциальный триггер-фактор соматических заболеваний // Annals of Mechnicov Institute. — 2006. — № 4. — С. 29-33.
8. Kyto V., Vuorinen T., Saukko P., Lautenschlager I., Lignitz E., Saraste A., Voipio-Pulkki L.M. Cytomegalovirus infection of the heart is common in patients with fatal myocarditis // Clin. Infect. Dis. — 2005. — 40(5). — 683-8.
9. Appleton A.L., Sviland L. Pathigenesisof GVHD: Role of herpes virus // Bone Marrow Transplant. — 1993. — Vol. 115. — P. 349-355.
10. Braun Z.A. Neonatal herpes simplex virus infection in relation to asymptomatic material infection at the time of labor // N. Engl. J. Med. — 2001. — 324. — 1247-1252.
11. Нагорная Н.В., Юлиш Е.И., Пшеничная Е.В., Виноградов К.В. Значение герпесвирусной инфекции в кардиальной патологии детского возраста // Современная педиатрия. — 2007. — 3(16). — С. 153-158.
12. Нагорная Н.В., Юлиш Е.И., Виноградов К.В., Пшеничная Е.В. Роль герпесвирусной инфекции в кардиальной патологии у детей // Современная педиатрия. — 2007. — 2(15). — С. 115-118.
13. Зильбер Л.А. Основы иммунитета. — М., 1948. — 423 с.
14. Тихомиров Д.С., Гаранжа Т.А., Троицкая В.В., Суворова П.А., Ярославцева Н.Г., Туполева Т.А., Грумбкова Л.О., Игнатова Е.Н., Романова Т.Ю., Филатов Ф.П., Савченко В.Г. Лабораторная диагностика герпесвирусных инфекций у больных острыми лейкозами // Вопросы вирусологии. — 2009. — № 1.
15. De Martel C., Ferlay J., Franceschi S., Vignat J., Bray F., Forman D., Plummer M. Global burden of cancers attributable to infections in 2008: a review and synthetic analysis // Lancet Oncol. — Published online May 8.

/95.jpg)
/96.jpg)