Статтю опубліковано на с. 11-15
Вступ
Серед захворювань раннього дитячого віку одне з провідних місць посідає патологія органів травлення [2, 4, 5, 13]. В Україні середній показник поширеності гастроентерологічних захворювань серед дітей за період з 1990 р. до 2012 р. виріс майже на 42,2 %, а захворюваність за цей же період — на 22,6 ‰. Серед них особливу роль відіграють захворювання та стани, пов’язані з гастроінтестинальними розладами внаслідок харчової непереносимості (ХН) [6, 8]. Причому останніми десятиріччями відмічається поширення не лише реакцій непереносимості продуктів харчування, а й посилення ступеня їх тяжкості. Складність цієї проблеми полягає в тому, що непереносимість харчових продуктів може бути обумовлена різними механізмами [1, 16, 17]. З одного боку, це алергічна реакція на компоненти їжі, що призводить до розвитку алергічного запалення — якісно нової форми реагування кишечника [11]. З іншого боку, харчова непереносимість може бути обумовлена наявністю супутніх захворювань, таких як порушення процесів травлення та всмоктування харчового субстрату, інфекції, спадкові або набуті порушення ферментних систем тощо [8, 9].
Клінічно ХН у дітей перших місяців життя незалежно від етіологічного фактора (харчова алергія, недостатність лактози (НЛ), дисбактеріоз кишечника) проявляється у вигляді порушень з боку шлунково-кишкового тракту (ШКТ) — зригування, блювання, метеоризму, кишкових кольок (КК), діареї, запорів, неспокою після прийому їжі. Одним з найбільш частих проявів ХН у дітей грудного віку є кишкові кольки [2, 5, 6].
Малюкові кишкові кольки — найбільш частий симптом, що турбує батьків немовляти та зустрічається при багатьох функціональних та органічних захворюваннях ШКТ. Вони реєструються у 10–15 %, а за деякими даними — у 30–70 % немовлят. За даними Ю.В. Білоусова, поширеність КК серед дітей перших місяців життя становить від 5 до 19 % у доношених та близько 70 % — у недоношених дітей. КК проявляються раптовими і вираженими нападами плачу й неспокою немовлят протягом 3 і більше годин упродовж доби не менше від 3 днів на тиждень протягом хоча б одного тижня.
Особливу стурбованість викликає поширеність гастроінтестинальних розладів, пов’язаних із харчовою непереносимістю, у дітей грудного та раннього віку, які, за даними різних досліджень, становлять 60–65 % [6, 7, 13]. Порушення моторики шлунково-кишкового тракту при ХН у дітей раннього віку супроводжується синдромами мальдигестії та мальабсорбції, пов’язаними з порушенням зовнішньосекреторної функції підшлункової залози, що потребують призначення поліферментних препаратів [3, 9–11].
Для корекції недостатності травлення при порушеннях моторики в дітей різного віку сьогодні все ширше застосовуються дієтичні добавки, що містять різні харчові та фітокомпоненти. Так, дієтична добавка Санзим сироп (Pharco Pharmaceuticals, Єгипет), що являє собою комбіновану форму специфічних травних ферментів (пепсин — 800 мг, папаїн — 1600 мг та мультиензимний комплекс санзим 2000 — 200 мг у 100 мл сиропу), сприяє розщепленню білків, жирів, вуглеводів та рослинних волокон. Протеолітичний фермент, отриманий з плодів та листя папаї (динне дерево), — папаїн каталізує гідроліз білків, пептидів, амідів і естерів. За своєю фізіологічною дією він схожий на пепсин, але на відміну від пепсину активний не лише в кислих, а й у нейтральних та лужних середовищах (діапазон рH 3–12, оптимум рH 5), зберігає активність у широкому температурному діапазоні. Санзим 2000 — мультиензимний комплекс, отриманий із гриба Aspergillus oryzae. Цей комплекс складається з більше ніж 30 ферментів: протеази, ліпази, рибонуклеази, пектинази тощо й використовується для нормалізації травлення, сприяє завершенню гідролізу. Добавка не містить алкоголю й не впливає на сапрофітну кишкову мікрофлору. В Україні Санзим сироп раніше був відомий як лікарський засіб з торговою назвою Дигестин і добре зарекомендував себе в лікуванні дітей, у тому числі раннього віку, з патологією органів травлення. З огляду на вищезазначене метою нашої роботи було визначення ефективності застосування поліферментної дієтичної добавки Санзим сироп у комплексному лікуванні дітей раннього віку з гастроінтестинальними проявами харчової непереносимості.
Матеріали і методи
Оцінка ефективності дієтичної добавки проведена у складі комплексної терапії недостатності травлення у 70 дітей віком від 3 місяців до 3 років з ХН протягом 14 днів (немовлята з 3 місяців до 1 року отримували по 8–15 крапель тричі на добу під час або одразу після їжі, діти від 1 до 3 років — 1 чайну ложку тричі на добу під час або одразу після їжі).
Критеріями включення були синдром мальабсорбції у хворих із ХН, що проявлялась змінами консистенції і частоти випорожнень, наявністю домішок крові та слизу у випорожненнях; порушеннями моторики верхніх відділів ШКТ; атопічним дерматитом.
Клінічна ефективність застосування дієтичної добавки оцінювалась у динаміці за інтенсивністю клінічних проявів кишкових кольок, метеоризму, зригувань та динамікою нутритивного статусу, а також за показниками результатів копрологічного дослідження.
Методом простої рандомізації діти були поділені на дві групи: основну групу становили 45 дітей, які у складі комплексної терапії гастроінтестинальних розладів отримували поліферментну дієтичну добавку, контрольну групу — 25 дітей, які отримували стандартну терапію, що включала: дієтотерапію (безлактозні суміші, у разі НЛ при грудному вигодовуванні — замісна ферментотерапія (лактаза), елімінаційна дієта, прокінетики (домперидон), цитопротектори, спазмолітики, препарати симетикону, антигістамінні препарати).
Серед дітей основної групи 27 пацієнтів мали недостатність лактози та 18 пацієнтів — гастроінтестинальну харчову алергію (ГХА). Контрольну групу становили 15 дітей з НЛ та 10 дітей з ГХА.
Ефективність лікування оцінювали на підставі динаміки скарг, об’єктивних даних, результатів копрологічного дослідження в динаміці на 3, 7, 14-й день лікування.
Реєстрація суб’єктивних скарг та об’єктивних даних проводилась за бальною системою з урахуванням ступеня їх інтенсивності: 0 балів — відсутність прояву (ознаки) симптому; 1 бал — слабкий ступінь прояву (ознаки) симптому; 2 бали — помірний ступінь та 3 бали — значний ступінь прояву (ознаки) симптому.
Обробку отриманих результатів проводили загальноприйнятими математичними методами варіаційної статистики.
Оцінка безпечності застосування поліферментної дієтичної добавки проводилась на підставі аналізу її переносимості за суб’єктивними даними щодо стану дитини, що повідомлялись батьками, та за результатами об’єктивного спостереження.
Результати дослідження
При обстеженні на початку дослідження інтенсивні та тривалі КК були виявлені в переважної більшості дітей як із ЛН, так і з ГХА. Крім того, внаслідок розладів роботи ШКТ та погіршення самопочуття дітей при ХН у більшості із них мали місце зменшення добового об’єму спожитої їжі, незадовільна прибавка маси тіла, порушення з боку нервової системи, зменшення середньодобової тривалості сну та його глибини.
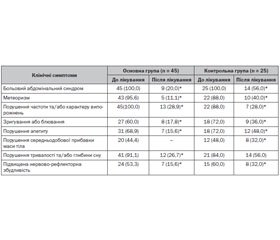
При ХН у більшості випадків КК у дітей поєднувались із вираженими клінічними проявами метеоризму, змінами частоти та характеру випорожнень, зригуванням або блюванням (табл. 1).
Як свідчать результати обстеження після лікування, у більшості (91,1 %) дітей основної групи відмічалась тенденція до більш швидкого зменшення больового абдомінального синдрому порівняно з контрольною групою (p = 0,07). При цьому больовий абдомінальний синдром та метео-ризм повністю зникли в основній групі у 36 (80 %) та у 38 (84,4%) пацієнтів відповідно (табл. 1).
Крім того, серед дітей основної групи наприкінці дослідження вірогідно нижчим був відсоток дітей із зригуваннями або блюванням, порушенням апетиту. У всіх дітей основної групи середньодобова прибавка маси тіла відповідала віковій нормі.
В основній групі відмічено також покращення неврологічного статусу дітей. При опитуванні матерів основної групи 12 (91,1 %) із них на початку дослідження відмічали порушення характеру сну дітей (уривчастий, нетривалий, неглибокий). Після проведеного лікування в більшості дітей сон нормалізувався, а дітей із порушеннями сну було тільки 22,2 %, у той час як у групі контролю порушення сну зберігались у 56 % дітей.
Крім того, у більшості дітей основної групи при огляді після курсу лікування відмічено зменшення або зникнення проявів підвищеної нервово-рефлекторної збудливості.
Зменшення інтенсивності та тривалості КК, інтенсивності метеоризму в переважної більшості дітей основної групи було відмічене батьками вже на 3-тю добу прийому препарату. Лікування дітей основної групи дозволило також значно зменшити тривалість та частоту епізодів кольок протягом доби (табл. 2).
Клінічна характеристика кишкових кольок у порівнюваних групах подана в табл. 2.
Клінічне обстеження дітей контрольної групи показало, що зменшення інтенсивності та тривалості КК у них відбувалось повільніше (p = 0,09). Так, на 3-тю добу лікування інтенсивність КК у цій групі зберігалось на рівні 2,25 ± 0,22 бала, на 7-му добу — 1,9 ± 0,1 бала, і тільки на 14-ту добу лікування поряд із покращенням стану дитини та зникненням клінічних проявів ХН внаслідок лікування основного захворювання було відмічено також зменшення інтенсивності КК до 1,55 ± 0,12 бала, у той час як кількість епізодів та тривалість кольок протягом доби залишились на досить високому рівні (табл. 2).
Обстеження дітей у динаміці лікування показало, що призначення пацієнтам поліферментної дієтичної добавки (основна група) сприяє більш значному та швидкому зменшенню частоти та інтенсивності КК порівняно із групою пацієнтів, які його не отримували (контрольна група), що свідчить про виражений терапевтичний ефект даного лікувального засобу.
Аналіз показників копрограми обстежених пацієнтів з ХН виявив численні неперетравлені м’язові волокна (креаторея), нейтральний жир (стеаторея), велику кількість крохмальних зерен (амілорея) (табл. 3).
Прийом поліферментної дієтичної добавки сприяв зникненню стеатореї в 43 пацієнтів (95,5 %), креатореї — у 40 дітей (88,9 %), амілореї — у 37 (82,2 %) хворих, що свідчить про значне покращення процесів травлення.
Індивідуальна переносимість поліферментної дієтичної добавки була доброю у всіх 45 дітей основної групи. У процесі лікування не було відмічено алергічних або інших негативних реакцій на прийом поліферментної дієтичної добавки, у тому числі не було виявлено алергічних реакцій або посилення клінічної симптоматики захворювання у дітей з ГХА.
Висновки
1. Призначення поліферментної дієтичної добавки Санзим сироп дітям раннього віку з ХН (із недостатністю лактози та гастроінтестинальною харчовою алергією) підвищує ефективність терапії у 91,1 % хворих, що клінічно проявляється зменшенням проявів абдомінального больового синдрому, кольок, зригувань, метеоризму, нервово-рефлекторної збудливості та покращенням процесів травлення за результатами копрологічного дослідження у вигляді зникнення стеатореї у 43 пацієнтів (95,5 %), креатореї — у 40 дітей (88,9 %), амілореї — у 37 (82,2 %).
2. Призначення поліферментної дієтичної добавки Санзим сироп дітям раннього віку з гастроінтестинальними проявами харчової непереносимості у вікових дозах (немовлятам — з 3 місяців до 1 року — 8–15 крапель тричі на добу під час або одразу після їжі, дітям від 1 до 3 років — 1 чайна ложка тричі на добу під час або одразу після їжі протягом 14 днів) не викликає розвитку побічних реакцій.
Список литературы
1. Абдоминальный болевой синдром у детей с лактазной недостаточностью / Нагорная Н.В., Бордюгова Е.В., Дубовая А.В., Дудчак А.П. // Современная педиатрия. — 2014. — № 1 (57). — С. 106-112.
2. Аряев Н.Л., Кожевин Р.В. Младенческая кишечная колика: современные подходы к лечению // Современная педиатрия. — 2010. — № 5 (33). — С. 162-166.
3. Безкаравайный Б.А. Синдром мальабсорбции у детей: поиск новых способов лечения / Б.А. Безкаравайный, А.Н. Волошин, Г.Г. Бондаренко, И.Ю. Митякина, О.П. Неженцева // Современная педиатрия. — 2010. — № 6. — С. 87-89.
4. Белоусова Е.А. Синдром избыточного бактериального роста тонкой кишки при хроническом панкреатите // РМЖ. — 2009. — Т. 17, № 5. — С. 317-322.
5. Беляева И.А. Новые возможности комплексной терапии кишечных колик у грудных детей / И.А. Беляева, Г.В. Яцык, А.Н. Евдокимова // Педиатрия. — 2011. — № 90 (2). — С. 231-241.
6. Бережний В.В. Кишкові кольки в дітей раннього віку та методи корекції: Нац. підр. з педіатрії / В.В. Бережний, В.Г. Козачук; за ред. В.В. Бережного. — К., 2013. — 1040 с.
7. Корниенко Е.Ф., Вагеманс Н.В., Нетребенко О.К. Младенческие кишечные колики: современные представления о механизмах развития и новые возможности терапии // Современная педиатрия. — 2010. — № 5(33). — С. 176-183.
8. Проблемні питання перебігу та терапії лактазної недостатності у дітей раннього віку / Шадрін О.Г., Марушко Т.Л., Місник В.П. [та ін.] // Совр. педиатрия. — 2011. — № 6. — С. 157-161.
9. Сенаторова А.С., Урываева М.К. Синдром мальабсорбции у детей. Диагностика, дифференциальный диагноз, лечение // Здоровье ребенка. — 2010. — № 5(26).
10. Синдром избыточного газообразования у детей / Абатуров А.Е., Агафонова Е.А., Русакова Е.А., Петренко Л.Л., Ивашина В.И. // Здоровье ребенка. — 2012. — № 6 (41). — С. 149-153.
11. Ткач С.М., Сизенко А.К. Синдром мальабсорбции: новая классификация, основные причины и механизмы развития // Сучасна гастроентерологія. — 2012. — № 3(65). — С. 114-121.
12. Уніфіковані клінічні протоколи медичної допомоги дітям із захворюваннями органів травлення: Наказ МОЗ України № 59 від 29 січня 2013 р. [Електронний документ]. — Режим доступу: http://www.moz.gov.ua. — Назва з екрана.
13. Шадрін О.Г. Гастроентерологія дітей раннього віку: Навч.-метод. посібник / О.Г. Шадрін, О.М. Муквіч. — К., 2010. — С. 88-90.
14. Applying case definition criteria to irritable bowel syndrome / Yale S.H., Musana A.K., Kieke A. [et al.] // Clin. Med. Res. — 2008. — Vol. 6, № 1. — P. 9-16.
15. Damaso Infante Dietary treatment of colic caused by excess gas in infants: Biochemical evidence / Damaso Infante, Oscar Segarra, Bernard Le Luyer // World J. Gastroenterol. — 2011. — Vol. 17 (16). — P. 2104-2108. — Published online Apr. 28, 2011.
16. Montalto M., Santoro L., D’Onofrio F., Curiglano V. Classification of Malabsorption syndromes // Dig. Dis. — 2008. — Vol. 26. — P. 104-111.
17. World Gastroenterology Organisation (WGO) Practice Guideline: Malabsorption. — Режим доступу: http://www.worldgastroenterology.org; cited 29 Feb 2012.

/13.jpg)
/14.jpg)