Журнал «Здоровье ребенка» 3 (71) 2016
Вернуться к номеру
Застосування кристалоїдних розчинів в інфузійнiй терапії у дітей (огляд літератури)
Авторы: Снісарь В.І., Єгоров С.В. - Дніпропетровська медична академія МОЗ України, м. Дніпро, Україна
Рубрики: Педиатрия/Неонатология
Разделы: Справочник специалиста
Версия для печати
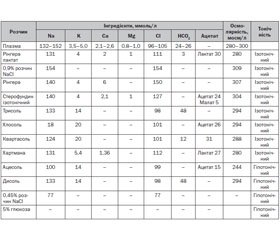
Внутрішньовенна інфузійна терапія останнім часом активно розвивається. Рекомендації M.A. Holliday, W.E. Segar, що лягли в основу проведення рідинної терапії, призвели до переважного використання гіпотонічних розчинів. Гіпонатріємія, що часто розвивається у дітей і має ряд серйозних ускладнень, була викликана в основному їх використанням. Щоб уникнути розвитку гострої гіпонатріємії, було рекомендовано внутрішньовенне введення 0,9% розчину NaCl. Однак кислотно-основні порушення внаслідок розвитку гіперхлоремічного ацидозу обмежують його застосування. Останніми роками створюються й активно застосовуються розчини, що не тільки сприяють корекції водного балансу, електролітних порушень, кислотно-основного стану, але і мають органопротективний ефект, що, безумовно, дуже важливо. Тому використання збалансованих сольових розчинів як ізотонічної рідини вибору повинно мати перевагу перед уведенням 0,9% фізіологічного розчину. Мета даного огляду — надати короткий виклад сучасної концепції внутрішньовенного введення рідини в педіатричних відділеннях інтенсивної терапії. Викладено певні постулати, яких потрібно дотримуватися, призначаючи дитині внутрішньовенне введення рідини. Описано певні переваги та недоліки сольових розчинів, які застосовуються у дітей. Більшою мірою порівнюється 0,9% розчин NaCl із збалансованим ізотонічним сольовим розчином стерофундин, який має концентрацію натрію 140 ммоль/л і значно більш низьку концентрацію хлориду — 127 ммоль/л, а також він містить калій, магній, що більше наближено до складу плазми. В огляді наведені дані щодо сольового розчину Рінгер-лактат, який має дещо знижену концентрацію натрію (131 ммоль/л) порівняно з нормальним фізіологічним розчином і стерофундином. Низька концентрація натрію і вміст лактату дещо обмежують його застосування, особливо при нейрохірургічній патології.
Внутривенная инфузионная терапия в последнее время активно развивается. Рекомендации M.A. Holliday, W.E. Segar, которые легли в основу проведения жидкостной терапии, привели к преимущественному использованию гипотонических растворов. Гипонатриемия, которая часто развивается у детей и имеет ряд серьезных осложнений, была вызвана в основном их использованием. Во избежание развития острой гипонатриемии рекомендовано внутривенное введение 0,9% раствора NaCl. Однако кислотно-основные нарушения вследствие развития гиперхлоремического ацидоза ограничивают его применение. В последние годы создаются и активно применяются растворы, не только способствующие коррекции водного баланса, электролитных нарушений, кислотно-основного состояния, но и обладающие органопротективным эффектом, что, безусловно, очень важно. Поэтому использование сбалансированных солевых растворов в качестве изотонической жидкости выбора имеет преимущество перед введением 0,9% физиологического раствора. Цель данного обзора — предоставить краткое изложение современной концепции внутривенного введения жидкости в педиатрических отделениях интенсивной терапии. Изложены определенные постулаты, которых нужно придерживаться, назначая ребенку внутривенное введение жидкости. Описаны определенные преимущества и недостатки солевых растворов, применяющихся у детей. В большей степени сравнивается 0,9% раствор NaCl с сбалансированным изотоническим солевым раствором стерофундин, имеющим концентрацию натрия 140 ммоль/л и значительно более низкую концентрацию хлорида — 127 ммоль/л, а также он содержит калий, магний, что более приближено к составу плазмы. В обзоре представлены данные о солевом растворе Рингера лактат, который имеет сниженную концентрацию натрия (131 ммоль/л) в сравнении с нормальным физиологическим раствором и стерофундином. Низкая концентрация натрия и содержание лактата ограничивают его применение, особенно при нейрохирургической патологии.
Intravenous infusion therapy recently has a significant upward trend. Recommendations of M.A. Holliday, W.E. Segar included in the basis of fluid therapy led to predominant use of hypotonic solutions. Hyponatremia, which often develops in children and has a number of serious complications, was caused mainly by using them. To prevent the development of acute hyponatremia, it was recommended intravenous administration of 0.9% NaCl solution. However, acid-base disorders due to the development of hyperchloremic acidosis limit its use. In recent years, there are created and actively used solutions that not only help to correct fluid balance, electrolyte disorders, acid-base status, but also have organ-protective effect, which is certainly very important. Therefore, the use of balanced salt solutions as isotonic fluid of choice should take precedence over the introduction of 0.9% saline. The objective of this review — to provide a summary of the current concept of intravenous fluid administration in pediatric intensive care units. Certain tenets to be followed, when prescribing intravenous fluid to a child, are presented. We describe certain advantages and disadvantages of salt solutions, which are used in children. 0.9% NaCl solution is mainly compared with a balanced isotonic saline sterofundin, which has a concentration of sodium 140 mmol/l and significantly lower chloride concentration — 127 mmol/l, as well as potassium, magnesium that is more close to the composition of plasma. The review contains data on lactated Ringer’s solution, which has a somewhat lower concentration of sodium (131 mmol/l) compared to a normal saline and sterofundin. The low concentration of sodium and lactate content somewhat limit its use, especially in neurosurgical pathologies.
діти, збалансовані сольові розчини, внутрішньовенна інфузія рідини.
дети, сбалансированные солевые растворы, внутривенная инфузия жидкости.
children, balanced salt solutions, intravenous fluid infusion.
Статтю опубліковано на с. 128-135
Актуальність
Аналіз досліджень та обговорення
Кристалоїдні розчини
Висновок
1. Arieff A.I. Hyponatraemia and death or permanent brain damage in healthy children / A.I. Arieff, J.C. Ayus, C.L. Fraser // BMJ. — 1992. — Vol. 304, № 6836. — P. 1218-22.
2. Hypotonic versus isotonic saline in hospitalised children: A systematic review / K. Choong, M.E. Kho, K. Menon, D. Bohn // Arch. Dis. Child. — 2006. — Vol. 91, № 10. — P. 828-35.
3. Acute hyponatremia related to intravenous fluid administration in hospitalized children: An observational study / E.J. Hoorn, D. Geary, M. Robb, M.L. Halperin [et al.] // Pediatrics. — 2004. — Vol. 113, № 5. — P. 1279-1284.
4. Hyponatremia-related death after paediatric surgery still exists in France / Y. Auroy, D. Benhamou, F. Péquignot, E. Jougla [et al.] // Br. J. Anaesth. — 2008. — Vol. 101, № 5. — P. 741.
5. McRae R.G. Iatrogenic hyponatremia: A cause of death following pediatric tonsillectomy / R.G. McRae, A.J. Weissburg, K.W. Chang // Int. J. Pediatr. Otorhinolaryngol. — 1994. — Vol. 30, № 3. — P. 227-232.
6. Duke T. Hyponatremia and seizures in oncology patients associated with hypotonic intravenous fluids / T. Duke, S. Kinney, K. Waters // J. Paediatr. Child. Health. — 2005. — Vol. 41, № 12. — P. 685-686.
7. Plain D5W or hypotonic saline solutions post-op could result in acute hyponatremia and death in healthy children. ISMP Med Saf Alert 2009 Aug 13 [cited 2009 Sept 15]; 14(16): 1-4 http://ismp.org/newsletters/acutecare/articles/20090813.asp (Accessed August 7, 2012).
8. Hyponatremia in children. Ottawa (ON): Canadian Medical Protective Association; 2008 Dec: IL0840-1-E [cited 2009 Sept 16]: http://www.cmpa-acpm.ca/cmpapd04/docs/resource_files/infoletters/2008/com_il0840_1-e.cfm (Accessed August 7, 2012).
9. Report of the Paediatric Death Review Committee and Deaths Under Five Committee, Toronto (ON) // Office of the chief Coroner Province of Ontario. — Toronto, 2007. — P. 19-20.
10. Paediatric Research Society. Hyponatremia and hypokalemia during intravenous fluid administration / K. Armon, A. Riordan, S. Playfor [et al.] // Arch. Dis. Child. — 2008. — Vol. 93, № 4. — P. 285-287.
11. Moritz M.L. Prevention of hospital-acquired hyponatremia: A case for using isotonic saline / M.L. Moritz, J.C. Ayus // Pediatrics. — 2003. — Vol. 111. — P. 227-230.
12. Halberthal M. Lesson of the week: Acute hyponatraemia in children admitted to hospital; Retrospective analysis of factors contributing to its development and resolution / M. Halberthal, M.L. Halperin, D. Bohn // BMJ. — 2001. — Vol. 322, № 7289. — P. 780-782.
13. Holliday M.A. The maintenance need for water in parenteral fluid therapy / M.A. Holliday, W.E. Segar // Pediatrics. — 1957. — Vol. 19, № 5. — P. 823-832.
14. Александрович Ю.С. Современные принципы инфузионной терапии в педиатрической практике / Ю.С. Александрович, В.И. Гордеев, К.В. Пшениснов // Российский вестник детской хирургии, анестезиологии и реаниматологии. — 2011. — № 3.
15. Steurer M.A. Infusion therapy for neonates, infants and children / M.A. Steurer, T.M. Berger // Anaesthesist. — 2011. — P. 13.
16. Holliday M.A. Reducing errors in fluid therapy management / M.A. Holliday, W.E. Segar, A. Friedman // Pediatrics. — 2003. — Vol. 111, № 2. — P. 424-425.
17. Rapid saline infusion produces hyperchloremic acidosis in patients undergoing gynecologic surgery / S. Scheingraber, M. Rehm, C. Sehmisch, U. Finsterer // Anesthesiology. — 1999. — Vol. 90, № 5. — P. 1265-1270.
18. The effect of different crystalloid solutions on acid-base balance and early kidney function after kidney transplantation / N. Ha–dimioglu, I. Saadawy, T. Saglam, Z. Ertug [et al.] // Anesth. Analg. — 2008. — Vol. 107. — P. 264-269.
19. Normal saline versus lactated Ringer's solution for intra-operative fluid management in patients undergoing abdominal aortic aneurysm repair: an outcome study / A. Gottlieb, P. Schoenwald, M. Popovich, J. Sprung [et al.] // Anesth. Analg. — 2001. — Vol. 93. — P. 817-822.
20. Houghton J. Choice of isotonic perioperative fluid in children / J. Houghton, N. Wilton // Anesth. Analg. — 2011. — Vol. 112, № 1. — P. 246-247.
21. Beck C.E. Hypotonic versus isotonic maintenance intravenous fluid therapy in hospitalized children: A systematic review / C.E. Beck // Clin. Pediatrics. — 2007. — Vol. 46, № 9. — P. 764-770.
22. Burrows F.A. Inappropriate secretion of antidiuretic hormone in a postsurgical pediatric population / F.A. Burrows, J.G. Shutack, R.K. Crone // Crit. Care Med. — 1983. — Vol. 11, № 7. — P. 527-531.
23. Brazel P. Inappropriate secretion of antidiuretic hormone in postoperative scoliosis patients: The role of fluid management / P. Brazel, I.B. McPhee // Spine. — 1996. — Vol. 21, № 6. — P. 727.
24. Isotonic is better than hypotonic saline for intravenous rehydration of children with gastroenteritis: A prospective randomized study / K.A. Neville, C.F. Verge, A.R. Rosenberg [et al.] // Arch. Dis. Child. — 2006. — Vol. 91, № 3. — P. 226-232.
25. The use of isotonic fluid as maintenance therapy prevents iatrogenic hyponatremia in pediatrics: A randomized, controlled open study / P.A. Montañana, V. Modesto, V. Alapont, A.P. Ocón [et al.] // Pediatr. Crit. Care. Med. — 2008. — Vol. 9, № 6. — P. 589-597.
26. Yung M. Randomised controlled trial of intravenous maintenance fluids / M. Yung, S. Keeley // J. Paediatr. Child. Health. — 2009. — Vol. 45, № 1–2. — P. 9-14.
27. Hypotonic versus isotonic maintenance fluids in critically ill children: A multicenter prospective randomized study / C. Rey, M. Los-Arcos, A. Hernández [et al.] // Acta Paediatrica. — 2011. — Vol. 100, № 8. — P. 1138-1143.
28. Intravenous fluid regimen and hyponatremia among children: A randomized controlled trial / L. Kannan, R. Lodha, S. Vivekanandhan [et al.] // Pediatr. Nephrol. — 2010. — Vol. 25, № 11. — P. 2303-2309.
29. Hypotonic versus isotonic maintenance fluids after surgery in children: A randomized controlled trial / K. Choong, S. Arora, J. Cheng [et al.] // Pediatrics. — 2011. — Vol. 128, № 5. — P. 857-866.
30. A randomized controlled trial of isotonic versus hypotonic maintenance intravenous fluids in hospitalized children / T.G. Saba, J. Fairbairn, F. Houghton [et al.] // BMC Pediatrics. — 2011. — Vol. 11. — P. 82.
31. Perioperative Crystalloid and Colloid Fluid Managementin Children: Where Are We and How Did We Get Here? / A.G. Bailey, P.P. McNaull, E. Jooste, J.B. Tuchman // Pediatric Anesthesiology. — 2010. — Vol. 110, № 2.
32. Royal Children’s Hospital Melbourne. Clinical practice guidelines / Intravenous fluids. — 2013.
33. Hospital for Sick Children, Toronto. Clinical practice guidelines/Fluid and electrolyte administration in children, 2007 [revised June 2010; reviewed January 2011]: http://www.sickkids.ca/clinical-practice-guidelines/clinical-practice-guidelines/Fluid-and-Electrolyte-Administration-in-Children.html (Accessed August 2, 2012).
34. National Patient Safety Agency. Background information, Patient safety alert 22: Reducing the risk of hyponatraemia when administering intravenous infusions to children. London (UK), March 2007: http://www.nrls.npsa.nhs.uk/resources/?entryid45=59809 (Accessed August 13, 2012).
35. Dodge С. Crystalloid and colloid therapy / С. Dodge, D.D. Glass // Semin. Anesth. — 1982. — № 1. — P. 293-301.
36. Tranbaugh R.F. Crystalloid fluid / R.F. Tranbaugh, F.R. Lewis // Dailey R.H., Callaham M. Controversies in trauma management. Clinics in emergency medicine. — Churchill Livingstone, 1985. — P. 121-133.
37. Shackford S.R. Fluid resuscitation of the trauma victim / S.R. Shackford, A. Perel // Trauma. Problems in critical care. — Philadelphia: J.B. Lippincott, 1987. — Vol. 1. — P. 576-587.
38. Horton J. Cardiac response to fluid resuscitation from hemorrhagic shock / J. Horton, R. Landreau, T. Tuggle // Surg. Gynecol. Obstet. — 1985. — Vol. 260. — P. 444-452.
39. Steurer M.A. Infusion therapy for neonates, infants and children / M.A. Steurer, T.M. Berger // Anaesthesist. — 2011. — P. 13.
40. Murat I. Perioperative fluid therapy in pediatrics / I. Murat, M.C. Dubois // PediatricAnesthesia. — 2008. — P. 363-370.
41. Handy J.M. Physiological effects of hyperchloraemia and acidosis / J.M. Handy, N. Soni // Br. J. Anaesth. — 2008. — Vol. 101. — P. 141-150.
42. A comparison of albumin and saline for fluid resuscitation in the intensive care unit / S. Finfer, R. Bellomo, N. Boyce [et al.] // New. Engl. J. Med. — 2004. — Vol. 350. — P. 2247-2256.
43. Assessment of hemodynamic efficacy and safety of 6% hydroxyethylstarch 130/0.4 vs. 0.9% NaCl fluid replacement in patients with severe sepsis: the CRYSTMAS study / B. Guidet, O. Martinet, T. Boulain [et al.] // Crit. Care. — 2012. — Vol. 16. — P. 94.
44. Brain Trauma FoundationAmerican Association of Neurological SurgeonsCongress of Neurological Surgeons. Guidelines for the management of severe traumatic brain injury / Brain Trauma // J. Neurotrauma. — 2007. — Vol. 24. — S1-S106.
45. Hyperglycemic crisis in adult patients with diabetes (Consensus Statement) / A.E. Kitabchi, G.E. Umpierrez, J.M. Miles [et al.] // Diabetes Care. — 2009. — Vol. 32. — P. 1335-1343.
46. Fluid resuscitation in neonatal and pediatric hypovolemic shock: a Dutch Pediatric Society evidence-based clinical practice guideline / N. Boluyt, C.W. Bollen, A.P. Bos [et al.] // Intensive Care Med. — 2006. — Vol. 32. — P. 995-1003.
47. Major complications, mortality, and resource utilization after open abdominal surgery: 0.9% saline compared to Plasma-Lyte / A.D. Shaw, S.M. Bagshaw, S.L. Goldstein [et al.] // Ann. Surg. — 2012. — Vol. 255. — P. 821-829.
48. Association between a chloride-liberal vs chloride-restrictive intravenous fluid administration strategy and kidney injury in critically ill adults / N.M. Yunos, R. Bellomo, C. Hegarty [et al.] // JAMA. — 2012. — Vol. 30. — P. 1566-1572.
49. Kellum J.A. Hyperchloremic acidosis increases circulating inflammatory molecules in experimental sepsis / J.A. Kellum, M. Song, E. Almasri // Chest. — 2006. — Vol. 130. — P. 962-967.
50. Influence of acidosis and hypoxia on liver ischemia and reperfusion injury in an in vivo rat model / B.H. Heijnen, Y. Elkhaloufi, I. Straatsburg [et al.] // J. Appl Physiol. — 2002. — Vol. 93. — P. 319-323.
51. Bonventre J.V. Effects of metabolic acidosis on viability of cells exposed to anoxia / J.V. Bonventre, J.Y. Cheung // Am. J. Physiol. — 1985. — Vol. 249. — P. 149-159.
52. Morgan T.J. The meaning of acid-base abnormalities in the intensive care unit: part III — effects of fluid administration / T.J. Morgan // Crit. Care. — 2005. — Vol. 9. — P. 204-211.
53. Crystalloid or colloid fluid loading and pulmonary permeability, edema, and injury in septic and non septic critically ill patients with hypovolemia / M. Van der Heijden, J. Verheij, G. P. van Nieuw Amerongen [et al.] // Crit. Care Med. — 2009. — Vol. 37. — P. 1275-1281.
54. Sellards A.W. Tolerance for alkalis in Asiatic cholera / A.W. Sellards // Philippine J. Sci. — 1910. — № 5. — P. 363-390.
55. Hartmann A.F. Studies in the metabolism of sodium r-lactate. I. Response of normal human subjects to the intravenous injection of sodium r-lactate / A.F. Hartmann, M.J. Senn // J. Clin. Invest. — 1932. — № 11. — P. 327-335.
56. Crystalloids vs. colloids in fluid resuscitation. A systematic review / P.T. Choi, G. Yip, L.G. Quinonez, D.J. Cook // Crit. Care Med. — 1999. — Vol. 27. — P. 200-210
57. Forderungen und Erwartungen an einen optimalen Volumenersatz / R. Zander, H.A. Adams, J. Boldt [et al.] // Anästhesiol Intensivmed Notfallmed Schmerzther. — 2005. — Vol. 40.
58. Zander R. Base Excess und Laktatkonzentration von nfusionslösungen und Blutprodukten / R. Zander // Anästhesiol Intensivmed Notfallmed Schmerzther. — 2002. — Vol. 37. — P. 359-363.
59. Grifiith С.А. Natl Intravenous Therapy Association. — 1986. — № 9. — P. 480-3.
60. Berry M.N. The liver and lactic acidosis / M.N. Berry // Proc. R. Soc. Med. — 1967. — Vol. 60. — P. 1260-1262.
61. Siegal G. Basic Neurochemistry (molecular, cellular an medica aspects) / G. Siegal B. Agranoff, R. Albers // 5th ed. — N-Y: Raven Press, 1994. — 1080 p.
62. Hennes H-J. Schädel-Hirn-Trauma / H-J. Hennes // Neuroanästhesie / J-P. Jantzen, W. Löffler, Eds. Stuttgart, 2001.
63. Zander R. Fluid Management / R. Zander. — 2009. — P. 26.

/130.jpg)
/131.jpg)