Журнал «Здоровье ребенка» 3 (71) 2016
Вернуться к номеру
Транзиторный неонатальный сахарный диабет, ассоциированный с нарушением импринтинга хромосомы 6q24 Часть 4. Дифференциальная диагностика и лечение
Авторы: Абатуров А.Е., Никулина А.А., Русакова Е.А. - ГУ «Днепропетровская медицинская академия Министерства здравоохранения Украины», г. Днепр, Украина; Гирина И.А., Лыбенко Н.Н. - КУ «Днепропетровская ГДКБ № 1» ДОС, г. Днепр, Украина
Рубрики: Педиатрия/Неонатология
Разделы: Справочник специалиста
Версия для печати
У статті наведена диференціальна діагностика захворювань, що перебігають із неонатальною гіперглікемією. Указані загальні причини гіперглікемії в новонароджених, варіанти її поєднання з клінічними проявами з боку різних органів і систем. У статті запропонований алгоритм вибору лікувальних заходів при TNDM. Описані особливості дієти в новонароджених, проведення інсулінотерапії та інші напрямки медикаментозного лікування. Надано інформацію про медичні фонди синдрому, яку можна використовувати в процесі організації діагностики та лікування дітей із 6q24-TNDM.
В статье представлена дифференциальная диагностика заболеваний, протекающих с неонатальной гипергликемией. Указаны общие причины гипогликемии у новорожденных, варианты ее сочетания с клиническими проявлениями со стороны различных органов и систем. В статье предложен алгоритм выбора лечебных мероприятий при TNDM. Описаны особенности диеты у новорожденных, проведение инсулинотерапии и другие направления медикаментозного лечения. Предоставлена информация о медицинских фондах синдрома, которую можно использовать в процессе организации диагностики и лечения у детей с 6q24-TNDM.
The article presents the differential diagnosis of diseases that occur with neonatal hyperglycemia. The common causes of neonatal hypoglycemia, variants of its combination with clinical manifestations from the various organs and systems are indicated. There was presented an algorithm for the choice of therapeutic measures in transient neonatal diabetes mellitus (TNDM). The features of diet in newborns, insulin therapy and other directions of drug treatment were described. There was provided the information about medical funds of this syndrome, which can be used in the organization of the diagnosis and treatment in children with 6q24-TNDM.
неонатальний цукровий діабет, диференціальна діагностика, лікування.
неонатальный сахарный диабет, дифференциальная диагностика, лечение.
neonatal diabetes, differential diagnosis, treatment.
Статья опубликована на с. 143-148
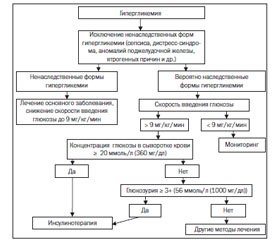
Дифференциальная диагностика 6q24-TNDM
Терапия
/146.jpg)
Диета
Инсулинотерапия
Препараты инсулина
Пути введения инсулина
Внутривенное введение
Расчет дозы инсулина
Осложнения инсулинотерапии
Другие направления медикаментозного лечения
Профилактика
Медицинские фонды синдрома
1. Kao L.S. Hyperglycemia and morbidity and mortality in extremely low birth weight infants / L.S. Kao, B.H. Morris, K.P. Lally et al. // J. Perinatol. — 2006 Dec. — 26 (12). — 730-6. doi:10.1038/sj.jp.7211593.
2. Flechtner I. Neonatal hyperglycaemia and abnormal development of the pancreas / I. Flechtner, M. Vaxillaire, H. Cavé et al. // Best Pract. Res. Clin. Endocrinol. Metab. — 2008 Feb. — 22 (1). — 17-40. doi: 10.1016/j.beem.2007.08.003.
3. Małecki M., Skupień J. Problems in differential diagnosis of diabetes types // Pol. Arch. Med. Wewn. — 2008 Jul-Aug. — 118 -(7-8). — 435-40. PMID: 18714740.
4. Decaro M.H., Vain N.E. Hyperglycaemia in preterm neonates: what to know, what to do // Early Hum. Dev. — 2011 Mar. — 87, Suppl. 1. — S19-22. doi: 10.1016/j.earlhumdev.2011.01.005.
5. Sabzehei M.K. Hyperglycemia in VLBW infants; incidence, risk factors and outcome / M.K. Sabzehei, S.A. Afjeh, M. Shakiba et al. // Arch. Iran. Med. — 2014 Jun. — 17 (6). — 429-34. doi: 014176/AIM.0010.
6. Bansal A. Glucocorticoid-induced preterm birth and neonatal hyperglycemia alter ovine beta cell development / A. Bansal, F.H. Bloomfield, K.L. Connor et al. // Endocrinology. — 2015 Jul 23: en20151095.
7. Flanagan S.E. Mutations in ATP-sensitive K+ channel genes cause transient neonatal diabetes and permanent diabetes in childhood or adulthood / S.E. Flanagan, A.M. Patch, D.J. Mackay et al. // Diabetes. — 2007 Jul. — 56 (7). — 1930-7. doi: 10.2337/db07-0043.
8. Edghill E.L., Flanagan S.E., Ellard S. Permanent neonatal diabetes due to activating mutations in ABCC8 and KCNJ11 // Rev. Endocr. Metab. Disord. — 2010 Sep. — 11 (3). — 193-8. doi: 10.1007/s11154-010-9149-x.
9. Habeb A.M. Permanent neonatal diabetes: different aetiology in Arabs compared to Europeans / A.M. Habeb, S.E. Flanagan, A. Deeb et al. // Arch. Dis. Child. — 2012 Aug. — 97 (8). — 721-3. doi: 10.1136/archdischild‑2012-301744
10. Greeley S.A. Neonatal diabetes mellitus: a model for personalized medicine / S.A. Greeley, S.E. Tucker, R.N. Naylor et al. // Trends Endocrinol. Metab. — 2010 Aug. — 21 (8). — 464-72. doi: 10.1016/j.tem.2010.03.004.
11. Naylor R.N. Genetics and pathophysiology of neonatal diabetes mellitus / R.N. Naylor, S.A. Greeley, G.I. Bell, L.H. Philipson // J. Diabetes Investig. — 2011 Jun 5. — 2 (3). — 158-69. doi: 10.1111/j.2040-1124.2011.00106.x.
12. Rubio-Cabezas O., Ellard S. Diabetes mellitus in neonates and infants: genetic heterogeneity, clinical approach to diagnosis, and therapeutic options // Horm Res. Paediatr. — 2013. — 80 (3). — 137-46. doi: 10.1159/000354219.
13. Stein S.A., Maloney K.L., Pollin T.I. Genetic Counseling for Diabetes Mellitus // Curr. Genet. Med. Rep. — 2014 Jun 1. — 2 (2). — 56-67. doi: 10.1007/s40142-014-0039-5.
14. Rubio-Cabezas O. ISPAD Clinical Practice Consensus Guidelines 2014. The diagnosis and management of monogenic diabetes in children and adolescents / O. Rubio-Cabezas, A.T. Hattersley, P.R. Njølstad, W. Mlynarski, S. Ellard, N. White, D.V. Chi, M.E. Craig. International Society for Pediatric and Adolescent Diabetes // Pediatr. Diabetes. — 2014 Sep. — 15 Suppl. 20. — 47-64. doi: 10.1111/pedi.12192.
15. Demirbilek H. Clinical characteristics and molecular genetic analysis of 22 patients with neonatal diabetes from the South-Eastern region of Turkey: predominance of non-KATP channel mutations / H. Demirbilek, V.B. Arya, M.N. Ozbek et al. // Eur. J. Endocrinol. — 2015 Jun. — 172 (6). — 697-705. doi: 10.1530/EJE‑14-0852.
16. Passanisi S. Treatment of transient neonatal diabetes mellitus: insulin pump or insulin glargine? Our experience / S. Passanisi, T. Timpanaro, D. Lo Presti, C. Mammí, M. Caruso-Nicoletti // Diabetes Technol. Ther. — 2014 Dec. — 16 (12). — 880-4. doi: 10.1089/dia.2014.0055.
17. Kairamkonda V.R., Khashu M. Controversies in the management of hyperglycemia in the ELBW infant // Indian. Pediatr. — 2008 Jan. — 45 (1). — 29-38. PMID: 18250502.
18. Smart C., Aslander-van Vliet E., Waldron S. Nutritional management in children and adolescents with diabetes // Pediatr. Diabetes. — 2009 Sep. — 10, Suppl. 12. — 100-17. doi: 10.1111/j.1399-5448.2009.00572.x.
19. Karges B. Management of diabetes mellitus in infants / B. Karges, T. Meissner, A. Icks, T. Kapellen, R.W. Holl // Nat. Rev. Endocrinol. — 2011 Nov 29. — 8 (4). — 201-11. doi: 10.1038/nrendo.2011.204.
20. Karp T.B., Scardino C., Butler L.A. Glucose metabolism in the neonate: the short and sweet of it // Neonatal Netw. — 1995 Dec. — 14 (8). — 17-23. PMID: 8552013.
21. Hume R. Glucose homeostasis in the newborn / R. Hume, A. Burchell, F.L. Williams, D.K. Koh // Early Hum. Dev. — 2005 Jan. — 81 (1). — 95-101. doi: http: // dx.doi.org/10.1016/j.earlhumdev.2004.10.005.
22. Milcic T.L. Neonatal glucose homeostasis // Neonatal Netw. — 2008 May-Jun. — 27 (3). — 203-7. Doi: http: // dx.doi.org/10.1891/0730-0832.27.3.203.
23. Thureen P.J. Early aggressive nutrition in the neonate // Pediatr. Rev. — 1999 Sep. — 20 (9). — e45-55. Review. No abstract available. PMID: 10473666.
24. Barone J.V., Tillman E.M., Ferry R.J. Jr. Treatment of transient neonatal diabetes mellitus with subcutaneous insulin glargine in an extremely low birth weight neonate // J. Pediatr. Pharmacol. Ther. — 2011 Oct. — 16 (4). — 291-7. doi: 10.5863/1551-6776-16.4.291.
25. Polak M., Cavй H. Neonatal diabetes mellitus: a disease linked to multiple mechanisms // Orphanet J. Rare Dis. — 2007 Mar 9. — 2. — 12 doi: 10.1186/1750-1172-2-12.
26. Kearns G.L. Developmental pharmacology — drug disposition, action, and therapy in infants and children / G.L. Kearns, S.M. Abdel-Rahman, S.W. Alander et al. // N. Engl. J. Med. — 2003 Sep 18. — 349 (12). — 1157-67. doi: 10.1056/NEJMra.
27. Beardsall K., Pesterfield C.L., Acerini C.L. Neonatal diabetes and insulin pump therapy // Arch. Dis. Child Fetal Neonatal Ed. — 2011 May. — 96 (3). — F223-4. doi: 10.1136/adc.2010.196709.
28. Park J.H. Insulin pump therapy in transient neonatal diabetes mellitus / J.H. Park, J.H. Kang, K.H. Lee et al. // Ann. Pediatr. Endocrinol. Metab. — 2013 Sep. — 18 (3). — 148-51. doi: 10.6065/apem.2013.18.3.148.
29. Bharucha T. Neonatal diabetes mellitus: Insulin pump as an alternative management strategy / T. Bharucha, J. Brown, C. McDonnell et al. // J. Paediatr. Child Health. — 2005 Sep-Oct. — 41 -(9-10). — 522-6. doi: 10.1111/j.1440-1754.2005.00696.x.
30. Tubiana-Rufi N. Insulin pump therapy in neonatal diabetes // Endocr. Dev. — 2007. — 12. — 67-74. PMID: 17923770.
31. Hoffmann A., Spengler D. Transient neonatal diabetes mellitus gene Zac1 impairs insulin secretion in mice through Rasgrf1 // Mol. Cell. Biol. — 2012 Jul. — 32 (13). — 2549-60. doi: 10.1128/MCB.06637-11.

/144.jpg)
/145.jpg)
/146_2.jpg)